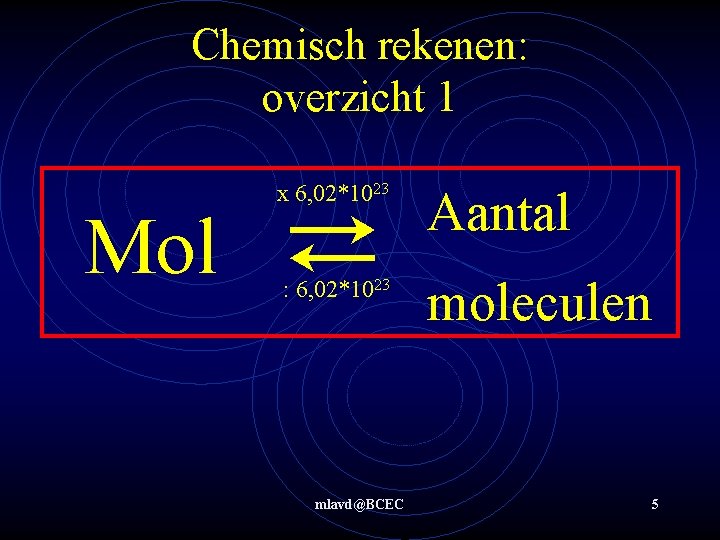
Hoeveel Deeltjes Is 1 Mol

Dus je zit hier, lekker aan je koffie, en je vraagt je ineens af: "Hoeveel deeltjes zit er nou eigenlijk in zo'n mol? En waarom zou ik dat überhaupt willen weten?!" Nou, relax, want ik ga het je vertellen, en ik beloof je dat het (misschien) minder saai is dan het klinkt. Stel je voor: je bent op een date, en je wilt indruk maken met je kennis over… chemie. Romantisch, toch?
Wat is een Mol, überhaupt?
Oké, dus een mol. Het is geen klein, harig diertje dat je tuin sloopt. Hoewel, als je tuin verpest wordt door iets kleins en onzichtbaars… dan zou het theoretisch gezien wél een chemische mol kunnen zijn! Nee, grapje. Een mol is eigenlijk een getal. Een enorm, belachelijk groot getal. Zo groot, dat als je het hardop zou zeggen, je waarschijnlijk al dood bent voordat je klaar bent. Maar wat ís dat getal dan?
Het is 6.022 x 1023. Wacht, niet wegrennen! Ik snap dat het er intimiderend uitziet. Maar denk er zo over: het is een 6 met 23 nullen erachter. Dat zijn dus 602,200,000,000,000,000,000,000 deeltjes! Stel je voor, je hebt zoveel sokken. Nooit meer sokken kwijt! Oké, misschien nog wel…
Must Read
Waarom zo'n gigantisch getal?
Waarom hebben we zo'n absurd groot getal nodig? Nou, dat komt omdat we over atomen en moleculen praten. Die zijn zó klein, dat je er biljoenen nodig hebt om überhaupt iets mee te kunnen. Als je een druppel water hebt, zitten daar al meer moleculen in dan er sterren zijn in het zichtbare universum. (Oké, misschien niet meer, maar het zit er dichtbij!)
Denk het zo: Stel je voor dat je mieren moet tellen. Je gaat toch niet elke mier apart zitten tellen? Je pakt een grote schep mieren en schat hoeveel mieren er in die schep zitten, en dan vermenigvuldig je dat met het aantal scheppen dat je hebt. De mol is een beetje zoals die "schep". Het is een handige manier om een heleboel atomen of moleculen te tellen.

Avogadro's Getal: De Held van de Mol
Die 6.022 x 1023, dat is dus het getal van Avogadro. Ja, een Italiaanse wetenschapper. En nee, ik weet ook niet hoe hij het precies heeft uitgevogeld. Waarschijnlijk met een hoop rare apparaten, koffie en een flinke dosis Italiaanse flair. Het verhaal gaat dat hij 's nachts droomde over een gigantische stapel atomen... Ik denk dat hij iets te veel pasta had gegeten die avond.
Wat kun je doen met een Mol?
Nu komt het leuke gedeelte! Wat kun je nou eigenlijk doen met zo'n mol? Nou, je kunt er bijvoorbeeld berekeningen mee maken! Stel je voor, je hebt een recept nodig voor een taart, maar het recept staat in mollen. Dan kun je met behulp van het getal van Avogadro uitrekenen hoeveel gram suiker, bloem, of chocolade je nodig hebt.
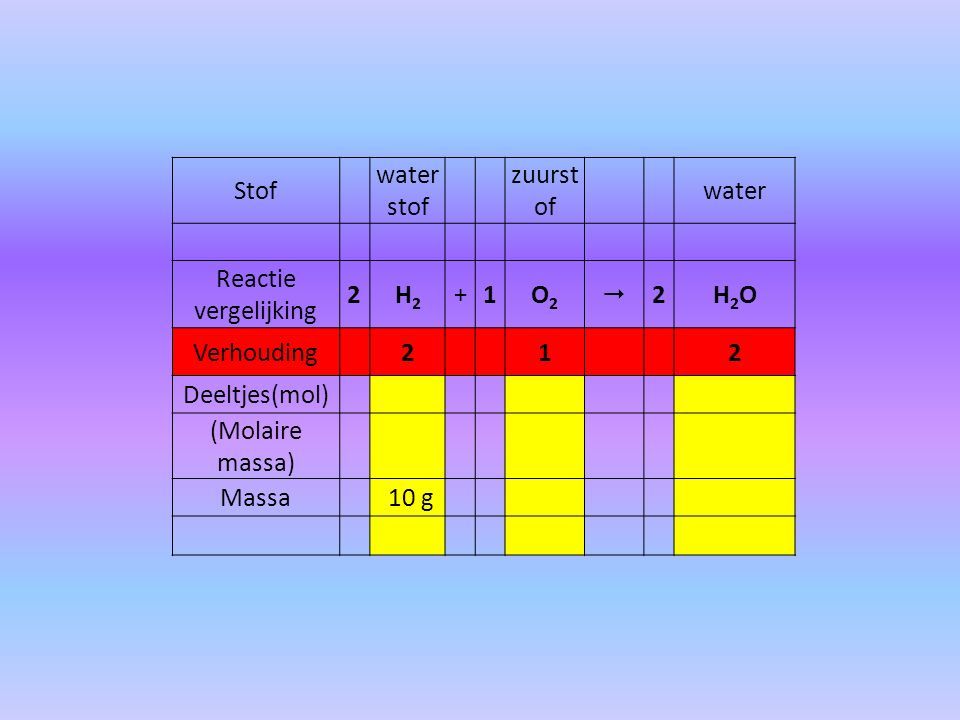
Kijk, stel je wilt water (H2O) maken. Je weet dat één watermolecuul bestaat uit twee waterstofatomen (H) en één zuurstofatoom (O). Met behulp van de mol kan je dan uitrekenen hoeveel gram waterstof en zuurstof je nodig hebt om een bepaalde hoeveelheid water te maken. Cool, toch?
- Taarten bakken: Zoals ik al zei, recepten omrekenen.
- Medicijnen maken: De juiste verhoudingen van ingrediënten bepalen is cruciaal.
- Raketbrandstof mengen: Zodat je niet per ongeluk de boel opblaast (of juist wél, als je dat de bedoeling is).
- Nieuwe materialen ontwerpen: Door de eigenschappen van atomen en moleculen te begrijpen.
Mollen in het dagelijks leven (of toch niet?)
Oké, eerlijk is eerlijk, je zult waarschijnlijk niet elke dag mollen tegenkomen. Tenzij je een scheikundige bent, natuurlijk. Maar zelfs dan, ga je niet rondlopen met een mol suiker in je zak. Tenzij je echt van suiker houdt… dan ben je misschien wel een beetje gek.
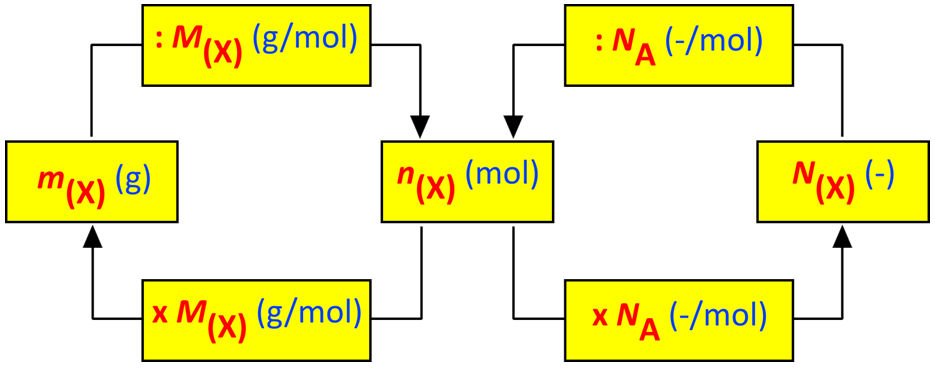
Maar de principes achter de mol, die zijn wél belangrijk. Ze helpen ons de wereld om ons heen te begrijpen. Van de lucht die we inademen tot het water dat we drinken, alles bestaat uit atomen en moleculen. En de mol is een handige manier om die atomen en moleculen te kwantificeren.
Stel je voor, je probeert uit te leggen aan je oma hoeveel pixels er in haar nieuwe tv zitten. Je kan niet elk pixel apart aanwijzen! Je moet een soort ‘eenheid’ gebruiken, zoals bijvoorbeeld het aantal megapixels. De mol is de ‘megapixels’ van de scheikunde.

Grappige Mol-feitjes (om je vrienden mee te imponeren)
- Als je een mol knikkers zou hebben, zouden ze de hele planeet Aarde bedekken met een laag van 80 kilometer dik! Pas op dat je niet struikelt!
- Als je een mol dollarbiljetten zou hebben, zou je er elke seconde één miljard dollar aan uit kunnen geven, en dan nog zou je er meer dan 19 miljoen jaar over doen om alles uit te geven! (Misschien toch maar een mol dollarbiljetten bestellen?)
- Als je een mol mieren op een rij zou zetten, zou de rij miljarden keren de afstand van de aarde naar de zon overbruggen! Hopelijk hebben ze een goede navigatie!
Conclusie: De Mol is Cool (echt waar!)
Dus, daar heb je het. De mol is misschien een beetje een abstract concept, maar het is eigenlijk best wel cool. Het is een handige manier om atomen en moleculen te tellen, en het helpt ons de wereld om ons heen te begrijpen. En wie weet, misschien kun je er zelfs je date mee imponeren. (Alhoewel, misschien toch eerst vragen of ze geïnteresseerd zijn in scheikunde…)
Onthoud: Een mol is 6.022 x 1023. En onthoud ook: scheikunde kan best leuk zijn! (Vooral als je er taarten mee kunt bakken.) Nu, ga je gang, en strooi rond met je nieuwe kennis. Je bent nu officieel een mol-expert. Gefeliciteerd!
En als je je ooit afvraagt waar al die deeltjes heen gaan… nou, dat is weer een verhaal voor een andere keer, met een andere koffie, en misschien wel een taart gebakken volgens een recept in mollen.