Wat Is Een Peptide Binding
_Image 3_Dutch.1600708639833-24ca7cd4b6dd01e3152a6935f46d4085.jpg)
Welkom bij dit artikel over de peptidebinding, een cruciale chemische binding die de bouwstenen van het leven – eiwitten – bij elkaar houdt. Eiwitten zijn essentieel voor vrijwel elke functie in ons lichaam, van het transporteren van zuurstof tot het katalyseren van chemische reacties. Om de complexiteit en diversiteit van eiwitten te begrijpen, is het fundamenteel om de aard van de peptidebinding te begrijpen. In dit artikel duiken we dieper in wat een peptidebinding precies is, hoe deze gevormd wordt, en waarom deze zo belangrijk is voor de werking van levende organismen.
De Basis: Wat is een Peptidebinding?
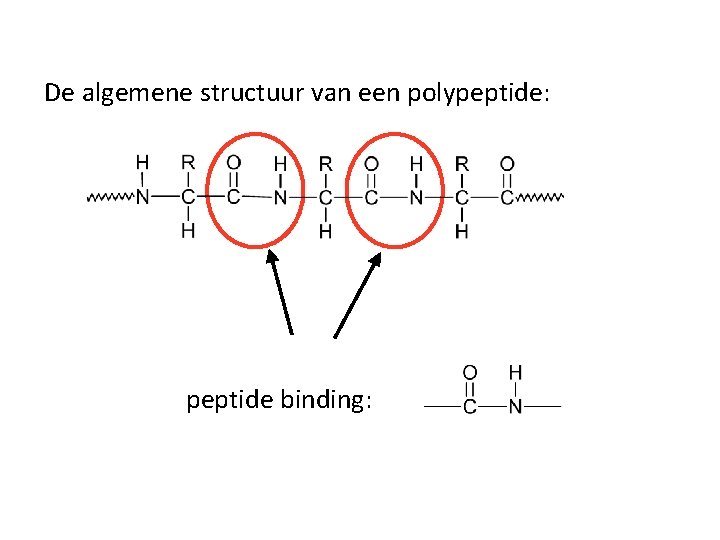
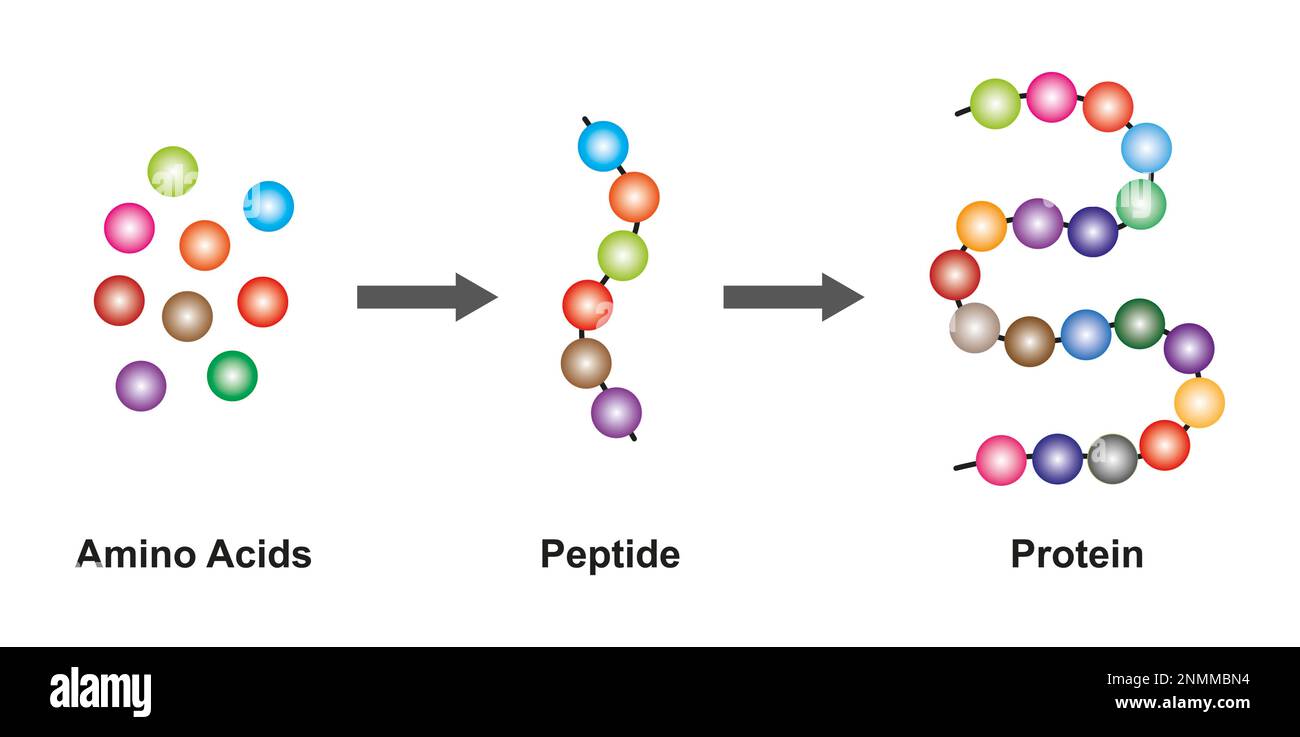
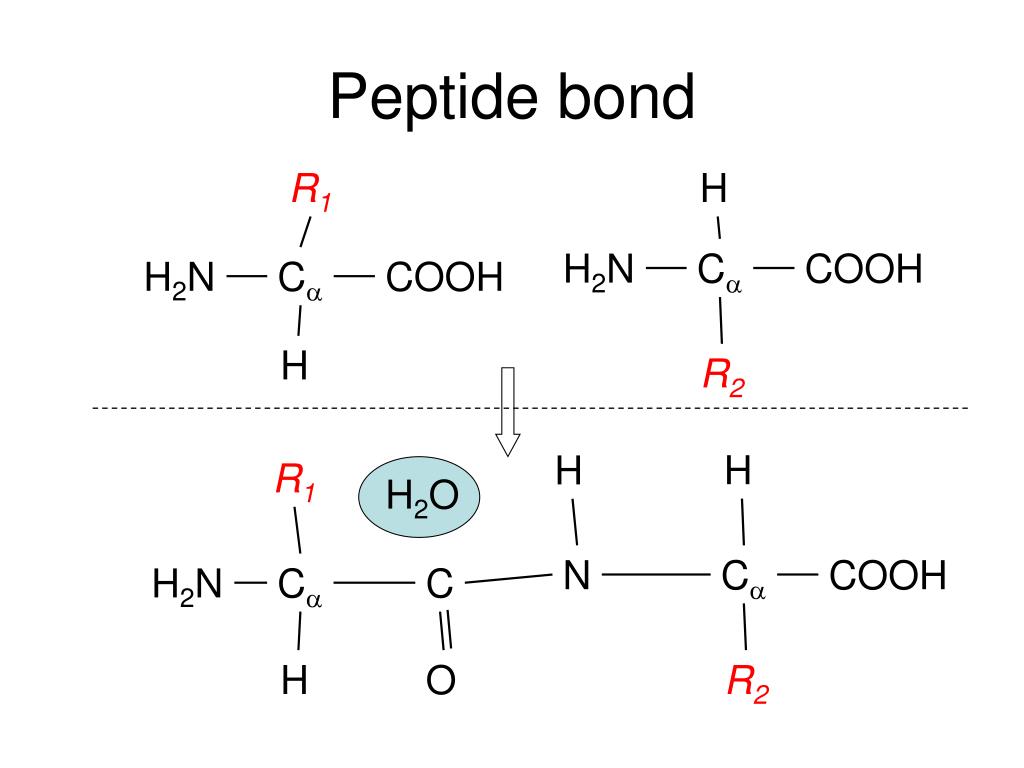
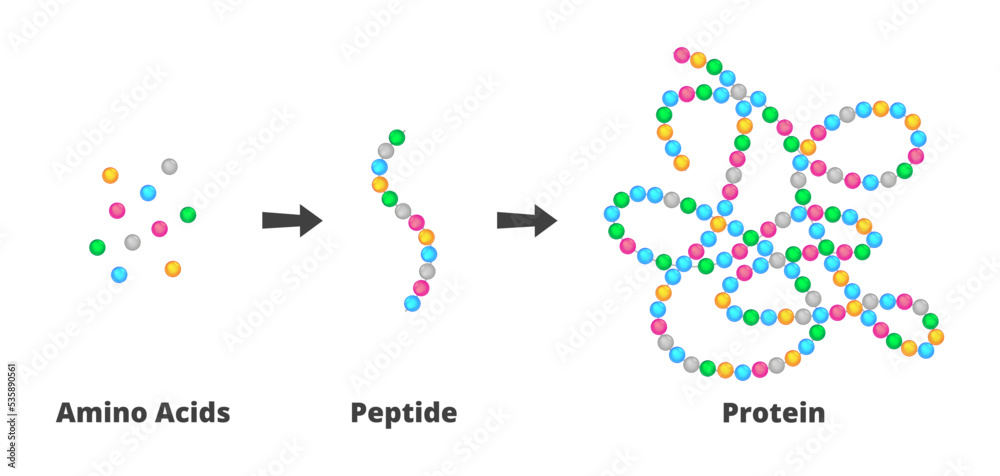
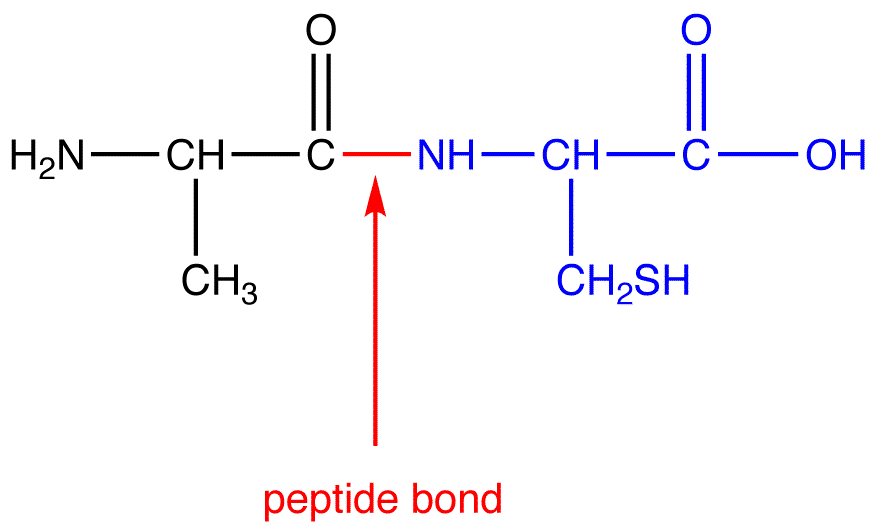
Een peptidebinding is een chemische binding die ontstaat tussen twee aminozuren. Aminozuren zijn de bouwstenen van eiwitten. Elk aminozuur heeft een aminogroep (-NH2) en een carboxylgroep (-COOH). De peptidebinding wordt gevormd wanneer de carboxylgroep van het ene aminozuur reageert met de aminogroep van een ander aminozuur. Deze reactie resulteert in de afsplitsing van een watermolecuul (H2O), en daarom wordt het ook wel een condensatiereactie of dehydratatiereactie genoemd.
De Chemische Structuur
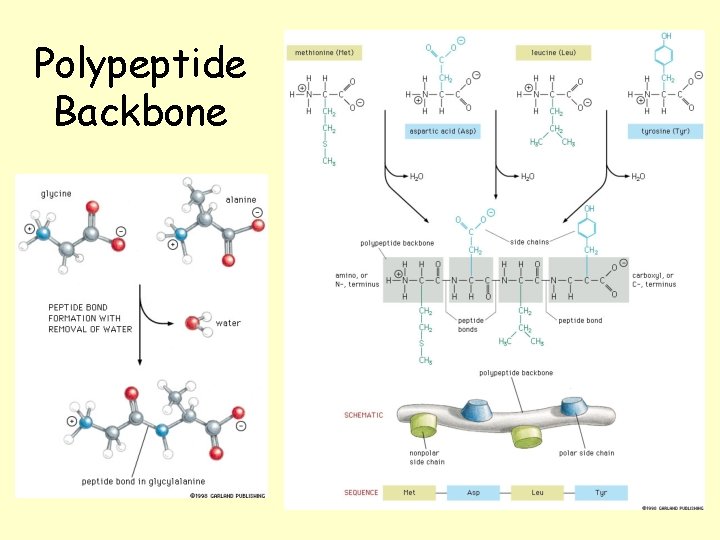
De resulterende binding tussen de koolstofatoom van de carboxylgroep en de stikstofatoom van de aminogroep wordt de peptidebinding genoemd. Chemisch gezien is de peptidebinding een amidebinding. De structuur is als volgt: -CO-NH-. Het is belangrijk om te begrijpen dat deze binding een gedeeltelijk dubbelbindingskarakter heeft vanwege de resonantie van elektronen tussen de koolstof-, zuurstof- en stikstofatomen. Dit gedeeltelijk dubbelbindingskarakter zorgt ervoor dat de peptidebinding vlak is (planair), wat betekent dat de zes atomen die direct betrokken zijn bij de binding (C, O, N, H, en de twee α-koolstofatomen van de aminozuren) zich in hetzelfde vlak bevinden.
Must Read
Vorming van de Peptidebinding
De vorming van een peptidebinding is een energetisch ongunstig proces in de cel. Dit betekent dat er energie nodig is om de binding te vormen. In levende organismen wordt deze energie geleverd door ATP (adenosinetrifosfaat), de belangrijkste energiebron van de cel. Het proces wordt gekatalyseerd door ribosomen, complexe moleculaire machines die in het cytoplasma van cellen voorkomen. Ribosomen begeleiden de aminozuren naar de juiste positie en faciliteren de vorming van de peptidebinding.
Het Proces in Detail
Het proces begint met een tRNA-molecuul (transfer RNA) dat een specifiek aminozuur naar het ribosoom brengt. Het tRNA-molecuul herkent een specifiek codon (een reeks van drie nucleotiden) op het mRNA (messenger RNA), dat de genetische code bevat voor het eiwit dat gesynthetiseerd wordt. Wanneer het tRNA-molecuul met het juiste aminozuur op de juiste positie op het ribosoom is aangekomen, wordt de peptidebinding gevormd tussen het aminozuur op het tRNA en de groeiende polypeptideketen. Nadat de peptidebinding is gevormd, verplaatst het ribosoom zich over het mRNA om het volgende codon te lezen en het proces te herhalen.

Belangrijke Eigenschappen van de Peptidebinding
De peptidebinding heeft een aantal belangrijke eigenschappen die cruciaal zijn voor de structuur en functie van eiwitten. Deze eigenschappen zijn direct gerelateerd aan de chemische structuur van de binding.
Planairiteit en Rotatiebeperking
Zoals eerder vermeld, is de peptidebinding planair vanwege het gedeeltelijk dubbelbindingskarakter. Dit betekent dat de rotatie rond de peptidebinding sterk beperkt is. Dit heeft een belangrijke invloed op de vouwing van het eiwit. De enige rotatie die mogelijk is, vindt plaats rond de bindingen van de α-koolstofatomen van de aminozuren. Deze rotaties worden beschreven door de Ramachandran plot, een grafiek die de toegestane rotaties weergeeft op basis van sterische hindering tussen de verschillende atomen in de aminozuurresiduen.
Polariteit
De peptidebinding is polair. Het zuurstofatoom in de carbonylgroep (C=O) is meer elektronegatief dan het koolstofatoom, waardoor het zuurstofatoom een partiële negatieve lading draagt en het koolstofatoom een partiële positieve lading. Op dezelfde manier is de stikstofatoom in de amidegroep (N-H) meer elektronegatief dan het waterstofatoom, waardoor de stikstofatoom een partiële negatieve lading draagt en het waterstofatoom een partiële positieve lading. Deze polariteit maakt waterstofbrugvorming mogelijk, wat essentieel is voor de stabilisatie van de secundaire en tertiaire structuur van eiwitten.

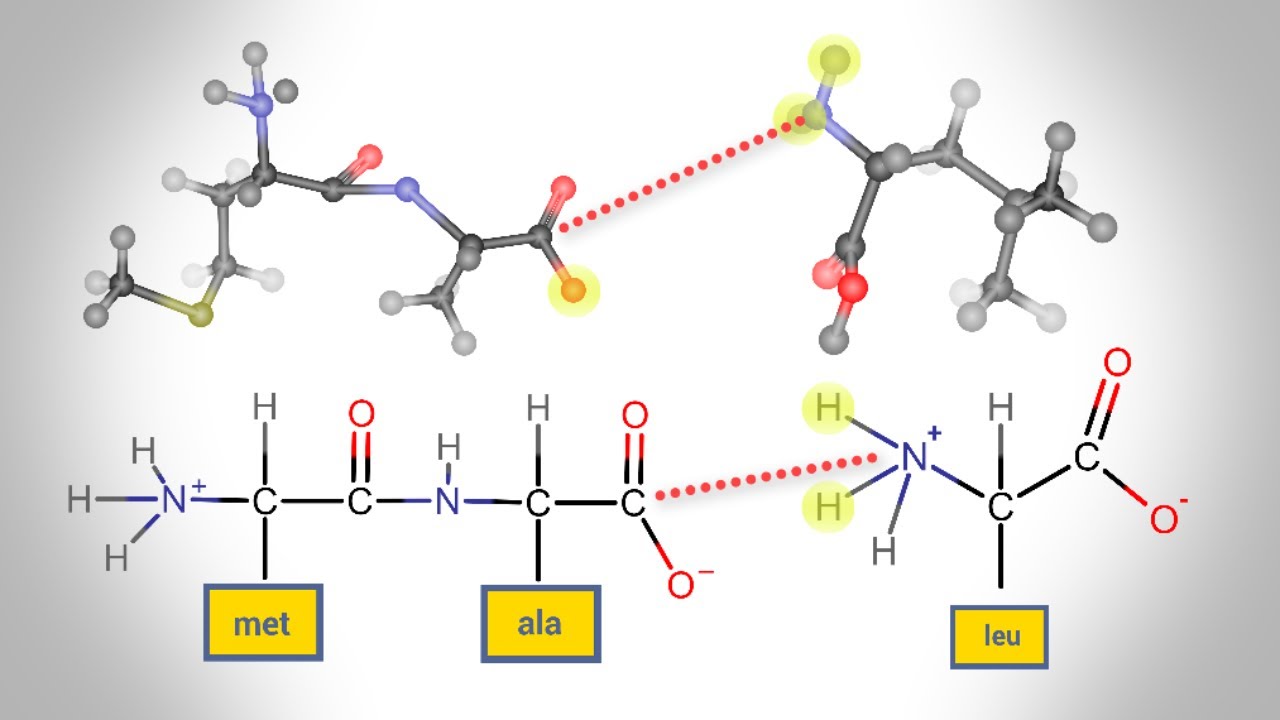
Waterstofbrugvorming
De waterstofatomen gebonden aan de stikstofatomen in de peptidebinding kunnen waterstofbruggen vormen met de zuurstofatomen van andere peptidebindingen of met andere atomen in de eiwitstructuur. Deze waterstofbruggen spelen een cruciale rol bij het stabiliseren van de α-helices en β-sheets, de belangrijkste secundaire structuren van eiwitten. Ze dragen ook bij aan de algemene stabiliteit van de driedimensionale structuur van het eiwit.
Real-World Voorbeelden en Data
De peptidebinding is van vitaal belang in tal van biologische processen. Hier zijn enkele voorbeelden om het belang ervan te illustreren:
Enzymen
Enzymen, de biologische katalysatoren van de cel, zijn eiwitten die reacties versnellen. De specifieke driedimensionale structuur van een enzym, die bepaald wordt door de peptidebindingen en de daaruit voortvloeiende vouwing van de polypeptideketen, is cruciaal voor de enzymatische activiteit. De actieve site van een enzym, waar de reactie plaatsvindt, is afhankelijk van de nauwkeurige positionering van aminozuurresiduen, die weer bepaald wordt door de peptidebindingen.

Hormonen
Veel hormonen, zoals insuline en groeihormoon, zijn peptiden of eiwitten. Hun werking is afhankelijk van hun specifieke structuur, die gevormd wordt door de peptidebindingen. Deze hormonen binden zich aan specifieke receptoren op cellen en activeren signaalcascades die verschillende fysiologische processen reguleren.
Structurele Eiwitten
Structurele eiwitten, zoals collageen en keratine, bieden steun en structuur aan weefsels en organen. Collageen, bijvoorbeeld, is het meest voorkomende eiwit in het menselijk lichaam en vormt de basis van bindweefsel, huid, botten en kraakbeen. De peptidebindingen in collageen zorgen voor de sterkte en flexibiliteit die nodig zijn voor deze structurele functie.
Farmaceutische Toepassingen
De kennis van de peptidebinding is essentieel in de farmaceutische industrie. Veel medicijnen zijn gebaseerd op peptiden of eiwitten, of ze zijn ontworpen om te interageren met eiwitten. Bijvoorbeeld, peptidegeneesmiddelen worden gebruikt voor de behandeling van diabetes, kanker en andere aandoeningen. Het begrijpen van hoe peptidebindingen de structuur en functie van deze medicijnen beïnvloeden, is cruciaal voor de ontwikkeling van effectieve therapieën.
Data: Studies naar de vouwing van eiwitten tonen aan dat de hoeken rond de peptidebinding (vooral phi en psi hoeken) beperkt zijn tot bepaalde waarden, zoals weergegeven in de Ramachandran plot. Afwijkingen van deze waarden kunnen leiden tot destabilisatie van de eiwitstructuur en verlies van functie.
Conclusie
De peptidebinding is een fundamentele chemische binding die de basis vormt van eiwitten, de werkpaarden van de cel. Het begrijpen van de structuur, vorming en eigenschappen van de peptidebinding is essentieel voor het begrijpen van de structuur en functie van eiwitten, en dus voor het begrijpen van de biologie van levende organismen. De polariteit, planariteit en de mogelijkheid tot waterstofbrugvorming spelen allemaal een cruciale rol bij het bepalen van de driedimensionale structuur van eiwitten en hun vermogen om specifieke functies uit te voeren.
Nu u een beter begrip heeft van de peptidebinding, kunt u dieper duiken in de wereld van de biochemie en moleculaire biologie. Overweeg om meer te leren over eiwitvouwing, enzymkinetiek, of de ontwikkeling van peptidegeneesmiddelen. De kennis van deze fundamentele bouwsteen van het leven opent deuren naar een dieper inzicht in hoe levende systemen functioneren en hoe we ziekten kunnen bestrijden. Blijf leren en ontdekken, want de wereld van de moleculaire biologie is oneindig fascinerend!