Wet Van Behoud Van Massa

Het beginsel van behoud van massa, ook wel bekend als de wet van Lavoisier, is een fundamenteel concept in de natuurwetenschappen, met name in de chemie en fysica. Het stelt dat de totale massa van een gesloten systeem constant blijft, ongeacht de processen die binnen dat systeem plaatsvinden. Dit betekent dat massa niet kan worden gecreëerd of vernietigd, alleen getransformeerd van de ene vorm naar de andere.
De Kern van het Behoud van Massa
Het behoud van massa is een empirische wet, wat betekent dat het gebaseerd is op herhaalde observaties en experimenten. Antoine Lavoisier, een Franse chemicus, wordt vaak gecrediteerd met de formulering van deze wet in de late 18e eeuw, hoewel het idee zelf al langer circuleerde. Lavoisier demonstreerde door middel van nauwkeurige experimenten dat bij chemische reacties de massa van de reagentia exact gelijk is aan de massa van de producten.
Belangrijke Aspecten
Er zijn een aantal belangrijke aspecten die bijdragen aan het begrijpen van de wet van behoud van massa:
Must Read
- Gesloten systeem: De wet geldt alleen voor gesloten systemen, dat wil zeggen systemen waarbij geen massa kan ontsnappen of binnendringen. Dit is cruciaal, omdat massa anders zou kunnen verdwijnen (lijken te verdwijnen) of verschijnen (lijken te verschijnen), wat de wet zou schenden.
- Chemische reacties: In chemische reacties worden atomen herschikt, maar ze verdwijnen niet en er komen er ook geen nieuwe bij. De massa van de atomen blijft constant.
- Fysische veranderingen: Ook bij fysische veranderingen, zoals het smelten van ijs of het koken van water, blijft de massa behouden. De aggregatietoestand verandert, maar de hoeveelheid materie blijft hetzelfde.
- Kernreacties (Uitzondering): Een belangrijke uitzondering op de wet van behoud van massa is de kernreactie. Hierbij wordt massa omgezet in energie, zoals beschreven door Einstein's beroemde formule E=mc². Echter, het behoud van massa-energie blijft wel gelden.
Uitleg Zonder Oversimplificatie
Hoewel het behoud van massa een relatief eenvoudig te begrijpen concept is, is het belangrijk om te erkennen dat de implementatie en interpretatie ervan in complexe situaties subtiel kunnen zijn. Bijvoorbeeld, in open systemen, waar massa kan uitwisselen met de omgeving, lijkt het behoud van massa mogelijk niet te gelden op het eerste gezicht. Denk aan een verbrandingsreactie: de rook die ontsnapt draagt massa weg, waardoor het lijkt alsof de massa afneemt.
De moderne interpretatie van het behoud van massa is nauw verbonden met het behoud van energie. Einstein's relativiteitstheorie heeft aangetoond dat massa en energie equivalent zijn. Daarom, in systemen waar significante hoeveelheden energie worden geproduceerd of verbruikt, zoals bij kernreacties, moet men het behoud van massa-energie beschouwen in plaats van alleen het behoud van massa. Het verschil is doorgaans verwaarloosbaar bij normale chemische reacties.
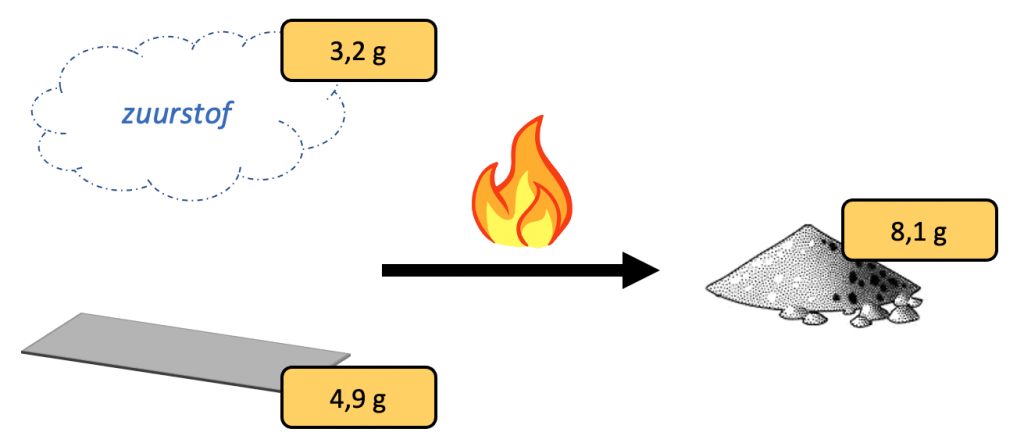
Het is ook belangrijk om te begrijpen dat "massa" verschillende betekenissen kan hebben, afhankelijk van de context. In de context van de speciale relativiteitstheorie onderscheidt men vaak tussen rustmassa (de massa van een object in rust) en relativistische massa (die toeneemt met de snelheid van het object). Het behoud van massa verwijst meestal naar het behoud van rustmassa.
Real-World Voorbeelden en Data
Het behoud van massa wordt in tal van industrieën en onderzoeksgebieden toegepast. Hier zijn enkele concrete voorbeelden:

Voorbeeld 1: Farmaceutische Industrie
In de farmaceutische industrie is het essentieel om de wet van behoud van massa toe te passen bij het synthetiseren van geneesmiddelen. Nauwkeurige metingen van reagentia en producten zijn vereist om de yield van een reactie te bepalen en om te garanderen dat de reactie verloopt zoals verwacht. Als er een verlies van massa is, kan dit wijzen op een probleem in het proces, zoals onvolledige reactie of verlies van product tijdens de zuivering.
Voorbeeld 2: Voedselverwerking
Bij de voedselverwerking wordt het behoud van massa gebruikt om de voedingswaarde van producten te controleren. Door de massa van de ingrediënten en de massa van het eindproduct te vergelijken, kan men nagaan of er sprake is van verlies van nutriënten tijdens de verwerking. Dit is cruciaal voor het waarborgen van de kwaliteit en veiligheid van voedingsmiddelen.
Voorbeeld 3: Milieubeheer
In het milieubeheer wordt het behoud van massa toegepast bij het monitoren van de verspreiding van vervuilende stoffen. Door de massa van een vervuilende stof op een bepaalde locatie te meten en te vergelijken met de massa op andere locaties, kan men de beweging van de vervuilende stof volgen en de bron van de vervuiling identificeren.
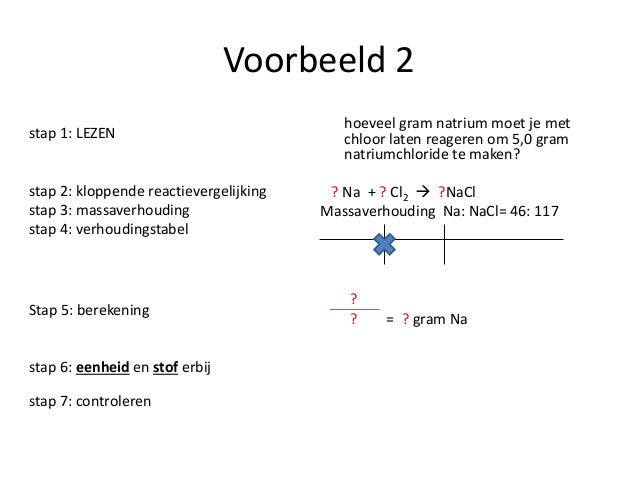
Voorbeeld 4: Verbranding van Hout
Stel, je verbrandt 1 kg hout. Na de verbranding blijft er een kleine hoeveelheid as over (bijvoorbeeld 50 gram). Waar is de rest van de massa gebleven? De 950 gram is omgezet in gassen zoals koolstofdioxide (CO2), waterdamp (H2O) en andere verbrandingsproducten. Deze gassen verdwijnen in de lucht, maar ze bevatten nog steeds de atomen die oorspronkelijk in het hout zaten. Als je alle gassen zou opvangen en wegen, zou je zien dat de totale massa van de as en de gassen gelijk is aan de oorspronkelijke massa van het hout plus de massa van de zuurstof die bij de verbranding is gebruikt.
Data en Kwantificatie
In experimenten wordt het behoud van massa vaak gedemonstreerd door chemische reacties in gesloten containers uit te voeren. Bijvoorbeeld, men kan een reactie tussen zilvernitraat (AgNO3) en natriumchloride (NaCl) in een afgesloten buis uitvoeren. De reactie produceert zilverchloride (AgCl), een wit neerslag, en natriumnitraat (NaNO3) in oplossing. Door de massa van de buis voor en na de reactie te meten, kan men aantonen dat de massa gelijk blijft (binnen de foutmarge van de meting).

Nauwkeurige metingen kunnen het behoud van massa tot op de miligram nauwkeurig aantonen, afhankelijk van de gebruikte apparatuur en de grootte van het systeem.
Conclusie en Oproep tot Actie
Het behoud van massa is een cruciaal en fundamenteel principe in de wetenschap, met wijdverspreide toepassingen in diverse disciplines. Het is belangrijk om dit principe te begrijpen en toe te passen bij het analyseren van systemen en processen.
Als studenten, onderzoekers of professionals is het essentieel om altijd kritisch te blijven en te overwegen of het behoud van massa van toepassing is in een bepaalde situatie. Begrijp de beperkingen van het principe en de uitzonderingen (zoals kernreacties). Door een dieper begrip van het behoud van massa kunnen we efficiëntere en duurzamere processen ontwerpen en implementeren, en beter inzicht krijgen in de complexe wereld om ons heen. Blijf onderzoeken, experimenteren en leren over de principes die de basis vormen van ons begrip van de natuur!