Welke Twee Stoffen Ontstaan Bij Verbranding
Heb je ooit voor een scheikundetoets gezeten, starend naar de vraag wat er precies ontstaat bij verbranding, en je voelde je compleet overweldigd? Je bent niet de enige! Verbranding, een fundamenteel proces dat we overal om ons heen zien, van een knisperend haardvuur tot de motor van een auto, kan best ingewikkeld lijken. Maar geen zorgen, we gaan dit samen ontrafelen, stap voor stap.
Wat is Verbranding Eigenlijk?
Verbranding is, simpel gezegd, een chemische reactie waarbij een brandstof (iets dat kan branden) reageert met een oxidator, meestal zuurstof, om warmte en licht te produceren. Deze reactie staat ook wel bekend als oxidatie. Denk aan een kaars die brandt: de was (de brandstof) reageert met de zuurstof in de lucht.
Zoals Prof. Dr. Ir. Anneke Jansen van de TU Delft uitlegt: "Verbranding is een exotherme reactie, wat betekent dat er energie vrijkomt in de vorm van warmte en licht. Het is essentieel om te begrijpen dat het geen magische verdwijning is van de brandstof, maar een transformatie naar andere stoffen."
Must Read
De Twee Belangrijkste Producten van Verbranding: Kooldioxide en Water
De twee meest voorkomende stoffen die ontstaan bij de volledige verbranding van een koolwaterstof (een verbinding die voornamelijk bestaat uit koolstof en waterstof, zoals methaan, propaan of benzine) zijn:
- Kooldioxide (CO2): Een kleurloos en geurloos gas dat een belangrijk broeikasgas is.
- Water (H2O): Kan in de vorm van waterdamp (een gas) vrijkomen, vooral als de verbranding plaatsvindt in een vochtige omgeving.
Je zou je kunnen afvragen: "Waarom juist deze twee stoffen?". Laten we dat verder bekijken.
Waarom Kooldioxide (CO2)?
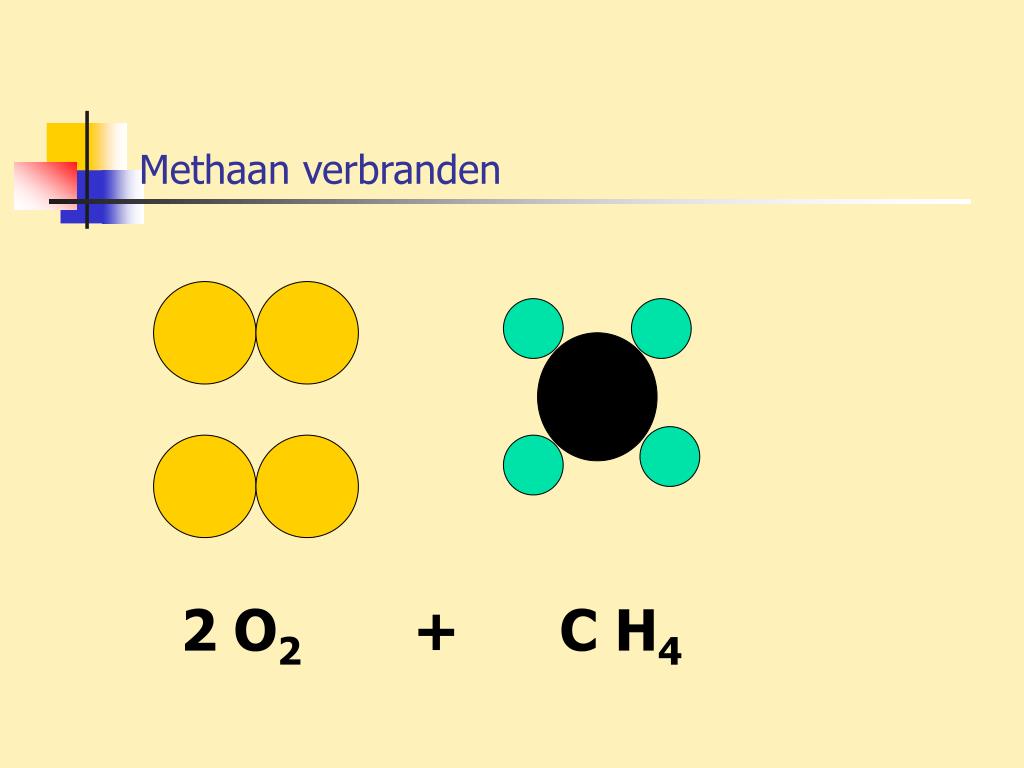
De meeste brandstoffen die we dagelijks gebruiken bevatten koolstof (C). Tijdens de verbranding reageren deze koolstofatomen met de zuurstof (O2) uit de lucht. Deze reactie vormt kooldioxide (CO2). De chemische vergelijking voor de verbranding van methaan (CH4), een veelvoorkomend aardgas, illustreert dit goed:

CH4 + 2O2 → CO2 + 2H2O
Zoals je ziet, combineert de koolstof uit methaan met zuurstof om kooldioxide te vormen.
Waarom Water (H2O)?
Veel brandstoffen bevatten ook waterstof (H). Tijdens de verbranding reageren deze waterstofatomen met de zuurstof (O2) uit de lucht om water (H2O) te vormen. In de meeste gevallen is dit in de vorm van waterdamp, omdat de verbranding veel warmte genereert.

In het voorbeeld van de verbranding van methaan (CH4) zie je dat de waterstofatomen in methaan reageren met zuurstof om water te vormen.
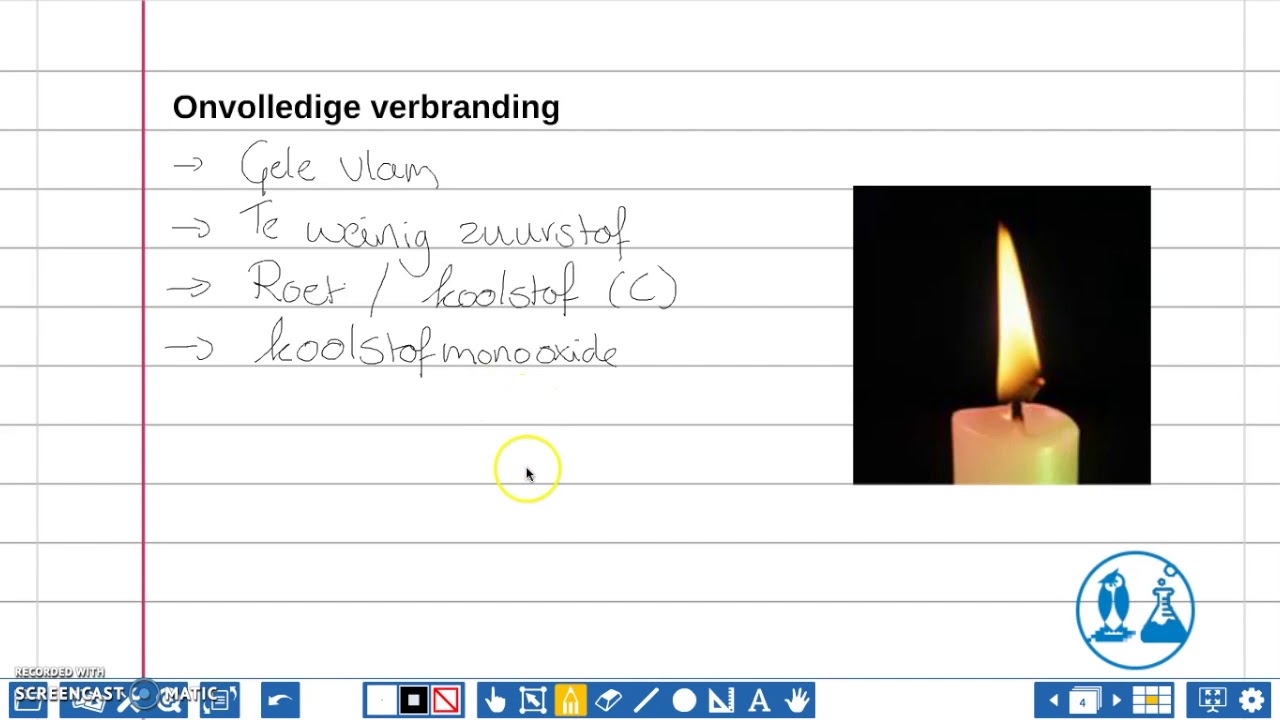
Onvolledige Verbranding: Een Belangrijke Uitzondering
Het is cruciaal om te begrijpen dat de hierboven beschreven verbranding een volledige verbranding is. Dat betekent dat er voldoende zuurstof aanwezig is om alle koolstof en waterstof in de brandstof volledig te oxideren. Maar wat gebeurt er als er niet genoeg zuurstof is?
In dat geval treedt er onvolledige verbranding op. Hierbij kunnen andere, schadelijke stoffen ontstaan, zoals:

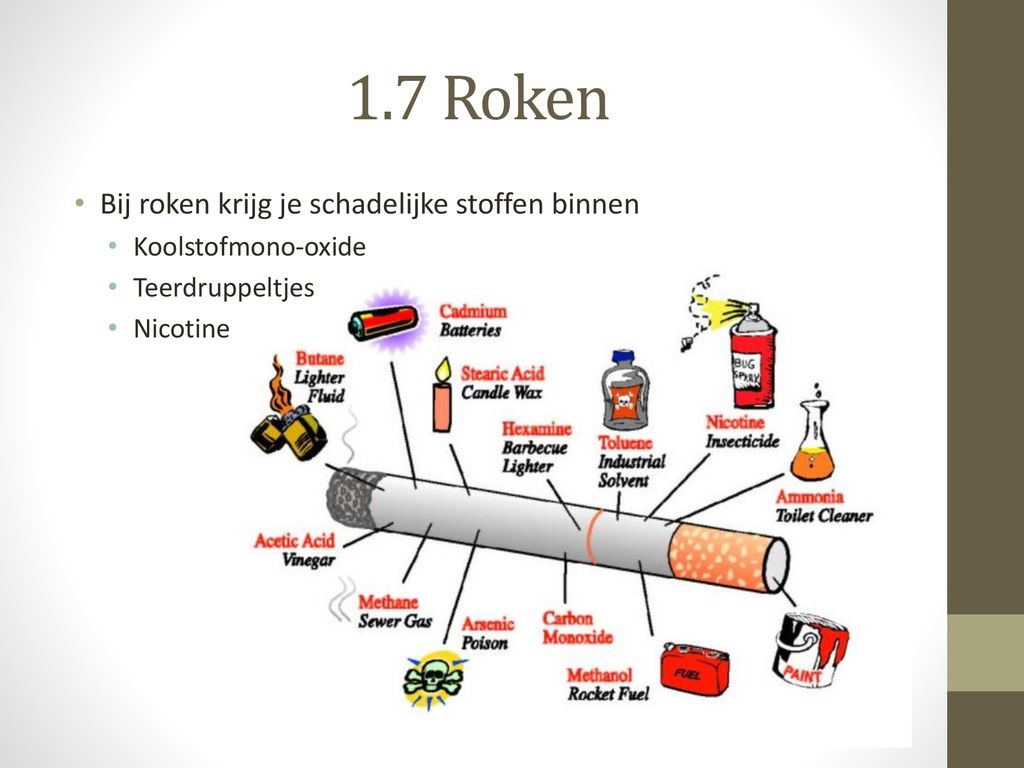
- Koolmonoxide (CO): Een zeer giftig gas dat de zuurstoftransport in het bloed kan belemmeren.
- Roet (C): Kleine, onverbrande koolstofdeeltjes die zwarte rook veroorzaken.
Een vlam die geel of oranje brandt, is vaak een teken van onvolledige verbranding. Een blauwe vlam daarentegen, duidt meestal op een volledige verbranding.
Hoe kan je dit in de praktijk toepassen?
Nu je de theorie kent, hoe kun je deze kennis in de praktijk toepassen?
- Observeer vlammen: Let op de kleur van de vlam bij het aansteken van een kaars of gasfornuis. Een blauwe vlam is efficiënter en produceert minder schadelijke stoffen dan een gele of oranje vlam.
- Denk aan ventilatie: Zorg altijd voor voldoende ventilatie bij het gebruik van brandende apparaten, zoals open haarden of kachels. Dit zorgt voor voldoende zuurstof voor een volledige verbranding en vermindert het risico op koolmonoxidevergiftiging.
- Experimenteer (onder toezicht!): Met de juiste veiligheidsmaatregelen en onder toezicht van een volwassene kun je kleine experimenten uitvoeren, zoals het verbranden van een theelichtje in een afgesloten glazen pot. Observeer wat er gebeurt en hoe de vlam verandert naarmate de zuurstof opraakt. Let op! Dit experiment kan gevaarlijk zijn en mag alleen onder toezicht van een volwassene en met de juiste veiligheidsmaatregelen worden uitgevoerd.
- Gebruik visualisaties: Er zijn online simulaties en video's beschikbaar die het verbrandingsproces visueel weergeven. Zoek bijvoorbeeld op "Verbranding simulatie" op YouTube.
Waarom is dit belangrijk om te weten?
Het begrijpen van verbranding is cruciaal om verschillende redenen:

- Milieu: Verbranding van fossiele brandstoffen is een belangrijke bron van kooldioxide (CO2), een broeikasgas dat bijdraagt aan klimaatverandering. Door verbranding efficiënter te maken en alternatieve energiebronnen te gebruiken, kunnen we onze impact op het milieu verminderen.
- Veiligheid: Inzicht in onvolledige verbranding en de vorming van koolmonoxide (CO) kan levens redden. Het is belangrijk om te weten hoe je de symptomen van koolmonoxidevergiftiging kunt herkennen en hoe je deze kunt voorkomen.
- Technologie: Verbranding is een essentieel proces in veel technologieën, zoals verbrandingsmotoren, energiecentrales en verwarmingssystemen. Door verbranding beter te begrijpen, kunnen we deze technologieën efficiënter en schoner maken.
Volgens onderzoek van het RIVM (Rijksinstituut voor Volksgezondheid en Milieu) zijn goede ventilatie en het regelmatig onderhouden van verbrandingsapparaten essentieel om de uitstoot van schadelijke stoffen, zoals koolmonoxide, te minimaliseren. ("RIVM, Koolmonoxide: wat is het en hoe voorkom je vergiftiging?", [bron: RIVM website]).
Samenvatting
Laten we de belangrijkste punten nog eens samenvatten:
- Verbranding is een chemische reactie tussen een brandstof en een oxidator, meestal zuurstof.
- De twee belangrijkste producten van volledige verbranding zijn kooldioxide (CO2) en water (H2O).
- Onvolledige verbranding kan leiden tot de vorming van schadelijke stoffen zoals koolmonoxide (CO) en roet (C).
- Het begrijpen van verbranding is belangrijk voor milieu, veiligheid en technologische ontwikkelingen.
Hopelijk heeft dit artikel je geholpen om de basisprincipes van verbranding beter te begrijpen. Blijf nieuwsgierig, blijf vragen stellen, en blijf leren!









licht+ook+twee+stoffen+nodig:+water+(H2O).jpg)