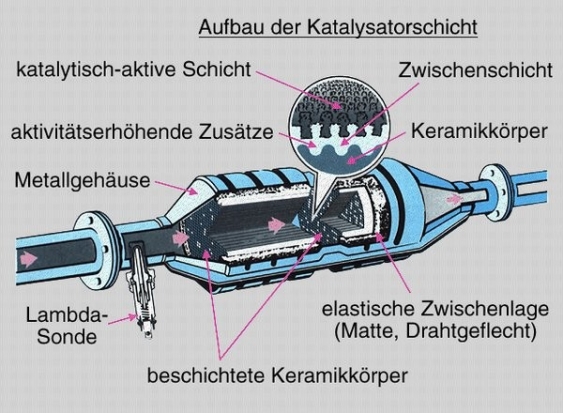
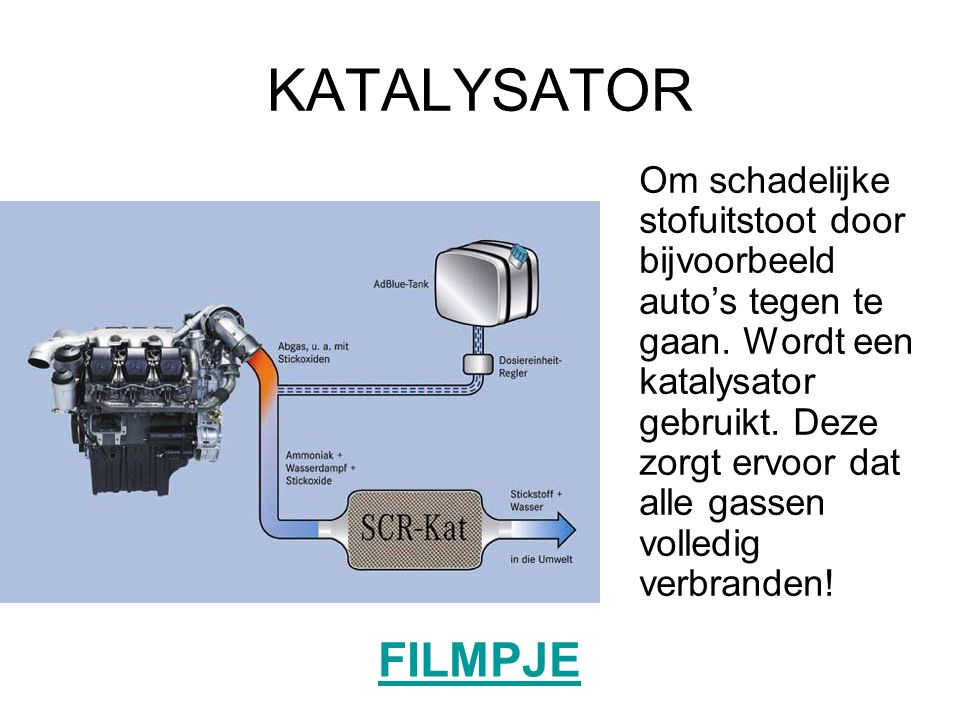
Wat Zit Er In Een Katalysator
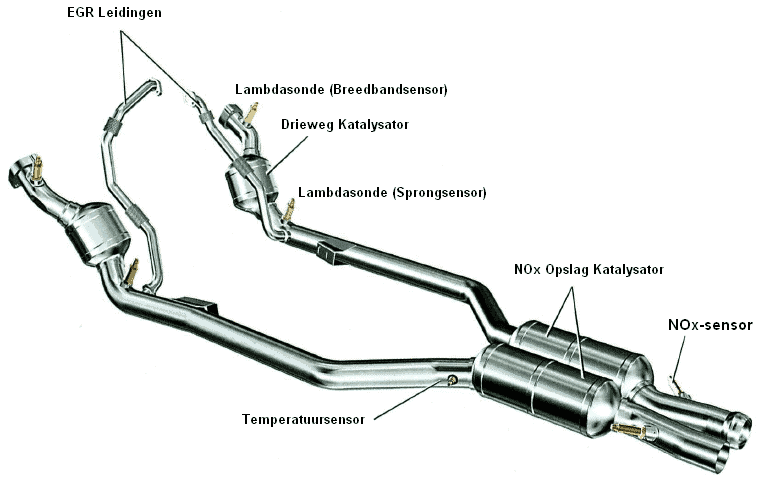
We begrijpen het. Scheikunde kan soms voelen als een doolhof, vol ingewikkelde termen en abstracte concepten. Geen zorgen, je bent niet de enige! Veel leerlingen vinden het lastig om alles te begrijpen. Laten we samen een van die lastige begrippen, de katalysator, eens grondig bekijken. We beginnen bij de basis en bouwen stap voor stap verder, zodat je aan het einde van dit artikel precies weet wat er in een katalysator zit en hoe hij werkt.
Wat is een Katalysator Eigenlijk?
Een katalysator is een stof die een chemische reactie versnelt, zonder zelf verbruikt te worden. Dat is de kern! Denk erover na als een soort matchmaker in de scheikunde. Hij brengt reactanten (de stoffen die reageren) dichter bij elkaar en zorgt ervoor dat ze gemakkelijker een verbinding aangaan. Zodra de reactie klaar is, stapt de katalysator er weer uit, klaar om een volgende reactie te helpen.
Waarom is dit belangrijk? Nou, veel industriële processen zouden simpelweg niet efficiënt (of zelfs mogelijk) zijn zonder katalysatoren. Ze besparen energie, verminderen afval en maken het mogelijk om complexe moleculen te produceren.
Must Read
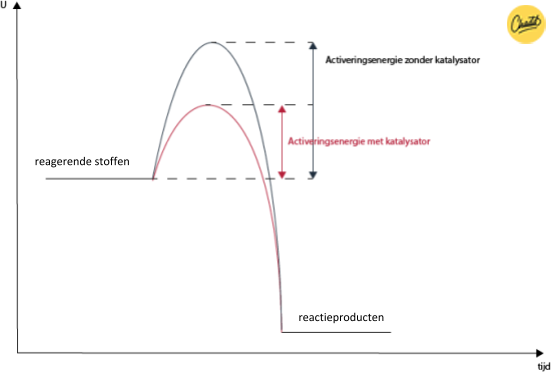
Een metafoor die vaak gebruikt wordt, is die van een heuvel. Stel je voor dat een reactie een bal is die over een heuvel moet rollen. De heuvel is de activeringsenergie – de energie die nodig is om de reactie op gang te brengen. Een katalysator maakt de heuvel lager, waardoor de bal er makkelijker overheen rolt en de reactie sneller verloopt. Belangrijk: De katalysator verandert de evenwichtspositie van de reactie niet. Het zorgt er alleen voor dat de reactie sneller zijn evenwicht bereikt.
De Ingrediënten van een Katalysator: Materialen en Structuur
Oké, we weten wat een katalysator doet. Maar waar is hij van gemaakt? Het antwoord is: het hangt er vanaf! Er zijn heel veel verschillende soorten katalysatoren, elk ontworpen voor specifieke reacties. Globaal gezien kunnen we ze indelen in een paar categorieën:
1. Metalen
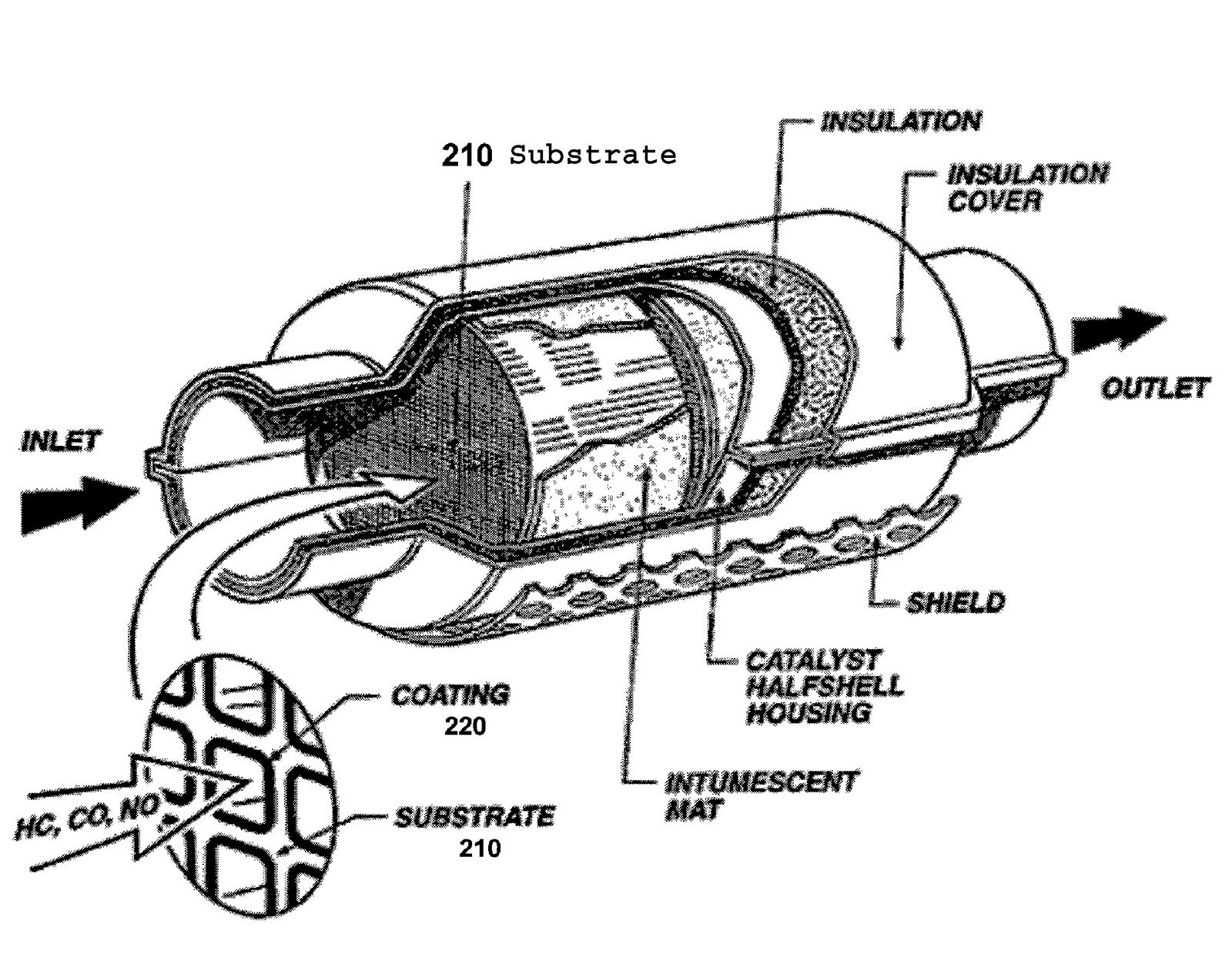
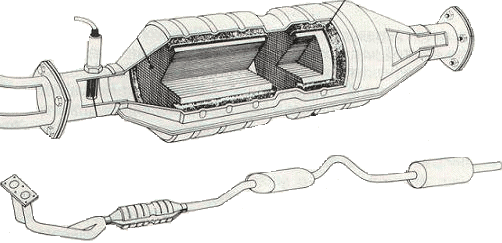
Metalen, en dan vooral overgangsmetalen zoals platina (Pt), palladium (Pd), rhodium (Rh), nikkel (Ni) en ijzer (Fe), zijn zeer populaire katalysatormaterialen. Waarom? Omdat ze de eigenschap hebben om gemakkelijk bindingen aan te gaan met andere moleculen. Denk aan de katalysator in je auto (een katalytische omzetter), die schadelijke gassen omzet in minder schadelijke stoffen. Deze bevat vaak platina, palladium en rhodium.

Tip voor docenten: Laat leerlingen een onderzoek doen naar verschillende industriële processen waarin metaalkatalysatoren gebruikt worden. Dit maakt het concept concreter.
2. Metaaloxiden
Naast pure metalen, worden ook metaaloxiden vaak gebruikt als katalysatoren. Voorbeelden zijn aluminiumoxide (Al2O3), siliciumdioxide (SiO2) en titaniumdioxide (TiO2). Deze materialen zijn vaak dragers voor de actieve metaalcomponenten, wat betekent dat de metalen fijntjes verdeeld worden over het oxide oppervlak. Dit vergroot het oppervlak van de katalysator, wat de efficiëntie ten goede komt.
Belangrijk: Het oppervlak van een katalysator is cruciaal! Een groter oppervlak betekent meer plekken waar de reactie kan plaatsvinden.

3. Zeolieten
Zeolieten zijn kristallijne aluminosilicaten met een unieke poreuze structuur. Ze hebben hele kleine kanaaltjes en holtes waar moleculen in en uit kunnen bewegen. Deze eigenschap maakt ze ideaal voor selectieve katalyse, waarbij alleen moleculen met een bepaalde grootte en vorm toegang hebben tot de actieve plaatsen. Zeolieten worden veel gebruikt in de petrochemische industrie voor het kraken van aardolie.
4. Enzymen (Biokatalysatoren)
In de biologie vinden we enzymen, de meest efficiënte katalysatoren die we kennen. Enzymen zijn eiwitten die specifieke reacties in levende organismen versnellen. Ze zijn ongelooflijk selectief en werken onder milde omstandigheden (kamertemperatuur, neutrale pH). Voorbeelden zijn amylase (verteert zetmeel) en lipase (verteert vetten). Hoewel enzymen natuurlijke producten zijn, worden ze ook steeds vaker in industriële processen gebruikt, bijvoorbeeld bij de productie van voedingsmiddelen en medicijnen.
Tip voor studenten: Vergelijk de werking van een metalen katalysator met die van een enzym. Wat zijn de overeenkomsten en verschillen?
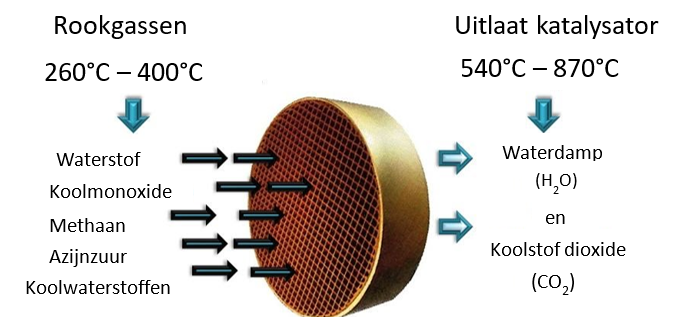
De Structuur Maakt het Verschil: Vorm en Grootte
Niet alleen het materiaal, maar ook de structuur van een katalysator is van groot belang. De vorm, grootte en poreusheid beïnvloeden de prestaties. Zoals eerder genoemd, is een groot oppervlak gunstig. Katalysatoren worden daarom vaak in de vorm van kleine deeltjes (nanodeeltjes), poeders of poreuze materialen gebruikt. De actieve metalen worden vaak verdeeld over een dragermateriaal om het oppervlak te maximaliseren.
De grootte van de poriën in een zeoliet bepaalt bijvoorbeeld welke moleculen er in de actieve centra kunnen komen. Dit principe wordt gebruikt om selectieve katalysatoren te maken, die alleen bepaalde reacties versnellen. Dit is vergelijkbaar met een sleutel die maar op één slot past.
Hoe Werkt het in de Praktijk?
Oké, theorie is leuk, maar hoe zit het met de praktijk? Laten we een paar concrete voorbeelden bekijken:
- Haber-Boschproces: De productie van ammoniak (NH3) uit stikstof (N2) en waterstof (H2) is een cruciaal proces voor de productie van kunstmest. Zonder een ijzerkatalysator zou deze reactie veel te langzaam verlopen.
- Katalytische omzetter in auto's: Zoals al eerder genoemd, zet de katalytische omzetter in auto's schadelijke gassen (koolmonoxide, stikstofoxiden, koolwaterstoffen) om in minder schadelijke stoffen (kooldioxide, stikstof, water).
- Polymerisatie: Bij de productie van plastics (polymeren) worden vaak katalysatoren gebruikt om de reactie van kleine moleculen (monomeren) tot lange ketens (polymeren) te versnellen.
- Voedingsindustrie: Enzymen worden gebruikt bij de productie van kaas, bier, brood en andere voedingsmiddelen.
Praktische oefening: Onderzoek een van deze processen en beschrijf welke katalysator er gebruikt wordt en waarom.
Tips voor het Leren over Katalysatoren
Vind je het nog steeds lastig? Hier zijn een paar tips die je kunnen helpen:
- Visualiseer: Probeer de processen visueel voor te stellen. Zoek online naar animaties of diagrammen.
- Gebruik metaforen: De heuvel-metafoor kan helpen om het concept van activeringsenergie te begrijpen.
- Maak het concreet: Zoek voorbeelden van katalysatoren in het dagelijks leven (auto, wasmiddel, voedsel).
- Werk samen: Bespreek de stof met klasgenoten of docenten. Leg het aan elkaar uit.
- Oefen: Maak oefenopgaven en test je kennis.
Tip voor ouders: Help je kind door vragen te stellen en samen naar voorbeelden te zoeken in de omgeving.
Conclusie: Je Kunt Het!
We zijn aan het einde gekomen van deze reis door de wereld van katalysatoren. Hopelijk heb je nu een beter begrip van wat er in een katalysator zit en hoe hij werkt. Onthoud: scheikunde kan lastig zijn, maar met de juiste aanpak en een beetje doorzettingsvermogen kun je het zeker begrijpen. Blijf vragen stellen, blijf onderzoeken en blijf leren! Jij kunt dit!





.png)