Wat Is Polair En Apolair

Ken je dat? Je staat in de keuken, probeert een vinaigrette te maken. Olijfolie, azijn, een beetje mosterd… Alles in een potje, flink schudden, en… BAM! Twee aparte lagen. Frustrerend, toch? Ik had dat laatst ook weer. Ik dacht: "Waarom lukt dit nou nooit meteen?!" Zucht. Maar hé, dat bracht me wel op een idee voor dit artikel! Want de boosdoener is iets heel simpels: polariteit. En geloof me, als je eenmaal snapt wat dat is, dan gaat die vinaigrette eindelijk lukken.
Wat is Polariteit Eigenlijk?
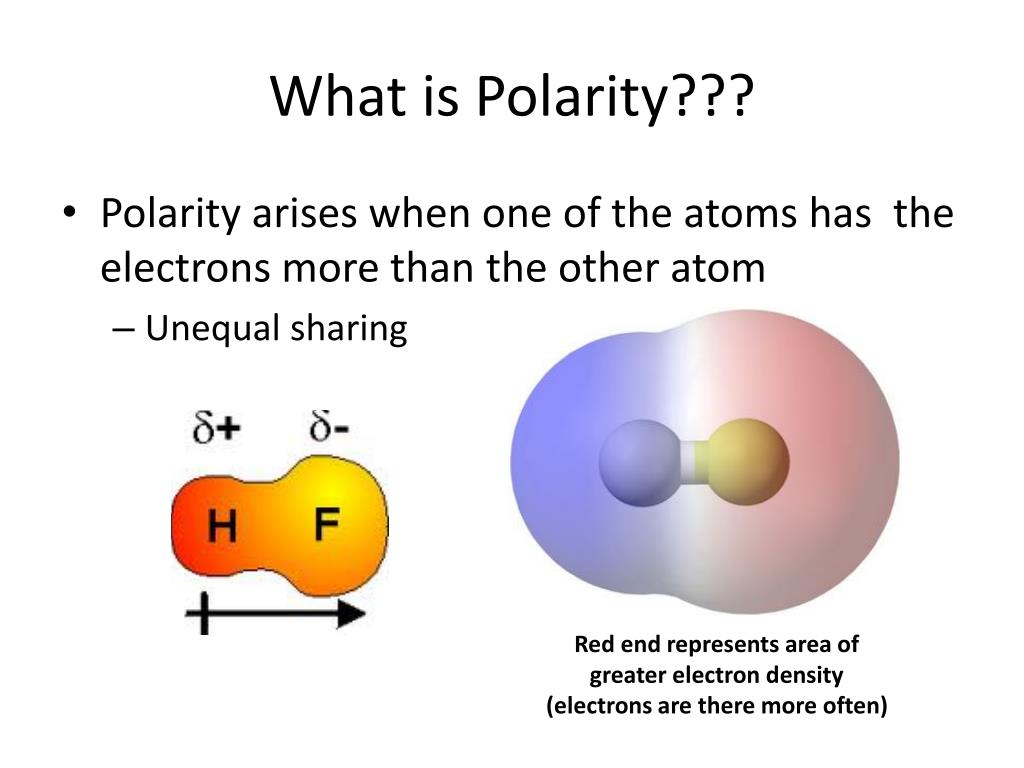
Polariteit, in de chemie, is eigenlijk niets meer dan een beschrijving van hoe gelijkmatig (of ongelijkmatig) elektronen verdeeld zijn in een molecuul. Denk aan een magneet. Die heeft een noordpool en een zuidpool. Moleculen kunnen ook 'polen' hebben, alleen dan met een iets andere lading. Het draait allemaal om de manier waarop atomen aan elkaar trekken.
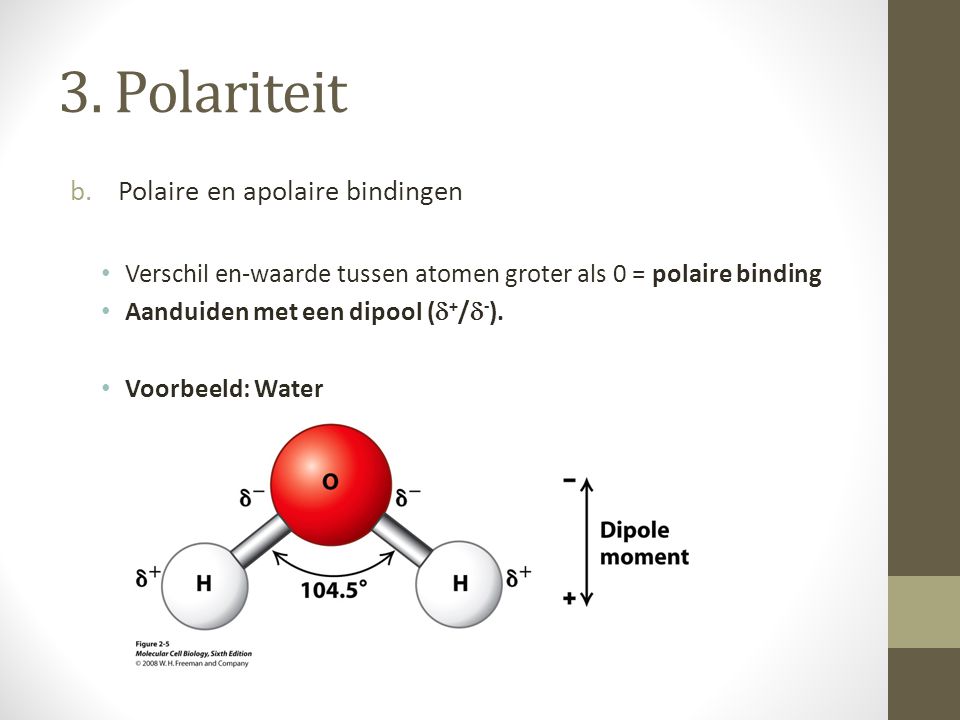
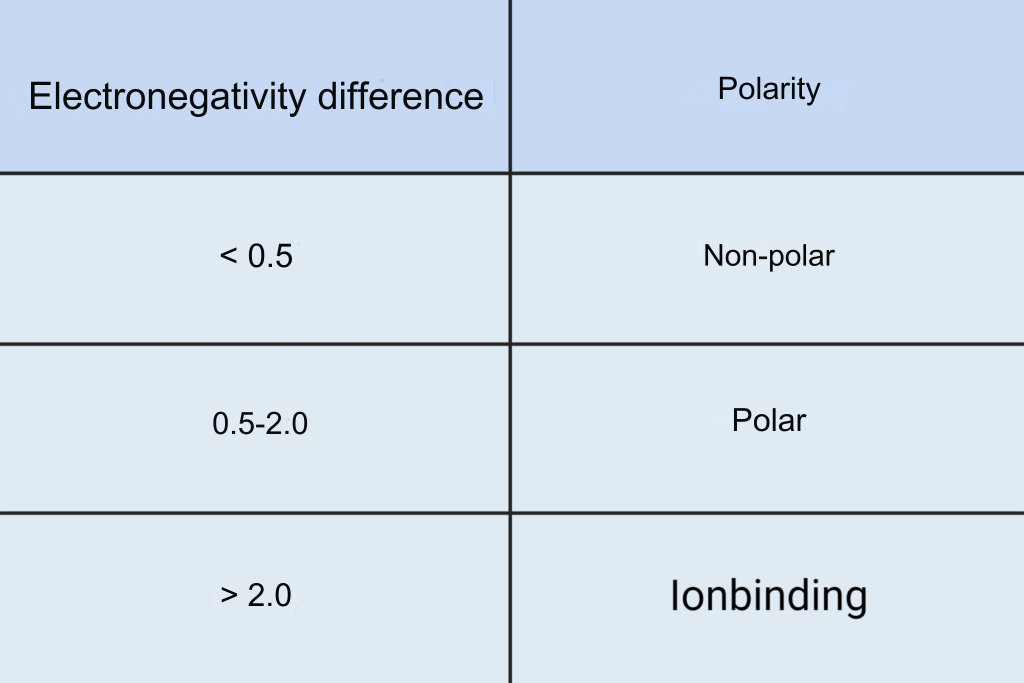
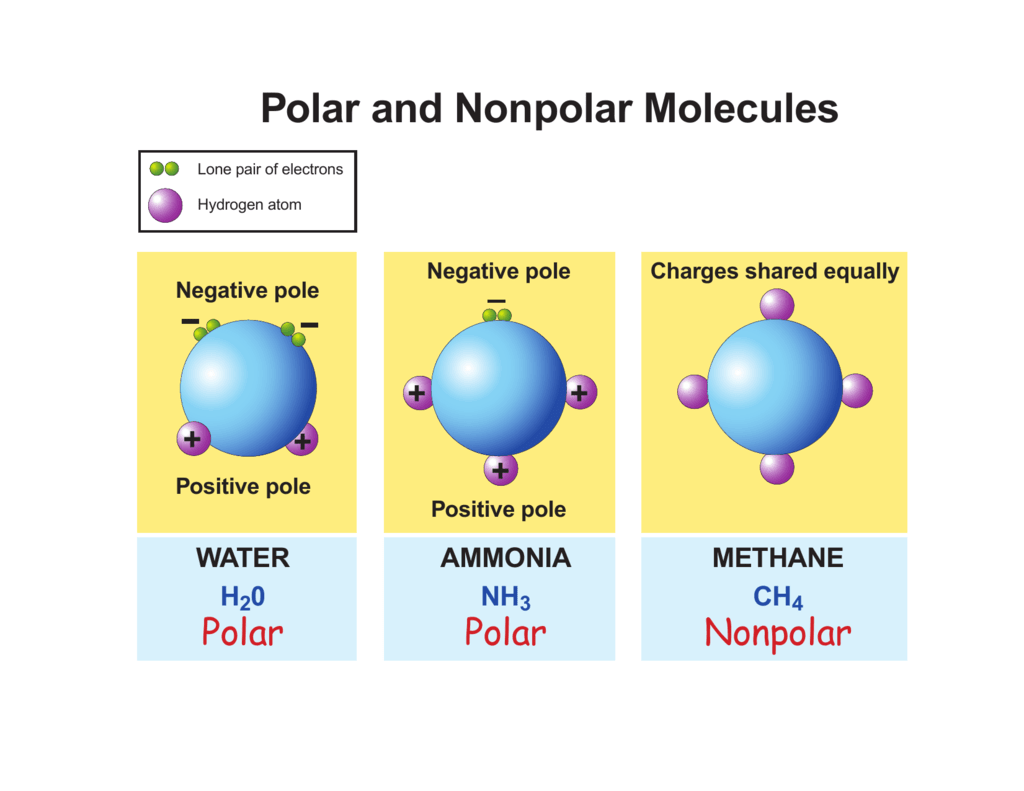
Polariteit ontstaat door een verschil in elektronegativiteit tussen atomen. Oké, dat is een mond vol. Simpel gezegd: sommige atomen zijn hebberiger naar elektronen dan andere. Zuurstof bijvoorbeeld, is een echte electronen-rover. Dus als zuurstof en waterstof een molecuul vormen (H₂O, oftewel water), trekt zuurstof harder aan de elektronen dan waterstof. Dit zorgt ervoor dat de zuurstofkant van het molecuul een beetje negatief geladen is (δ-, spreek uit: delta min) en de waterstofkant een beetje positief (δ+, delta plus).
Must Read
En daar heb je 'm: een polair molecuul! Het heeft dus een 'positieve' en een 'negatieve' kant, net als die magneet.
Polariteit: Even Samengevat
- Verschil in elektronegativiteit tussen atomen
- Ongelijkmatige verdeling van elektronen
- Molecuul heeft een positieve en negatieve kant (δ+ en δ-)
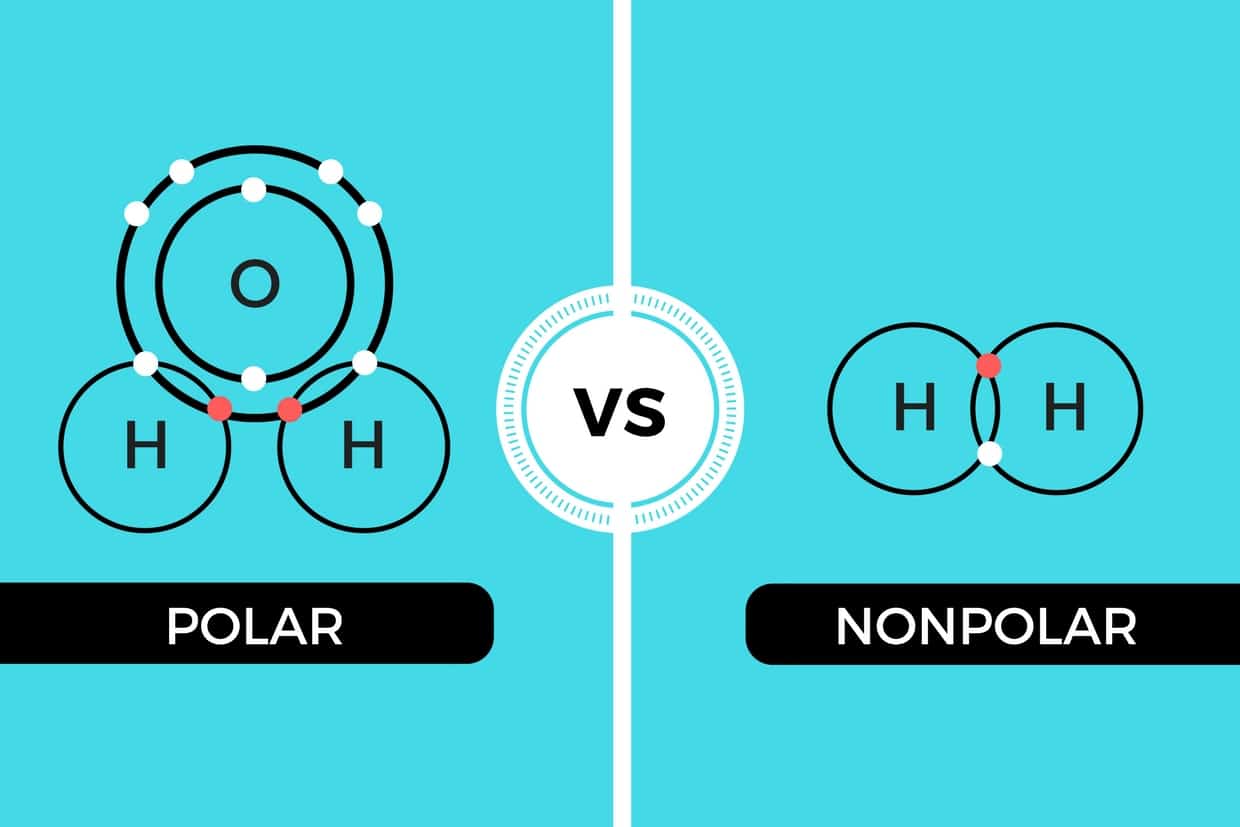
En Dan: Apolair!
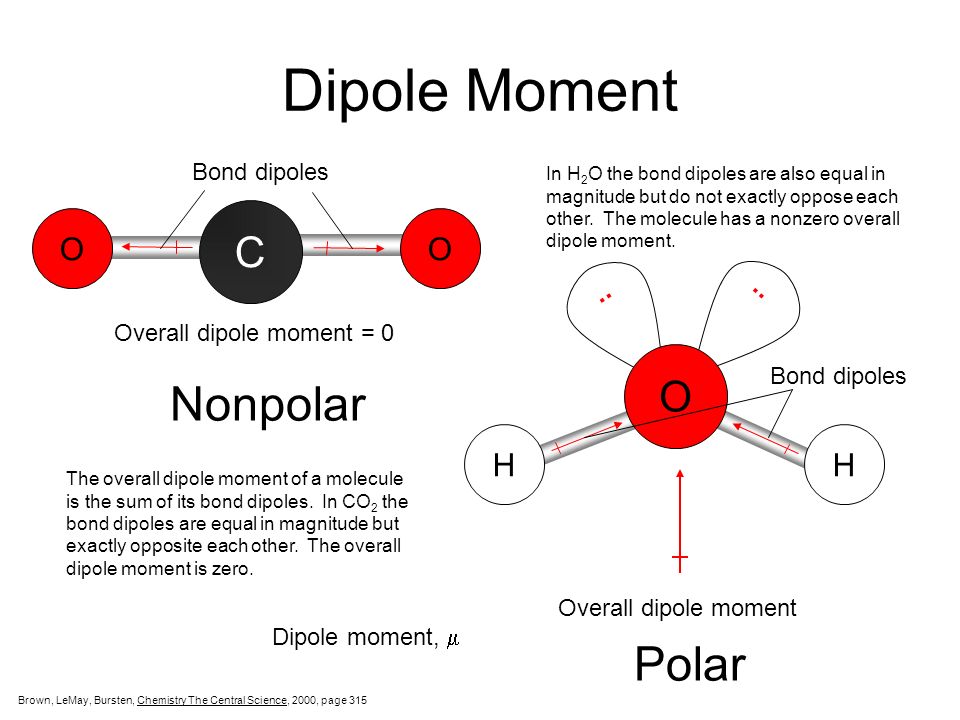
Je raadt het al: apolair is het tegenovergestelde. Hier is de elektronenverdeling wél gelijkmatig. Er is geen significant verschil in elektronegativiteit tussen de atomen, of de vorm van het molecuul heft de polariteit op. Denk bijvoorbeeld aan olie. Meestal bestaat het uit lange koolwaterstofketens (alleen koolstof- en waterstofatomen). Koolstof en waterstof hebben een vergelijkbare elektronegativiteit, dus de elektronen worden redelijk gelijkmatig verdeeld.
Dat betekent dus: geen 'positieve' of 'negatieve' kant. Apolaire moleculen zijn over het algemeen 'neutraal'.

Apolariteit: Ook Even Samengevat
- Geen (of nauwelijks) verschil in elektronegativiteit
- Gelijkmatige verdeling van elektronen
- Molecuul is 'neutraal', geen positieve of negatieve kant
Waarom is Dit Belangrijk? "Like Dissolves Like"!
De hamvraag! Waarom zouden we ons druk maken om of iets polair of apolair is? Nou, hier komt het gouden regeltje: "Like dissolves like". Oftewel: gelijk lost gelijk op.
Dat betekent dat:
- Polaire stoffen lossen goed op in andere polaire stoffen. Denk aan zout (polair) dat oplost in water (polair).
- Apolaire stoffen lossen goed op in andere apolaire stoffen. Denk aan olie (apolair) dat oplost in wasbenzine (apolair).
- Maar... polaire en apolaire stoffen mengen niet goed. En daar heb je de crux van die vinaigrette!
Olie is apolair, azijn is (voornamelijk) water en dus polair. BOEM. Ze stoten elkaar af. Ze mengen niet. En je staat daar met je potje te schudden als een bezetene, maar het helpt niks.
Dus, wat kun je eraan doen? Enter: emulgatoren!

De Redder in Nood: Emulgatoren!
Een emulgator is een stof die een beetje van beide kanten heeft: een polair deel en een apolair deel. Het fungeert als een soort brug tussen de polaire en apolaire stoffen.
Denk aan zeep. Zeep heeft een polair 'kopje' en een apolaire 'staart'. De staart hecht zich aan vet (apolair) en de kop hecht zich aan water (polair). Zo kan zeep vuil (wat vaak vettig en dus apolair is) losmaken en met water wegspoelen. Geniaal, toch?
En in die vinaigrette? Mosterd! Mosterd bevat emulgatoren die helpen om de olie en de azijn te mengen. Eigeel (in mayonaise bijvoorbeeld) is ook een goede emulgator.

Dus, de volgende keer dat je een vinaigrette maakt, denk aan de polariteit en voeg een emulgator toe. Je zult zien: het werkt als een tierelier!
Nog Wat Voorbeelden? Ja, Graag!
Oké, om het nog even concreter te maken, hier zijn nog wat voorbeelden van polaire en apolaire stoffen:
Polaire Stoffen
- Water (H₂O)
- Alcohol (zoals ethanol)
- Suiker (glucose, sucrose, etc.)
- Zout (NaCl)
- Ammoniak (NH₃)
Apolaire Stoffen
- Olie (plantaardige olie, minerale olie, etc.)
- Vet (boter, reuzel, etc.)
- Benzine
- Wasbenzine
- Lucht (voornamelijk stikstof en zuurstof, maar de moleculen zijn apolair)
Zie je het patroon? Stoffen die voornamelijk bestaan uit zuurstof-, stikstof- of andere elektronegatieve atomen zijn vaak polair. Stoffen die voornamelijk bestaan uit koolstof en waterstof zijn vaak apolair.
Polariteit in het Dagelijks Leven
Polariteit kom je overal tegen, zelfs als je het niet doorhebt! Denk bijvoorbeeld aan:
- Kleding wassen: Zeep (met zijn polaire en apolaire eigenschappen) helpt om vet en vuil van je kleding te verwijderen.
- Medicijnen: De polariteit van een medicijn bepaalt hoe goed het wordt opgenomen in je lichaam en hoe het zich verdeelt over verschillende weefsels.
- Verf: De polariteit van de verf en de ondergrond beïnvloedt hoe goed de verf hecht.
- Biologie: De celmembranen van je lichaam bestaan uit een dubbele laag fosfolipiden. Deze moleculen hebben een polaire kop en apolaire staarten, waardoor ze een barrière vormen die selectief stoffen doorlaat.
Het is eigenlijk best fascinerend, als je erover nadenkt. Zo'n simpel concept als polariteit heeft zo'n grote impact op de wereld om ons heen.
Conclusie: Polariteit Gesnapt! (Hopelijk...)
Dus, wat hebben we geleerd? Polariteit is een beschrijving van de verdeling van elektronen in een molecuul. Polaire stoffen hebben een positieve en negatieve kant, apolaire stoffen niet. "Like dissolves like" is de gouden regel. En emulgatoren helpen om polaire en apolaire stoffen te mengen. Pats!
Ik hoop dat dit artikel een beetje licht heeft geschenen op de wondere wereld van polariteit. En dat je de volgende keer dat je een vinaigrette maakt, aan dit artikel denkt en met een glimlach een beetje mosterd toevoegt. Succes!
En onthoud: chemie is overal! Dus blijf nieuwsgierig en blijf ontdekken!










![Polar vs Nonpolar molecules: How to tell? [GCE A Level Chemistry] - YouTube](https://i.ytimg.com/vi/WkiA4Du-5oE/maxresdefault.jpg)
