Wat Is Het Getal Van Avogadro
Heb je je ooit afgevraagd hoe wetenschappers het aantal atomen in een klein korreltje zout kunnen tellen? Of hoe ze de massa van een enkel atoom kunnen bepalen? Veel leerlingen, ouders en zelfs docenten worstelen met deze vragen, vooral als het gaat om een concept als het getal van Avogadro. Het klinkt ingewikkeld, maar geloof me, met een duidelijke uitleg en wat praktische voorbeelden, wordt alles een stuk begrijpelijker. In dit artikel ontrafelen we samen de mysteries van het getal van Avogadro, zodat je er straks met vertrouwen over kunt praten!
Wat is het Getal van Avogadro?
Het getal van Avogadro, vaak aangeduid met NA, is een fundamentele constante in de scheikunde. Het vertegenwoordigt het aantal deeltjes (atomen, moleculen, ionen, etc.) dat zich bevindt in één mol van een stof. De waarde van het getal van Avogadro is ongeveer 6,02214076 × 1023.
Simpel gezegd: Denk aan een dozijn eieren. Een dozijn is altijd 12, ongeacht of het kippeneieren, kwarteleitjes of zelfs fictieve draakeneieren zijn. Op dezelfde manier is een mol altijd 6,02214076 × 1023 deeltjes, ongeacht of het watermoleculen, natriumatomen of iets anders is.
Must Read
Waarom is het Getal van Avogadro Zo Belangrijk?
Het getal van Avogadro is cruciaal omdat het een brug slaat tussen de macroscopische wereld (wat we kunnen zien en wegen, zoals grammen) en de microscopische wereld (atomen en moleculen die we niet direct kunnen zien). Het stelt ons in staat om:
- De massa van een enkel atoom of molecuul te berekenen.
- Het aantal atomen of moleculen in een bepaalde massa van een stof te bepalen.
- Chemische reacties kwantitatief te begrijpen en te voorspellen.
Zonder het getal van Avogadro zou de chemie zoals we die kennen niet bestaan. Het is een fundamentele pijler voor het uitvoeren van berekeningen en het begrijpen van de samenstelling van stoffen.
De Geschiedenis Achter Avogadro's Getal
Het getal is vernoemd naar de Italiaanse wetenschapper Amedeo Avogadro (1776-1856). Hoewel Avogadro zelf de exacte waarde van het getal niet heeft berekend, formuleerde hij een belangrijke hypothese die later essentieel bleek voor de bepaling ervan. Avogadro's hypothese stelde dat gelijke volumes van gassen, bij dezelfde temperatuur en druk, hetzelfde aantal moleculen bevatten.
De eerste nauwkeurige bepaling van het getal van Avogadro werd pas veel later gedaan door de Franse natuurkundige Jean Perrin in de vroege 20e eeuw. Perrin bewees het bestaan van atomen en moleculen door zijn onderzoek naar Brownse beweging (de willekeurige beweging van deeltjes in een vloeistof). Zijn werk leverde hem in 1926 de Nobelprijs voor de Natuurkunde op.
Hoe wordt het Getal van Avogadro Bepaald?
Er zijn verschillende methoden om het getal van Avogadro te bepalen, elk met zijn eigen principes en uitdagingen. Enkele van de meest gebruikte methoden zijn:
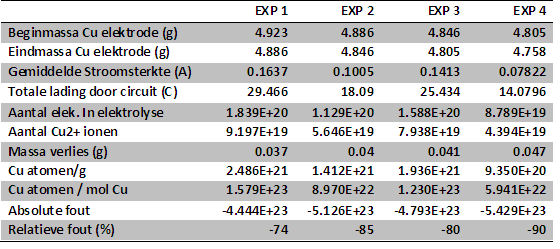
- Elektrolyse: Door de hoeveelheid elektriciteit te meten die nodig is om een bekende hoeveelheid van een stof te elektrolyseren (bijvoorbeeld water in waterstof en zuurstof), kan men het getal van Avogadro berekenen.
- Kristalstructuur: Met behulp van röntgendiffractie kan de afstand tussen atomen in een kristal worden gemeten. Door de dichtheid van het kristal te combineren met de afstand tussen de atomen, kan het getal van Avogadro worden berekend.
- Brownse Beweging: Zoals eerder vermeld, gebruikte Perrin de Brownse beweging van kleine deeltjes in een vloeistof om het getal van Avogadro te bepalen.
De waarde van het getal van Avogadro is door de jaren heen steeds nauwkeuriger bepaald dankzij de vooruitgang in experimentele technieken en meetapparatuur.

Voorbeelden en Toepassingen in de Praktijk
Laten we eens kijken naar een paar praktische voorbeelden om het concept van het getal van Avogadro te illustreren:
Voorbeeld 1: Water (H2O)
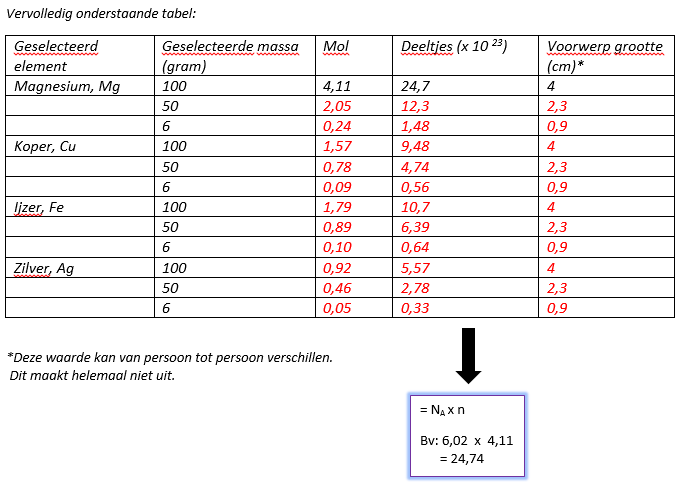
De molaire massa van water (H2O) is ongeveer 18 gram per mol. Dit betekent dat 18 gram water 6,02214076 × 1023 watermoleculen bevat. Stel je voor dat je een glas water hebt dat 18 gram weegt. In dat glas zitten ongelooflijk veel watermoleculen!
Voorbeeld 2: Koolstof (C)
De molaire massa van koolstof (C) is 12 gram per mol. Dus, 12 gram koolstof bevat 6,02214076 × 1023 koolstofatomen. Een diamant, die voornamelijk uit koolstof bestaat, bevat dus een gigantisch aantal koolstofatomen, zelfs als het een klein diamantje is.

Een Simpel Experiment voor in de Klas (of Thuis met Toezicht!)
Je kunt het concept van molaire massa en het getal van Avogadro illustreren met een eenvoudig experiment met suiker (sucrose, C12H22O11). De molaire massa van sucrose is ongeveer 342 gram per mol.
- Weeg 3.42 gram suiker af (dit is 0.01 mol suiker).
- Vertel de leerlingen/kinderen dat deze kleine hoeveelheid suiker 0.01 mol suiker bevat, wat gelijk staat aan 0.01 x 6,02214076 × 1023 suikermoleculen.
- Bespreek hoe ongelooflijk groot dit aantal is, en hoe klein de suikermoleculen moeten zijn.
Dit experiment geeft een concrete illustratie van de relatie tussen massa en het aantal deeltjes.
Veelgemaakte Fouten en Misverstanden
Er zijn een paar veelgemaakte fouten en misverstanden als het gaat om het getal van Avogadro:

- Verwarring met molaire massa: Het is belangrijk om te begrijpen dat het getal van Avogadro een aantal is, terwijl molaire massa een massa is. Het getal van Avogadro vertelt je hoeveel deeltjes er in een mol zitten, terwijl de molaire massa je vertelt hoeveel een mol van die stof weegt.
- Denken dat het alleen voor atomen geldt: Het getal van Avogadro geldt voor alle soorten deeltjes: atomen, moleculen, ionen, elektronen, enz.
- De enorme schaal niet begrijpen: 6,02214076 × 1023 is een ongelooflijk groot getal. Het is moeilijk om de schaal ervan te bevatten. Vergelijk het bijvoorbeeld met het aantal zandkorrels op alle stranden van de wereld, of het aantal sterren in het heelal.
Het Getal van Avogadro in de Moderne Wetenschap
Het getal van Avogadro blijft een cruciale constante in de moderne wetenschap. Het wordt gebruikt in een breed scala aan toepassingen, van de nanotechnologie tot de farmaceutische industrie. Het speelt een essentiële rol bij het ontwerpen en ontwikkelen van nieuwe materialen, het begrijpen van chemische reacties en het ontwikkelen van nieuwe medicijnen.
Bovendien is het getal van Avogadro een belangrijk onderdeel van het Internationaal Stelsel van Eenheden (SI). In 2019 is de definitie van de kilogram herzien en gebaseerd op het getal van Avogadro, wat de fundamentele aard ervan benadrukt.
Conclusie
Het getal van Avogadro is misschien een abstract concept, maar het is een krachtig hulpmiddel dat ons helpt om de microscopische wereld te begrijpen en te manipuleren. Door de relatie tussen massa en het aantal deeltjes te begrijpen, kunnen we chemische reacties voorspellen, nieuwe materialen ontwerpen en de mysteries van de natuur ontrafelen.
Dus, de volgende keer dat je een korreltje zout ziet, bedenk dan dat het een onvoorstelbaar aantal natrium- en chloride-ionen bevat, en dat het getal van Avogadro ons helpt om dat te begrijpen! Met een beetje oefening en duidelijke uitleg, kan iedereen het getal van Avogadro begrijpen en waarderen.






:.jpg)
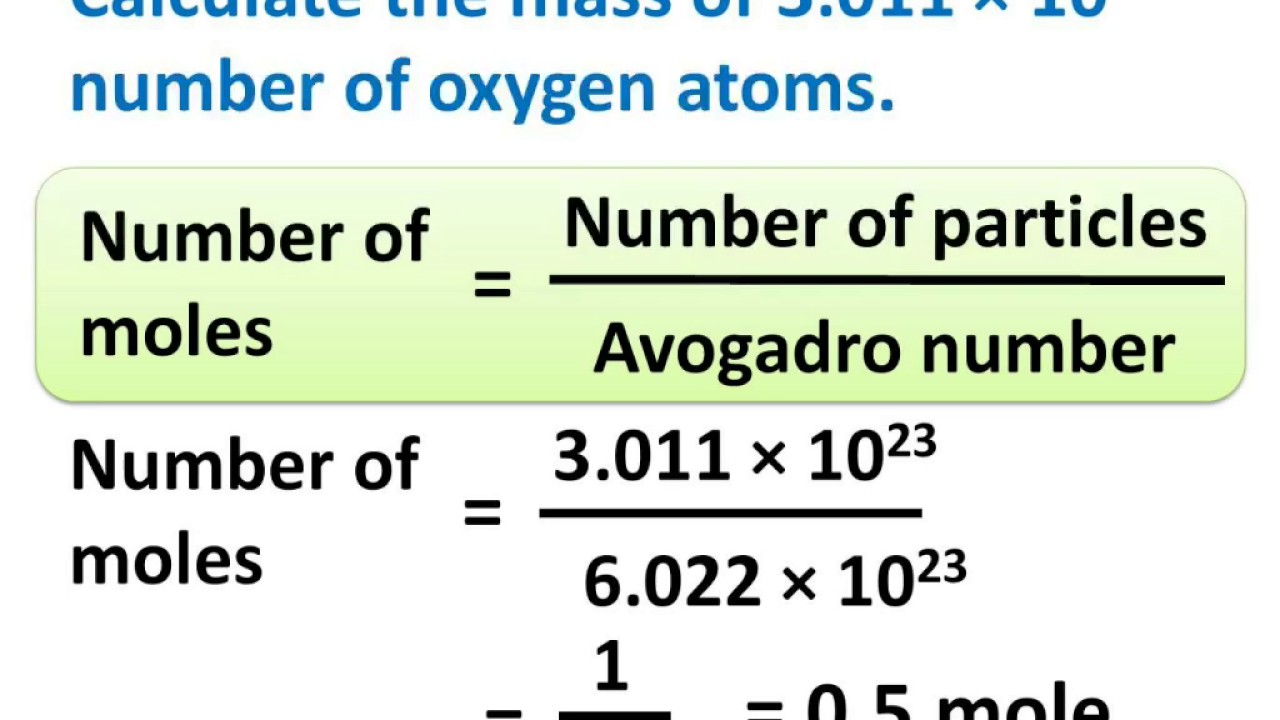

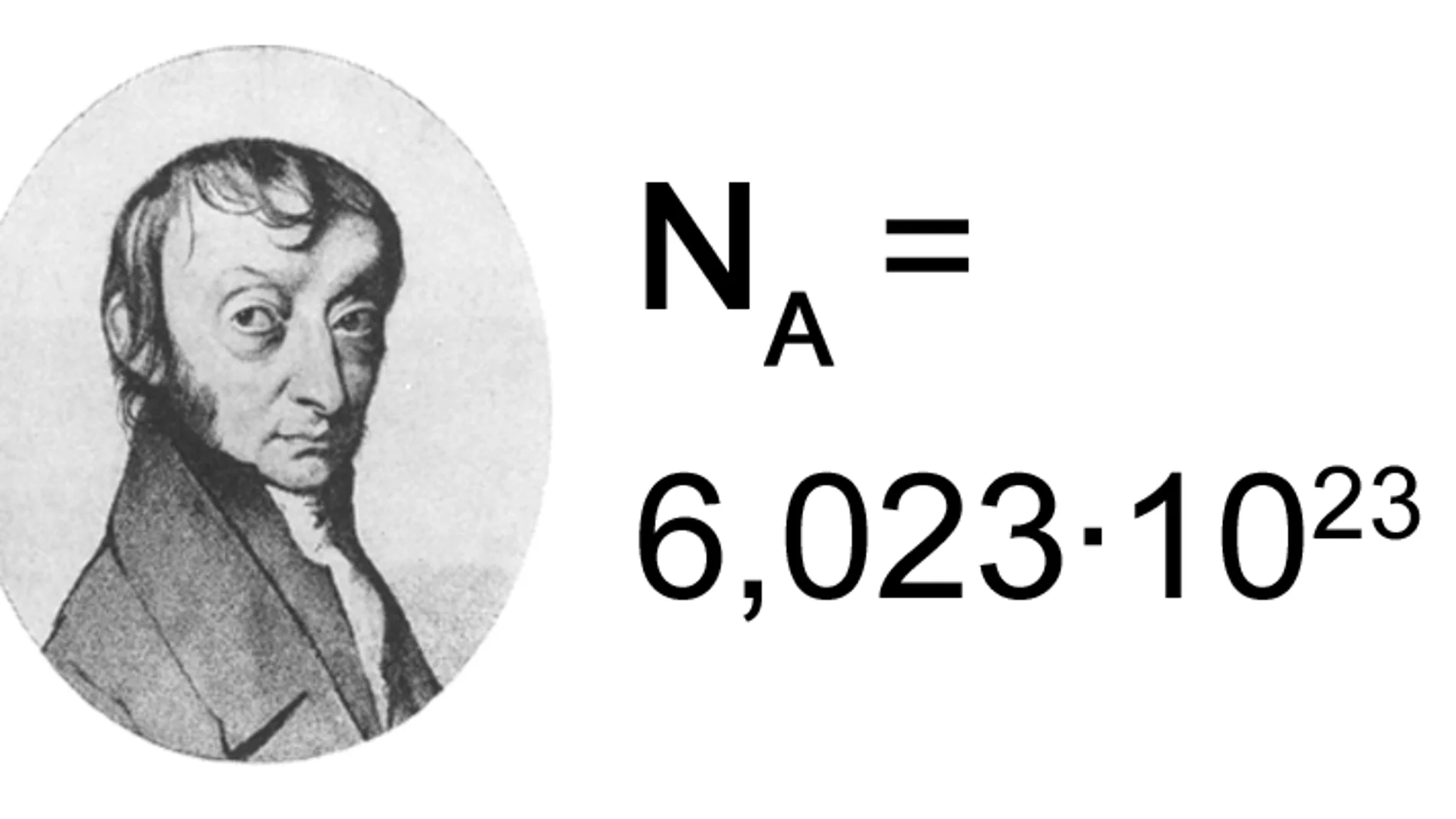


.jpg)
