Wat Is Een Zuur Base Reactie
Heb je je ooit afgevraagd waarom citroensap zo zuur smaakt of waarom bakpoeder je gebak zo luchtig maakt? De antwoorden liggen in de fascinerende wereld van zuur-base reacties! Deze reacties zijn niet alleen belangrijk in de chemie, maar spelen ook een cruciale rol in ons dagelijks leven. In dit artikel duiken we diep in wat een zuur-base reactie precies is, hoe het werkt, en waarom het zo belangrijk is.
Dit artikel is bedoeld voor iedereen die nieuwsgierig is naar chemie, van scholieren en studenten tot mensen die gewoon meer willen weten over de wereld om hen heen. We zullen de concepten op een duidelijke en begrijpelijke manier uitleggen, zonder ingewikkeld jargon.
Wat is een Zuur?
Laten we beginnen met de basis: wat is een zuur? Een zuur is een stof die in staat is om protonen (H+ ionen) af te staan. Denk aan citroensap (citroenzuur), azijn (azijnzuur) en zoutzuur (gebruikt in de industrie en aanwezig in je maag om voedsel te verteren!).
Must Read
Eigenschappen van Zuren:
- Zure smaak: Let op! Probeer nooit zuren te proeven, tenzij je zeker weet dat het veilig is. Concentreerde zuren kunnen erg gevaarlijk zijn.
- Corrosief: Zuren kunnen materialen aantasten.
- Reageren met metalen: Vaak produceert dit waterstofgas (H2).
- Verkleuren bepaalde indicatoren: Bijvoorbeeld lakmoes, dat rood wordt in een zure omgeving.
De sterkte van een zuur wordt bepaald door de mate waarin het protonen afstaat. Sterke zuren staan bijna al hun protonen af in water, terwijl zwakke zuren dit maar gedeeltelijk doen.
Wat is een Base?
Aan de andere kant van het spectrum hebben we basen. Een base is een stof die in staat is om protonen (H+ ionen) op te nemen. Basen worden ook wel alkaliën genoemd, vooral als ze oplosbaar zijn in water. Voorbeelden zijn natronloog (natriumhydroxide), zeep en bakpoeder.
Eigenschappen van Basen:
- Bittere smaak: Net als bij zuren, proef nooit basen tenzij je zeker weet dat het veilig is.
- Glad aanvoelen: Zeep is een goed voorbeeld.
- Corrosief: Ook basen kunnen materialen aantasten.
- Verkleuren bepaalde indicatoren: Bijvoorbeeld lakmoes, dat blauw wordt in een basische omgeving.
Net als bij zuren, hebben we ook sterke en zwakke basen. Sterke basen nemen bijna alle protonen op in water, terwijl zwakke basen dit maar gedeeltelijk doen.

De Zuur-Base Reactie: Neutralisatie
Nu komt het interessante deel: wat gebeurt er als we een zuur en een base bij elkaar brengen? Dan krijgen we een zuur-base reactie, ook wel neutralisatie genoemd. Bij deze reactie reageert het zuur met de base, waarbij een zout en water worden gevormd.
De algemene reactievergelijking ziet er als volgt uit:
Zuur + Base → Zout + Water
Laten we een simpel voorbeeld bekijken: de reactie tussen zoutzuur (HCl) en natriumhydroxide (NaOH):

HCl (zuur) + NaOH (base) → NaCl (zout - keukenzout) + H2O (water)
In deze reactie staat het zoutzuur (HCl) een proton (H+) af, dat wordt opgenomen door het hydroxide-ion (OH-) van het natriumhydroxide (NaOH). Het resultaat is natriumchloride (NaCl), oftewel keukenzout, en water (H2O).
De Rol van Water: Autodissociatie
Water speelt een cruciale rol in zuur-base reacties. Zuiver water is niet helemaal neutraal; het ondergaat een proces dat autodissociatie wordt genoemd. Hierbij reageren watermoleculen met elkaar, waarbij kleine hoeveelheden hydroniumionen (H3O+) en hydroxide-ionen (OH-) worden gevormd:
2 H2O ⇌ H3O+ + OH-

In zuiver water is de concentratie van H3O+ en OH- gelijk, waardoor het neutraal is. Als we een zuur toevoegen, verhoogt de concentratie van H3O+, waardoor de oplossing zuur wordt. Als we een base toevoegen, verhoogt de concentratie van OH-, waardoor de oplossing basisch wordt.
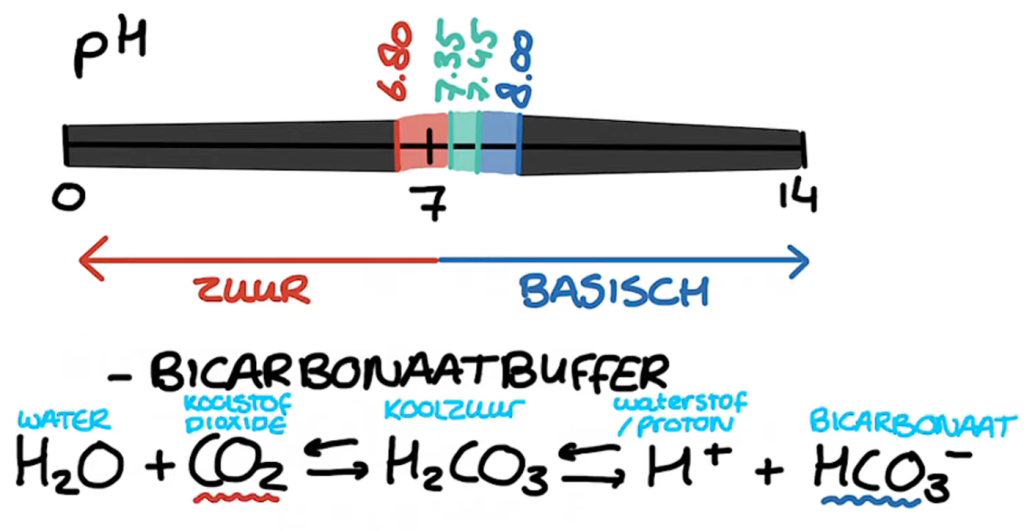
De pH-schaal: Een Maat voor Zuurheid en Basischheid
Om de zuurgraad of basiciteit van een oplossing aan te geven, gebruiken we de pH-schaal. Deze schaal loopt van 0 tot 14:
- pH < 7: Zuur
- pH = 7: Neutraal
- pH > 7: Basisch
De pH-waarde is een logaritmische schaal, wat betekent dat een verandering van één pH-eenheid een tienvoudige verandering in de zuurgraad of basiciteit vertegenwoordigt. Een oplossing met een pH van 3 is dus tien keer zuurder dan een oplossing met een pH van 4.
Voorbeelden van pH-waarden:
- Maagzuur: pH 1-2
- Citroensap: pH 2-3
- Azijn: pH 3
- Regenwater: pH 5.6 (licht zuur door opgeloste CO2)
- Zuiver water: pH 7
- Bloed: pH 7.4
- Zeewater: pH 8
- Zeep: pH 9-10
- Ammoniak: pH 11
- Natronloog: pH 14
Zuur-Base Reacties in het Dagelijks Leven
Zuur-base reacties zijn overal om ons heen, ook al realiseren we ons dat niet altijd. Hier zijn enkele voorbeelden:

- Spijsvertering: Je maag produceert zoutzuur (HCl) om voedsel te verteren. Soms kan er te veel maagzuur worden geproduceerd, wat leidt tot brandend maagzuur. Antacida, die basen bevatten (zoals calciumcarbonaat), neutraliseren het overmatige zuur en verlichten de symptomen.
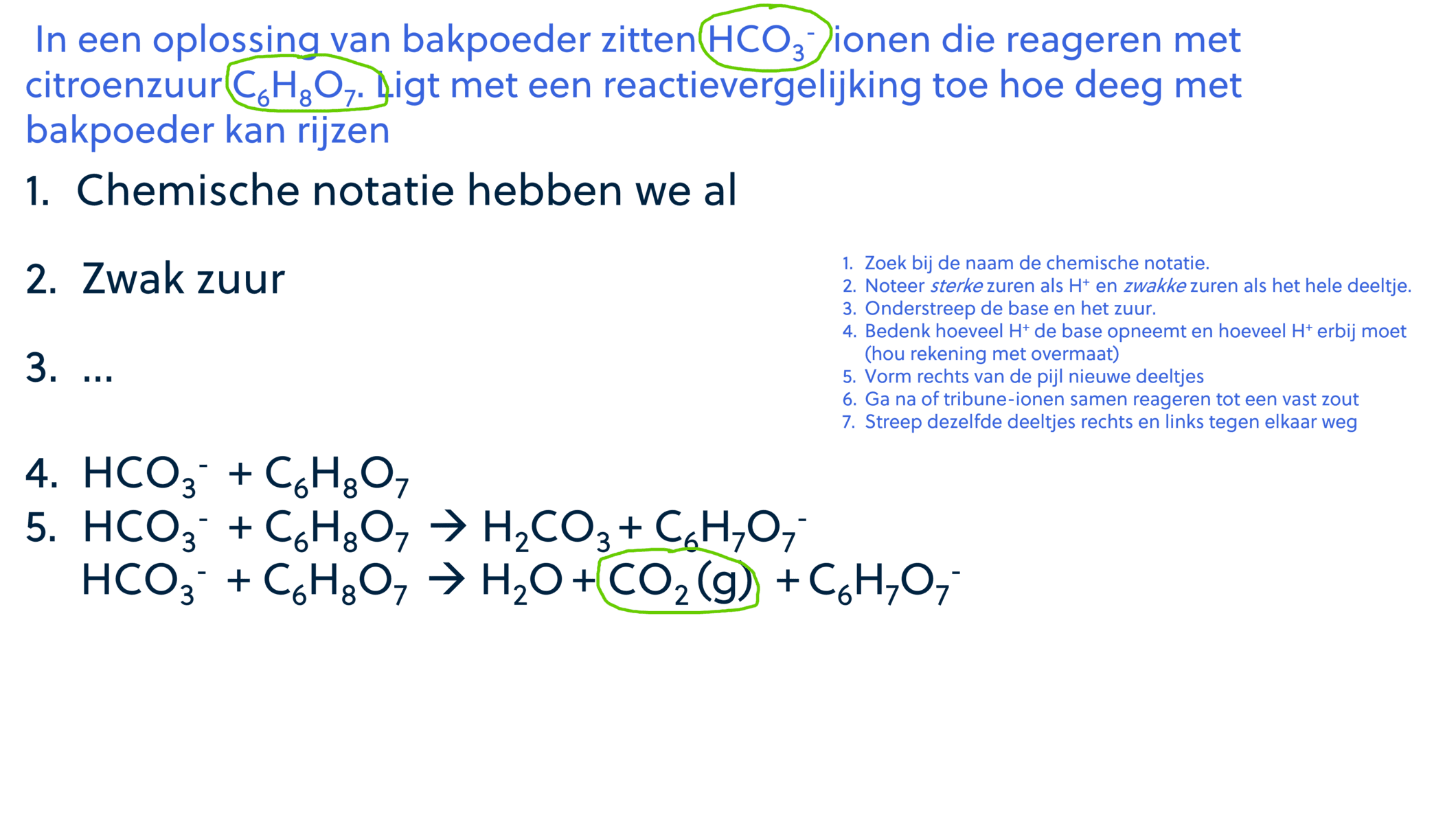
- Bakken: Bakpoeder (natriumbicarbonaat) reageert met een zuur ingrediënt (zoals karnemelk of citroensap) in het beslag om koolstofdioxide (CO2) gas te produceren. Dit gas zorgt ervoor dat het beslag rijst en luchtig wordt.
- Reiniging: Veel schoonmaakmiddelen bevatten basen, zoals ammoniak, om vet en vuil te verwijderen. Zuren, zoals azijn, kunnen worden gebruikt om kalkaanslag te verwijderen.
- Landbouw: De pH van de bodem is cruciaal voor de groei van planten. Als de bodem te zuur is, kan kalk (calciumcarbonaat) worden toegevoegd om de pH te neutraliseren.
- Titraties: In het laboratorium worden zuur-base reacties gebruikt om de concentratie van een zuur of base in een oplossing te bepalen. Dit proces staat bekend als titratie.
Indicatoren: Kleurrijke Hulpjes
Hoe weten we wanneer een zuur-base reactie is voltooid? We kunnen indicatoren gebruiken. Dit zijn stoffen die van kleur veranderen afhankelijk van de pH van de oplossing. Een bekende indicator is lakmoes, maar er zijn veel andere indicatoren met verschillende kleuromslagen.
Indicatoren worden vaak gebruikt bij titraties om het equivalentiepunt te bepalen, het punt waarop het zuur en de base elkaar volledig hebben geneutraliseerd. De kleurverandering van de indicator geeft aan wanneer dit punt is bereikt.
Conclusie: Het Belang van Zuur-Base Reacties
Zuur-base reacties zijn fundamentele processen in de chemie die een enorme impact hebben op ons dagelijks leven. Van de spijsvertering tot het bakken, van schoonmaken tot landbouw, zuur-base reacties spelen een cruciale rol. Door te begrijpen wat zuren en basen zijn en hoe ze reageren, kunnen we de wereld om ons heen beter begrijpen en zelfs verbeteren.
Hopelijk heeft dit artikel je geholpen om een beter inzicht te krijgen in de fascinerende wereld van zuur-base reacties. Blijf nieuwsgierig en blijf leren!