Wat Is Een Zout Scheikunde

Heb je ooit het gevoel gehad dat scheikunde een ondoordringbare muur is? Dat je begrippen als zouten, zuren en basen wel hoort, maar ze nooit echt begrijpt? Je bent niet de enige! Veel leerlingen worstelen met deze basisconcepten. Het goede nieuws is: het is absoluut te leren! Met de juiste aanpak en een beetje geduld kan iedereen de scheikunde van zouten ontrafelen.
Wat is een Zout: De Basis Uitgelegd
Laten we beginnen bij het begin: wat is een zout eigenlijk? In de scheikunde is een zout een chemische verbinding die ontstaat door de reactie tussen een zuur en een base. Dit is een neutralisatiereactie. De reactie produceert niet alleen een zout, maar ook water (H2O). Denk bijvoorbeeld aan de reactie tussen zoutzuur (HCl) en natronloog (NaOH):
HCl + NaOH → NaCl + H2O
Must Read
Hier is NaCl (natriumchloride), beter bekend als keukenzout, het zout dat gevormd wordt.
De Structuur van Zouten
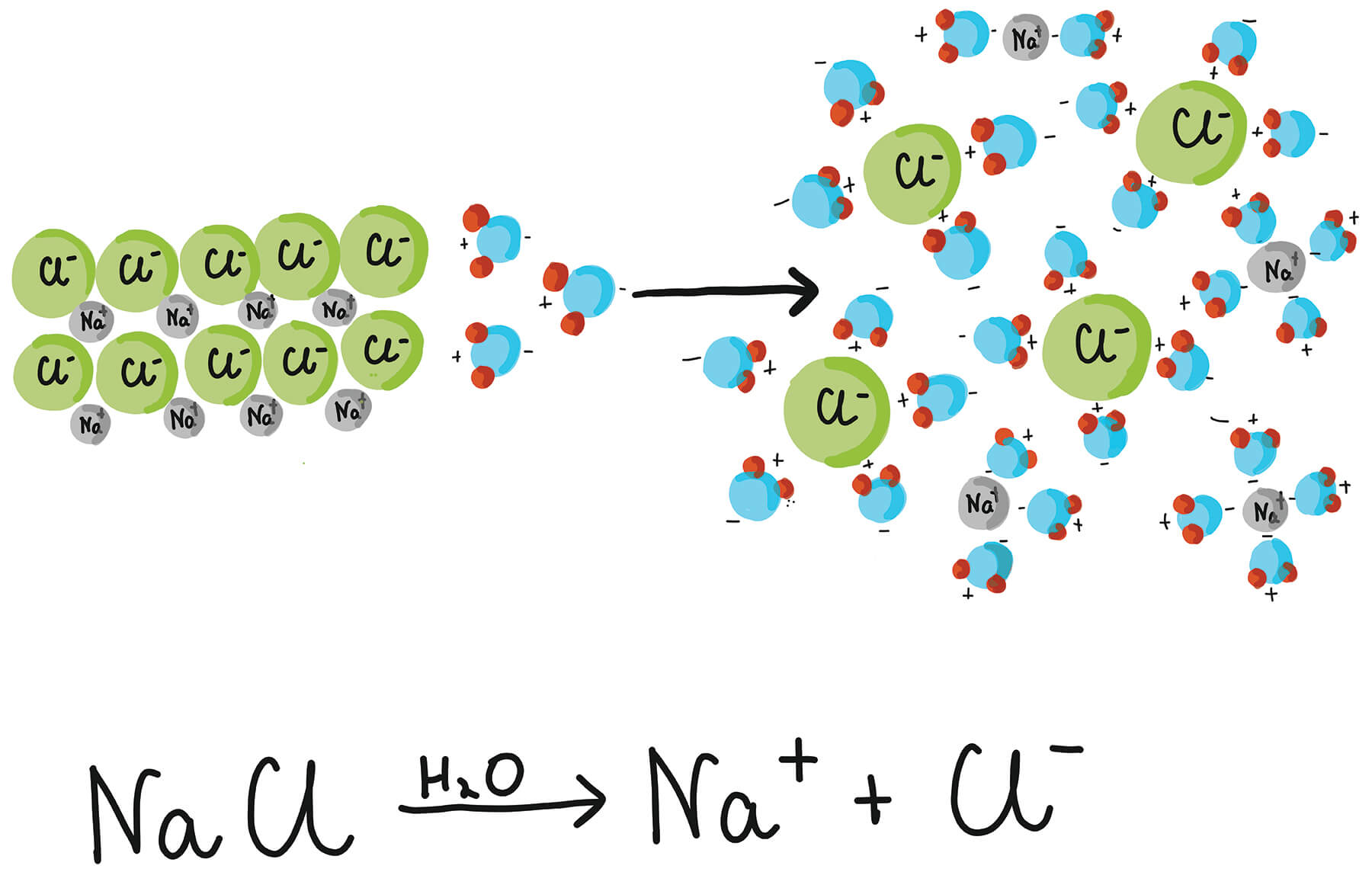
Zouten zijn opgebouwd uit ionen: positief geladen ionen (kationen) en negatief geladen ionen (anionen). Deze ionen zijn via ionbindingen met elkaar verbonden in een kristalrooster. Denk aan een soort legoblokjes die zich steeds herhalen in een vaste structuur. De sterkte van deze ionbindingen bepaalt onder andere het smeltpunt van het zout. Volgens onderzoek van de Universiteit van Californië, Berkeley, blijkt dat het visueel maken van deze kristalstructuren studenten helpt om het concept beter te begrijpen (zie hun online chemiedatabase).

Zuren en Basen: De Fundamenten van Zoutvorming
Om zouten echt te begrijpen, moeten we eerst de zuren en basen begrijpen. Zuren zijn stoffen die in water H+ ionen (protonen) afstaan. Basen zijn stoffen die in water OH- ionen (hydroxide-ionen) afstaan, of protonen opnemen.
Een sterk zuur staat gemakkelijk H+ ionen af, terwijl een zwak zuur dit minder gemakkelijk doet. Hetzelfde geldt voor basen: sterke basen nemen gemakkelijk protonen op, en zwakke basen minder gemakkelijk.
De sterkte van een zuur of base wordt gemeten met de pH-schaal. Een pH van 7 is neutraal, waarden lager dan 7 zijn zuur, en waarden hoger dan 7 zijn basisch.

Hoe Zuren en Basen Zouten Vormen
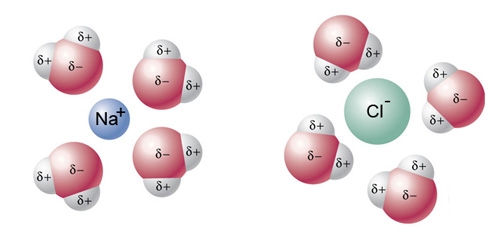
Tijdens de reactie tussen een zuur en een base, neutraliseren de H+ ionen van het zuur de OH- ionen van de base (of worden opgenomen door de base). De overgebleven ionen van het zuur en de base vormen vervolgens het zout. Het anion van het zuur en het kation van de base vormen dus samen het zout.
Soorten Zouten en Hun Eigenschappen
Er zijn ontzettend veel verschillende soorten zouten, elk met hun eigen unieke eigenschappen. Enkele voorbeelden:
- Natriumchloride (NaCl): Keukenzout, essentieel voor het leven en veel gebruikt in de voedingsindustrie. Het is goed oplosbaar in water.
- Calciumcarbonaat (CaCO3): Komt voor in kalksteen, marmer en schelpen. Wordt gebruikt in cement en als zuurteregelaar. Het is slecht oplosbaar in water.
- Koper(II)sulfaat (CuSO4): Een blauw gekleurd zout dat gebruikt wordt als fungicide en in de galvanotechniek. Het is oplosbaar in water.
De eigenschappen van een zout, zoals oplosbaarheid, smeltpunt en elektrische geleiding, worden bepaald door de ionen waaruit het is opgebouwd en de sterkte van de ionbindingen.

Oplosbaarheid van Zouten
Niet alle zouten lossen even goed op in water. Sommige zouten lossen heel goed op, andere nauwelijks. De oplosbaarheid van een zout wordt beïnvloed door verschillende factoren, zoals:
- De aard van de ionen: Sommige ioncombinaties lossen beter op dan andere. Algemene oplosbaarheidsregels (te vinden in veel scheikundeboeken en online) kunnen je hierbij helpen.
- De temperatuur: Over het algemeen neemt de oplosbaarheid van zouten toe bij hogere temperaturen.
- De aanwezigheid van andere ionen: De aanwezigheid van bepaalde andere ionen kan de oplosbaarheid van een zout beïnvloeden (het common ion effect).
Toepassingen van Zouten in het Dagelijks Leven
Zouten zijn overal om ons heen en spelen een cruciale rol in ons dagelijks leven. Hier zijn enkele voorbeelden:
- Voeding: Keukenzout (NaCl) wordt gebruikt om smaak aan eten te geven en als conserveermiddel. Andere zouten, zoals calciumzouten, zijn belangrijk voor onze gezondheid.
- Industrie: Zouten worden gebruikt in een breed scala aan industriële processen, zoals de productie van plastics, papier en medicijnen.
- Landbouw: Zouten worden gebruikt als meststoffen om de groei van gewassen te bevorderen.
- Geneeskunde: Zouten worden gebruikt in medicijnen en intraveneuze oplossingen om de elektrolytenbalans in het lichaam te herstellen.
Zonder zouten zou ons leven er heel anders uitzien! Ze zijn essentieel voor veel processen in de natuur en in de industrie.

Tips voor het Leren over Zouten in de Scheikunde
Hier zijn een paar praktische tips om het leren over zouten in de scheikunde makkelijker en leuker te maken:
- Maak het visueel: Gebruik modellen, animaties en diagrammen om de structuur van zouten en de reacties tussen zuren en basen te visualiseren. Er zijn tal van online resources beschikbaar, zoals PhET Interactive Simulations, die gratis interactieve simulaties aanbieden.
- Oefen, oefen, oefen: Maak veel oefenopgaven om je kennis te testen en je vaardigheden te verbeteren. Begin met eenvoudige opgaven en werk langzaam naar moeilijkere toe.
- Begrijp de basisconcepten: Zorg dat je de basisconcepten van zuren, basen, ionen en ionbindingen goed begrijpt voordat je verdergaat.
- Werk samen: Studeer samen met andere leerlingen en bespreek de stof. Elkaar uitleggen helpt om de stof beter te begrijpen.
- Vraag hulp: Aarzel niet om hulp te vragen aan je docent, tutor of medeleerlingen als je ergens vastloopt.
- Maak het relevant: Zoek naar voorbeelden van zouten in het dagelijks leven en probeer de chemische principes te koppelen aan praktische toepassingen.
Voor docenten: Overweeg om praktische experimenten op te nemen in je les, zoals het maken van zouten door een zuur en een base te laten reageren. Dit maakt de leerstof tastbaarder en interessanter voor de leerlingen. Een studie van de Universiteit van York toonde aan dat studenten die actief betrokken zijn bij experimenten in de scheikunde significant betere resultaten behalen (York, 2018).
Conclusie: Je Kunt Het!
Het begrijpen van zouten in de scheikunde kan in het begin lastig lijken, maar met de juiste aanpak en een beetje doorzettingsvermogen is het zeker haalbaar. Onthoud dat oefening baart kunst en dat je niet bang hoeft te zijn om fouten te maken. Fouten zijn juist leermomenten! Blijf nieuwsgierig, blijf vragen stellen en vertrouw op je eigen kunnen. Je kunt dit!