Wat Is Een Moleculaire Stof

Hoi allemaal! Heb je je ooit afgevraagd waaruit alles om ons heen is opgebouwd? Van de lucht die we inademen tot het water dat we drinken, alles is gemaakt van superkleine deeltjes. Vandaag duiken we in een heel belangrijk concept: de moleculaire stof. Het klinkt misschien ingewikkeld, maar ik beloof je, het is reuze interessant en superrelevant voor je schoolwerk en daarbuiten!
Wat is een moleculaire stof?
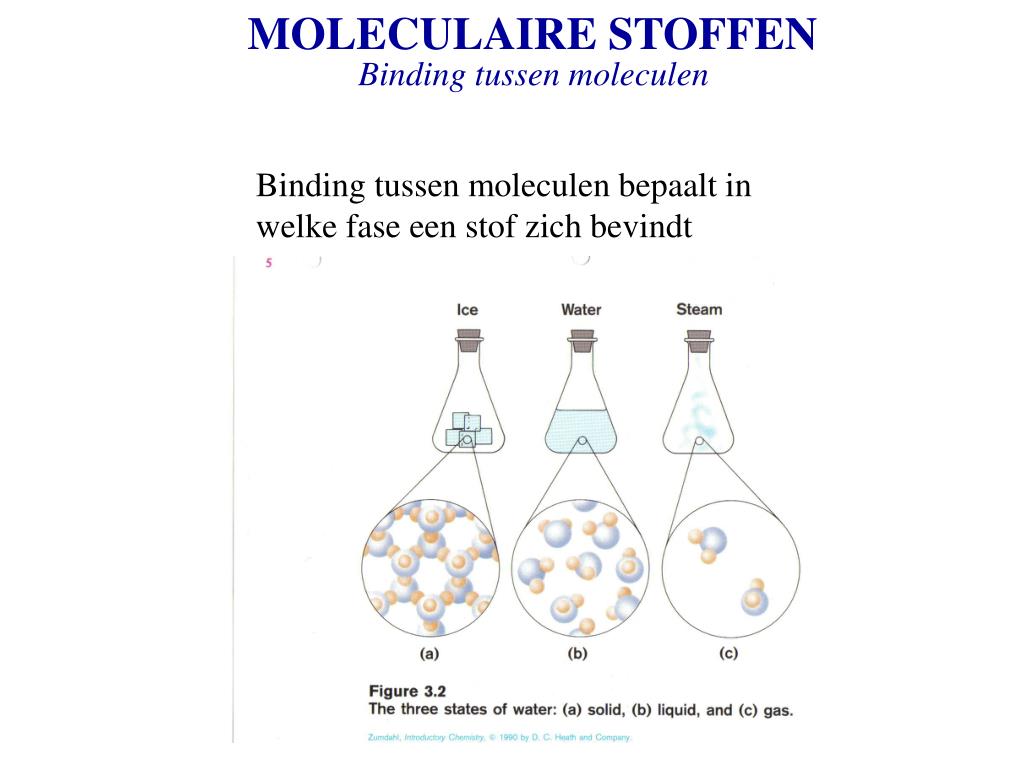
Laten we het simpel houden. Een moleculaire stof is een stof die bestaat uit afzonderlijke moleculen. En wat zijn moleculen dan weer? Dat zijn groepen van twee of meer atomen die aan elkaar zijn gebonden. Denk aan water (H₂O). Elk watermolecuul bestaat uit twee waterstofatomen (H) en één zuurstofatoom (O) die samen een eenheid vormen. Deze eenheid, het watermolecuul, is verantwoordelijk voor de eigenschappen van water. Het is anders dan keukenzout (NaCl), dat een ionaire verbinding is en geen losse moleculen heeft.
Voorbeelden die je overal ziet
Moleculaire stoffen kom je overal tegen! Denk aan:
Must Read
- Zuurstof (O₂): Essentieel om te ademen!
- Stikstof (N₂): Het grootste deel van de lucht die we inademen.
- Koolstofdioxide (CO₂): Belangrijk voor planten en een broeikasgas.
- Suiker (C₁₂H₂₂O₁₁): Geeft ons energie!
Al deze stoffen bestaan uit moleculen, groepen atomen die stevig met elkaar verbonden zijn en de eigenschappen van de stof bepalen. Zonder deze moleculen zou de wereld er heel anders uitzien!
Wat je leert van moleculaire stoffen voor school en het leven
Het begrijpen van moleculaire stoffen leert je veel meer dan alleen scheikunde. Het stimuleert je logisch denken en je probleemoplossend vermogen. Als je begrijpt hoe moleculen in elkaar zitten, kun je voorspellen hoe stoffen zich zullen gedragen onder verschillende omstandigheden. Dat is superhandig bij vakken als natuurkunde en biologie, maar ook bij alledaagse situaties.

“Kennis is macht,” zei Francis Bacon ooit. En dat geldt zeker voor de kennis over moleculaire stoffen!
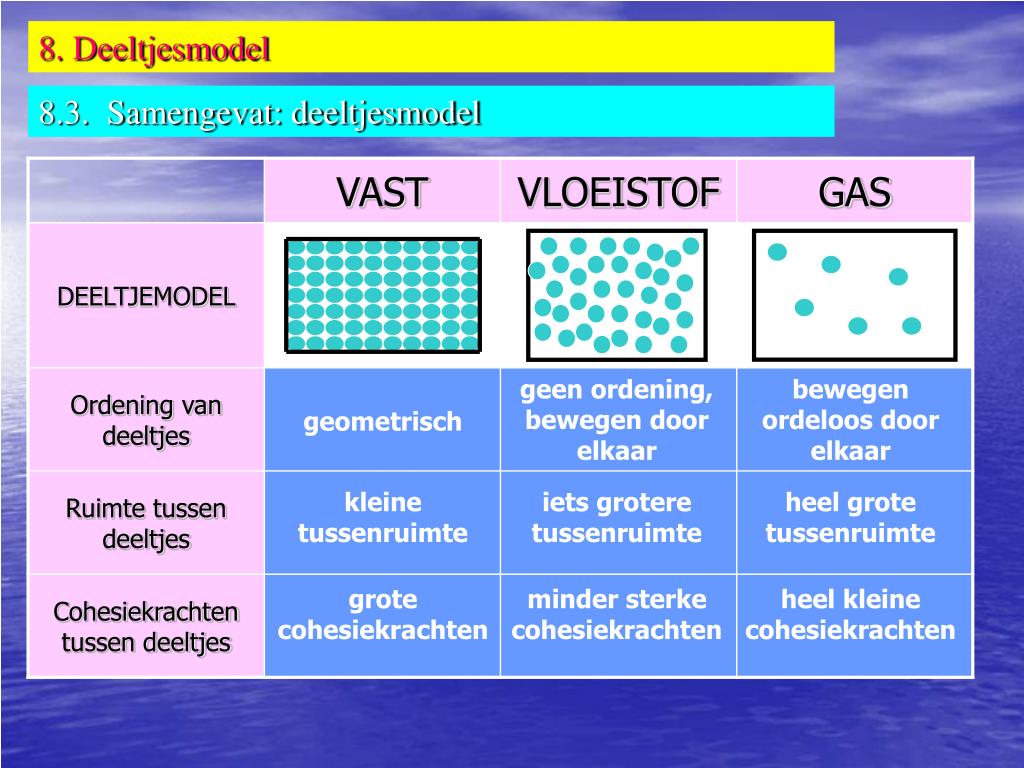
Stel je voor: je bent aan het koken en je weet dat water kookt bij 100 graden Celsius. Dat is een direct gevolg van de eigenschappen van de watermoleculen! Of je begrijpt waarom ijs drijft (ook al is het vast) doordat de watermoleculen zich in een roosterstructuur organiseren. Deze kennis helpt je om de wereld om je heen beter te begrijpen en om doordachte beslissingen te nemen.
Discipline en doorzettingsvermogen
Het kan soms lastig zijn om al die formules en structuren te onthouden, maar onthoud: discipline is de sleutel! Door regelmatig te oefenen en de stof te herhalen, zul je merken dat het steeds makkelijker wordt. Zie het als een training voor je hersenen. Elke keer dat je een nieuw concept leert, maak je nieuwe verbindingen in je hersenen. Hoe meer je oefent, hoe sterker die verbindingen worden.

Laat je niet ontmoedigen door fouten. Fouten zijn juist leermomenten! Analyseer waar je fout zat en probeer het opnieuw. Dat is hoe je groeit, zowel in de scheikunde als in het leven. Het vraagt doorzettingsvermogen, maar de voldoening die je krijgt als je iets begrijpt, is het dubbel en dwars waard!
Motivatie en plezier
Het klinkt misschien gek, maar scheikunde kan ook heel leuk zijn! Probeer de stof te verbinden met de wereld om je heen. Ga op zoek naar experimenten die je thuis kunt doen (onder toezicht van een volwassene natuurlijk!) of kijk naar interessante video’s over scheikunde. Je zult versteld staan van de prachtige en fascinerende wereld die zich achter de moleculaire structuren schuilhoudt.
.jpg)
Onthoud: leren is een reis, geen bestemming. Geniet van de reis en wees nieuwsgierig! Elke vraag die je stelt, elke formule die je begrijpt, elke moleculaire stof die je leert kennen, brengt je een stap dichter bij een beter begrip van de wereld.
Succes met studeren en blijf nieuwsgierig!