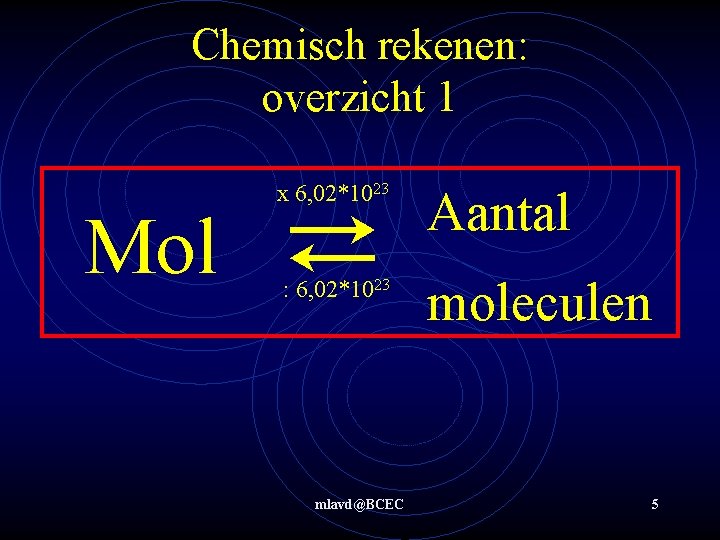
Wat Is Een Mol Scheikunde
Hé jij! Heb je je ooit afgevraagd wat die rare term 'mol' betekent in scheikunde? Nee, we hebben het niet over het beestje dat je gazon omwoelt. Het is iets... anders. Veel anders! Maak je klaar voor een duik in de wondere wereld van de mol!
Wat is een mol? Even geen graafwerk!
Oké, dus wat is een mol nou eigenlijk? Simpel gezegd: het is een aantal. Een héél groot aantal. Denk aan een dozijn eieren, maar dan veel groter. We praten hier over atomen en moleculen, niet over taart bakken.
Een mol is gelijk aan 6.022 x 1023. Indrukwekkend, toch? Dat getal noemen we het getal van Avogadro. Klinkt ingewikkeld, maar onthoud gewoon: het is een gigantisch grote hoop.
Must Read
Waarom hebben we zo'n enorm getal nodig?
Goede vraag! Atomen en moleculen zijn superklein! Zo klein, dat je ze niet kunt zien, zelfs niet met een normale microscoop. Om ze te kunnen wegen en ermee te rekenen, hebben we een handige manier nodig om een grote groep tegelijk te meten. Enter: de mol!
Stel je voor dat je 6.022 x 1023 knikkers hebt. Dat is ongeveer genoeg om de hele aarde te bedekken met een laag van een paar kilometer dik! Dat geeft wel een beetje een idee van hoe groot dat getal is!
Chemici gebruiken de mol om te praten over hoeveelheden van stoffen. Het is een soort scheikundige 'dozijn'. In plaats van 12 eieren, heb je 6.022 x 1023 atomen of moleculen.
Waarom de naam 'mol'? Geen idee!
Eerlijk gezegd weet niemand zeker waarom ze het een 'mol' hebben genoemd. Het heeft waarschijnlijk niets te maken met de kleine graafbeestjes. Misschien vond iemand het gewoon een leuke naam. Of misschien was het een inside joke onder scheikundigen. We zullen het waarschijnlijk nooit zeker weten!
Maar hé, het is wel een memorabele naam, toch? Wie vergeet er nou een 'mol' in de scheikunde? Veel leuker dan "Eenheid van de Hoeveelheid Substantie," toch?
De mol in actie: Praktijkvoorbeelden
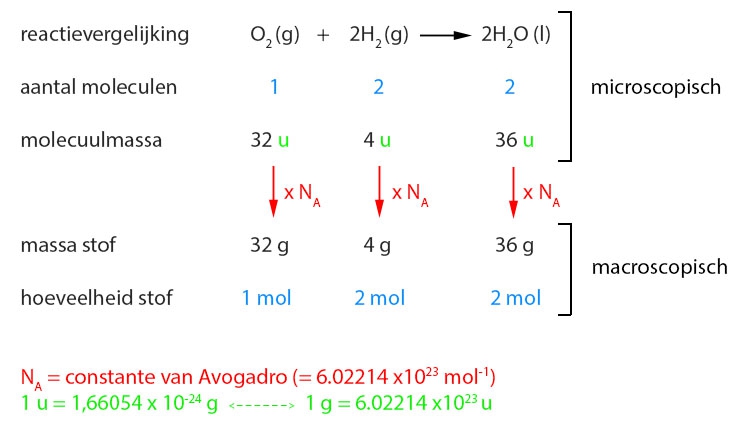
Laten we eens kijken hoe we die mol nou echt gebruiken. Stel, je wilt water (H2O) maken. Je weet dat water bestaat uit waterstof (H) en zuurstof (O).
Om één mol water te maken, heb je één mol zuurstofatomen en twee mol waterstofatomen nodig. Aha! De verhoudingen zijn belangrijk!
Dankzij de mol weten we hoeveel gram waterstof en zuurstof we precies nodig hebben. Zo kunnen we precies de juiste hoeveelheid water maken, zonder verspilling! (En hopelijk zonder explosies!)
De mol maakt scheikunde super praktisch. Denk aan het berekenen van hoeveel medicijnen iemand nodig heeft, of hoeveel mest een plant nodig heeft. Het is allemaal gebaseerd op die handige mol!
+1.jpg)
Molmassa: De link tussen mol en grammen
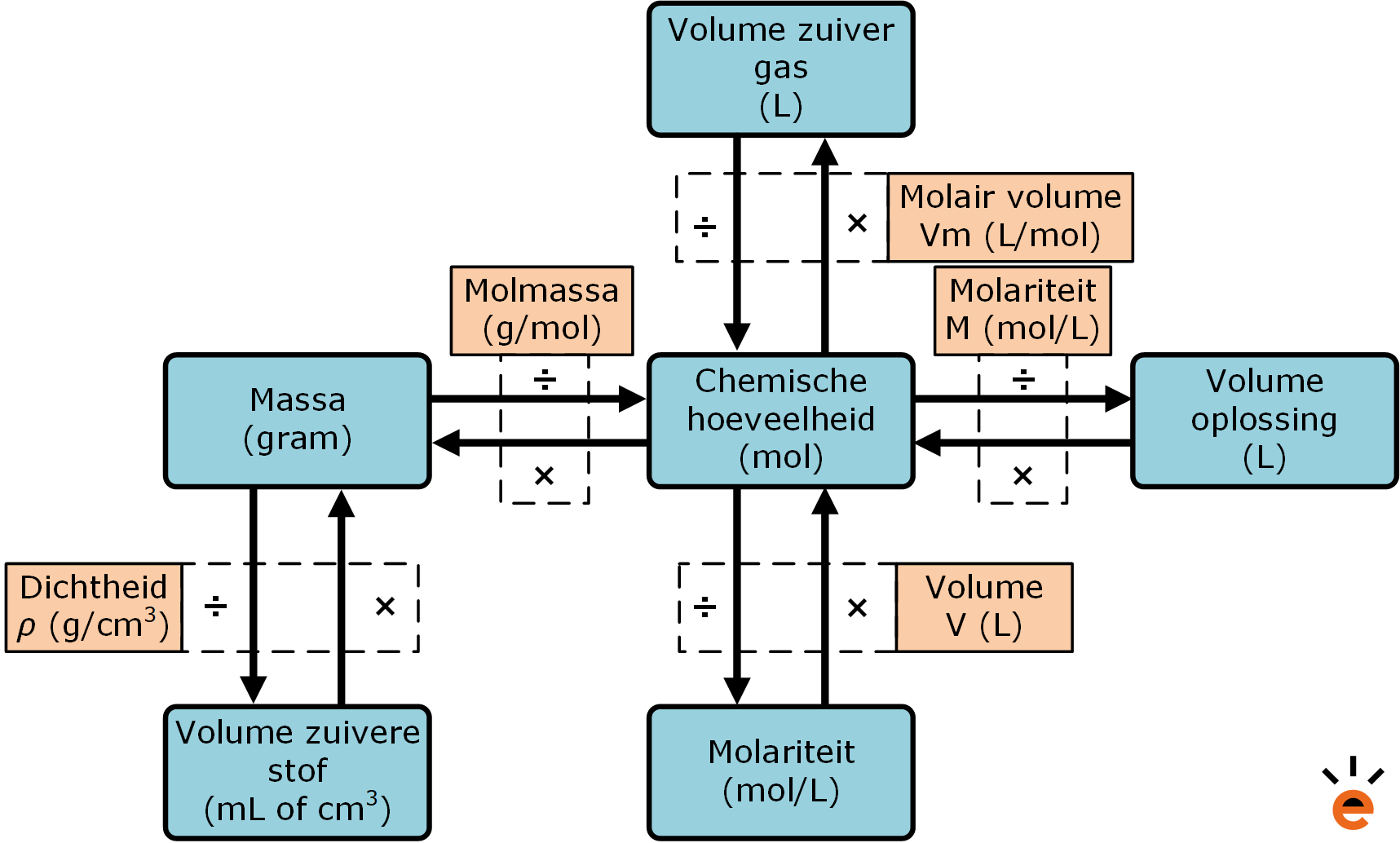
Hier komt een ander belangrijk concept om de hoek kijken: molmassa. Molmassa is de massa van één mol van een stof. Het wordt uitgedrukt in gram per mol (g/mol).
Voor water is de molmassa ongeveer 18 g/mol. Dat betekent dat één mol water (6.022 x 1023 watermoleculen) 18 gram weegt. Superhandig!
Met behulp van de molmassa kunnen we heel makkelijk grammen omrekenen naar mollen, en vice versa. Stel je voor: je hebt 36 gram water. Hoeveel mol is dat? Nou, 36 gram / 18 g/mol = 2 mol water. Simpel!
Waarom zou je dit allemaal willen weten?
Misschien denk je nu: "Waarom zou ik me hier druk over maken? Ik ben geen scheikundige!" Nou, zelfs als je geen labjas draagt, is de mol relevant voor je dagelijks leven!
Denk aan voeding. De hoeveelheid vitaminen en mineralen in je eten wordt vaak uitgedrukt in millimol (duizendste van een mol). Zo weet je precies hoeveel je binnenkrijgt! Gezondheid begint met scheikunde!
Of denk aan het milieu. De concentratie van vervuilende stoffen in de lucht of het water wordt ook vaak gemeten in mollen per liter. Zo kunnen we de vervuiling in de gaten houden! Een schone planeet, dankzij scheikunde!
En wie weet, misschien word je wel geïnspireerd om scheikunde te gaan studeren! De wereld heeft meer slimme scheikundigen nodig om problemen op te lossen. De mol kan de sleutel zijn tot een betere toekomst!
De mol: Meer dan alleen een getal
De mol is niet zomaar een getal. Het is een tool, een concept, een sleutel tot het begrijpen van de wereld om ons heen. Het is de basis van de moderne scheikunde en speelt een cruciale rol in talloze toepassingen.
Dus de volgende keer dat je de term 'mol' hoort, denk dan niet aan een graafbeestje. Denk aan die 6.022 x 1023 atomen of moleculen, die samen de bouwstenen vormen van alles wat we kennen.

De mol: klein van formaat, groots in impact!
Samenvattend: De Mol in een Notendop
Oké, laten we de belangrijkste punten nog eens herhalen:
- Een mol is een heel groot aantal: 6.022 x 1023.
- Het getal van Avogadro.
- We gebruiken de mol om atomen en moleculen te meten, omdat ze zo klein zijn.
- Molmassa is de massa van één mol van een stof.
- De mol is superhandig om te rekenen met scheikundige stoffen.
- De mol is relevant voor je dagelijks leven, bijvoorbeeld in voeding en milieu.
En het belangrijkste: Scheikunde is leuk!
Dus, de volgende keer dat je je vrienden wilt imponeren met je kennis, drop dan even de term 'mol'. Wedden dat ze onder de indruk zijn?
Veel plezier met het verkennen van de wondere wereld van de scheikunde! En onthoud: De mol is je vriend!