Wat Is Een Geconjugeerde Base

Ken je dat? Dat moment waarop je keukentafel vol ligt met boodschappen, je probeert een ingewikkeld recept te volgen, en je ineens beseft dat je een cruciaal ingrediënt mist? Zo voelde ik me dus gisteren, toen ik in de keuken stond te zwoegen op een zuurdesembrood. De desem bubbelde vrolijk, het water was precies op temperatuur... maar ineens realiseerde ik me dat ik geen idee had wat een geconjugeerde base nou precies was. Het leek wel alsof de hele chemie-wereld me uitlachte! En dat terwijl ik dacht dat ik aardig op de hoogte was. Tijd om de theorie weer eens op te frissen, dacht ik zo. En dat ga ik nu met jullie delen!
Want eerlijk, wie heeft nou zin in een stoffig scheikundeboek als je ook gewoon een gezellig artikel kunt lezen? Laten we dus eens duiken in de wondere wereld van zuren, basen, en hun geconjugeerde partners. En geloof me, het is minder eng dan het klinkt.
Wat is een zuur? (En waarom geeft het iets weg?)
Oké, voordat we überhaupt kunnen praten over geconjugeerde basen, moeten we even terug naar de basis (ha!). Wat is een zuur? Simpel gezegd, een zuur is een stof die protonen (H+, positief geladen waterstofionen) kan afstaan. Denk aan citroensap (citroenzuur) of azijn (azijnzuur). Ze zijn zuur, omdat ze die H+-jes graag kwijt willen. Het is net alsof ze een klein cadeautje hebben dat ze graag aan iemand anders geven.
Must Read
Er zijn verschillende theorieën over wat een zuur precies is, maar de Brønsted-Lowry definitie is voor ons nu het belangrijkst. Die zegt dus: een zuur is een protondonor. Punt.
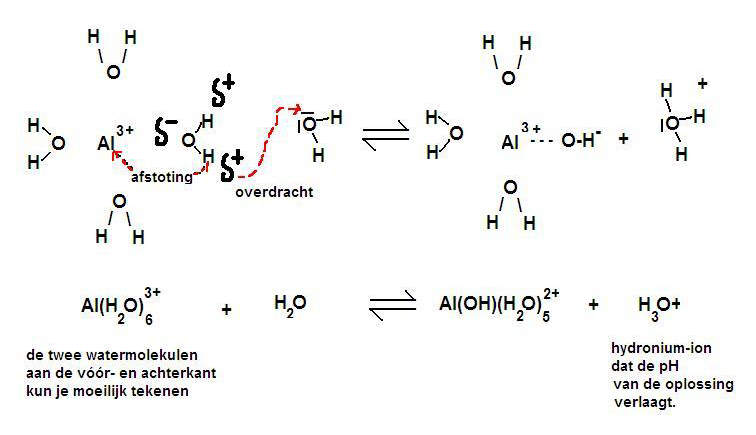
Even tussendoor: wist je dat de zuurgraad (pH) gemeten wordt aan de hand van de concentratie H+-ionen? Lage pH = veel H+ = zuur. Hoge pH = weinig H+ = basisch. Handig om te weten!
En dan nu: de Base (De gulzige ontvanger)
Je raadt het al, een base is het tegenovergestelde van een zuur. Volgens Brønsted-Lowry is een base een protonacceptor. Een base neemt dus protonen op. Denk aan bijvoorbeeld ammoniak (NH3) of natronloog (NaOH). Die stoffen vinden het heerlijk om een H+-je te ontvangen.
Nu snap je waarschijnlijk al een beetje waar dit naartoe gaat. Als een zuur een proton afstaat, en een base een proton opneemt... dan ontstaat er iets nieuws. Iets met een relatie. En dat is waar de geconjugeerde base om de hoek komt kijken.

Even een gedachte-experiment: stel je voor dat een zuur en een base elkaar ontmoeten op een feestje. Het zuur heeft een cadeautje (een proton), en de base is dolblij om dat cadeautje aan te nemen. Wat gebeurt er na de uitwisseling?
Tadaa: De Geconjugeerde Base in volle glorie
Hier komt de clou. Wanneer een zuur een proton (H+) afstaat, verandert het in iets anders. Dat "iets anders" is de geconjugeerde base. Het is dus wat er overblijft van het zuur, nadat het zijn proton heeft gedoneerd. Het heeft nu de potentie om weer een proton te accepteren, en dus als een base te functioneren (maar dan de "geconjugeerde" versie!).
Kijk, we nemen als voorbeeld een willekeurig zuur, HA (A staat dan voor de rest van de molecule). Als HA een proton (H+) afstaat, krijg je dit:
HA → H+ + A-
Die A- is dus de geconjugeerde base van het zuur HA. Let op de negatieve lading! Die komt doordat het zuur een positief geladen proton heeft afgestaan.
Zie je het? De geconjugeerde base is een soort "ex-zuur" dat nu de potentie heeft om een proton terug te pakken. Het is net alsof je een broek leent aan je vriend, en je het later weer terug kunt vragen. (Alleen dan met protonen.)
Een paar voorbeelden om het te laten bezinken:
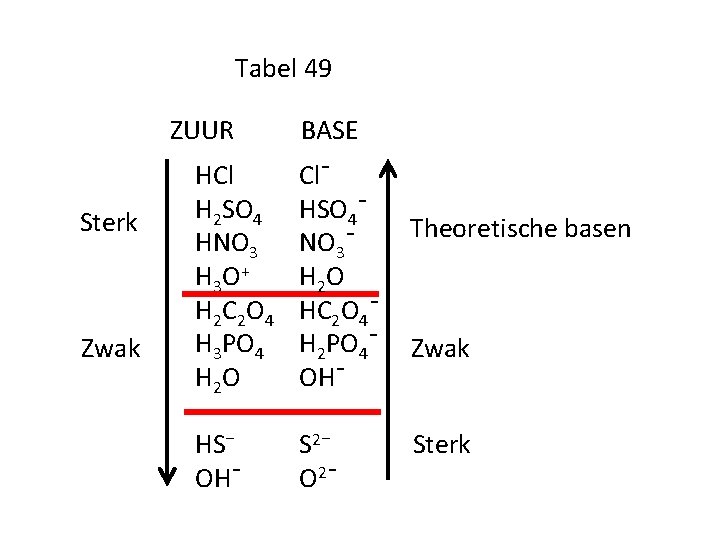
- Zuur: HCl (zoutzuur)
- Geconjugeerde base: Cl- (chloride-ion)
- Zuur: CH3COOH (azijnzuur)
- Geconjugeerde base: CH3COO- (acetaat-ion)
- Zuur: H2O (water)
- Geconjugeerde base: OH- (hydroxide-ion)
Zie je het patroon? Haal een H+ weg, en je hebt de geconjugeerde base. En vergeet die lading niet!
De Geconjugeerde Base in Actie
Oké, nu weten we wat een geconjugeerde base is, maar wat hebben we eraan? Nou, ze spelen een cruciale rol in zuur-base reacties. Denk aan de neutralisatie van een zuur met een base. Stel je voor: je hebt maagzuur (HCl) en je neemt een Rennie (bevat een base, bijvoorbeeld magnesiumcarbonaat). De base neutraliseert het zuur, en er ontstaat een zout en water. En ja, de geconjugeerde base speelt hierbij een belangrijke rol!
Het is eigenlijk een soort ping-pong spel met protonen. Het zuur staat een proton af aan de base, en de base accepteert het proton van het zuur. Daarbij ontstaan de geconjugeerde base en het geconjugeerde zuur (daarover zo meer!).
Bovendien is de sterkte van een zuur gerelateerd aan de stabiliteit van zijn geconjugeerde base. Een sterk zuur staat makkelijk een proton af, en dat betekent dat de geconjugeerde base die ontstaat relatief stabiel is. Andersom geldt: een zwak zuur staat minder makkelijk een proton af, en de geconjugeerde base is minder stabiel.
Even een voorbeeld: HCl is een sterk zuur. Cl- is een relatief stabiele geconjugeerde base. CH3COOH is een zwak zuur. CH3COO- is een relatief instabiele geconjugeerde base.
En wat dan met het geconjugeerde Zuur?
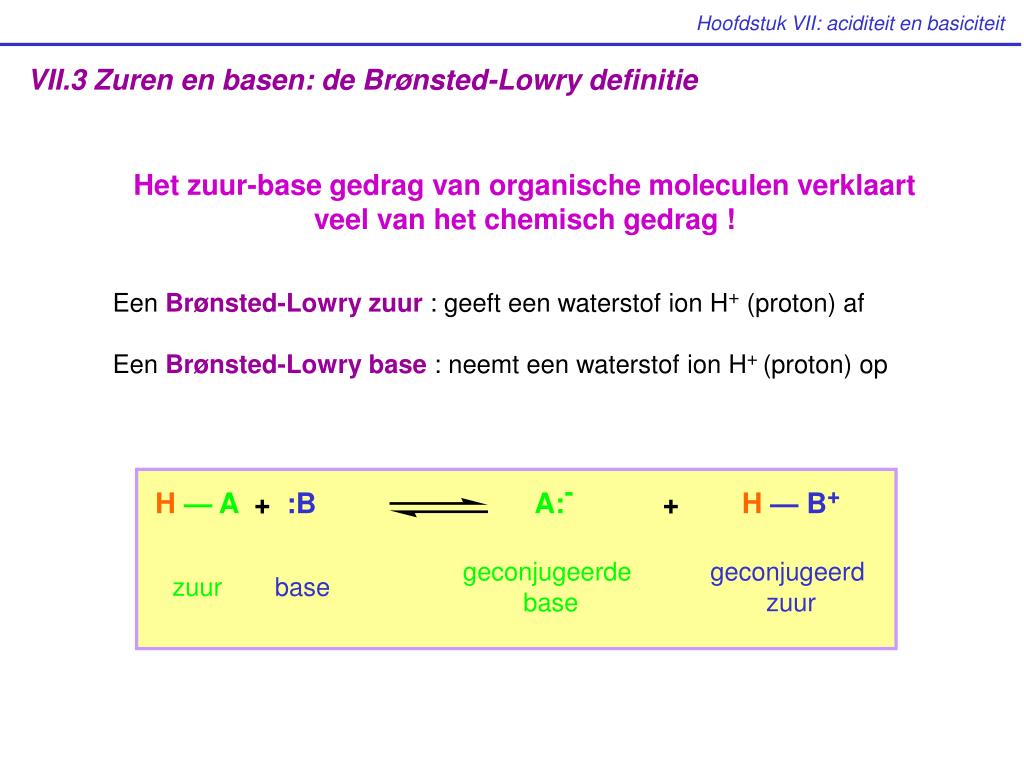
Ja, natuurlijk! We hebben het steeds over de geconjugeerde base gehad, maar er is ook zoiets als het geconjugeerde zuur. Dat is wat er gebeurt met de base, nadat het een proton heeft opgenomen. Het is dus de base plus een proton. De geconjugeerde base en het geconjugeerde zuur vormen samen een geconjugeerd zuur-base paar.
Als we weer ons willekeurige zuur HA en een willekeurige base B nemen, dan krijgen we dit:
HA + B ⇌ A- + BH+
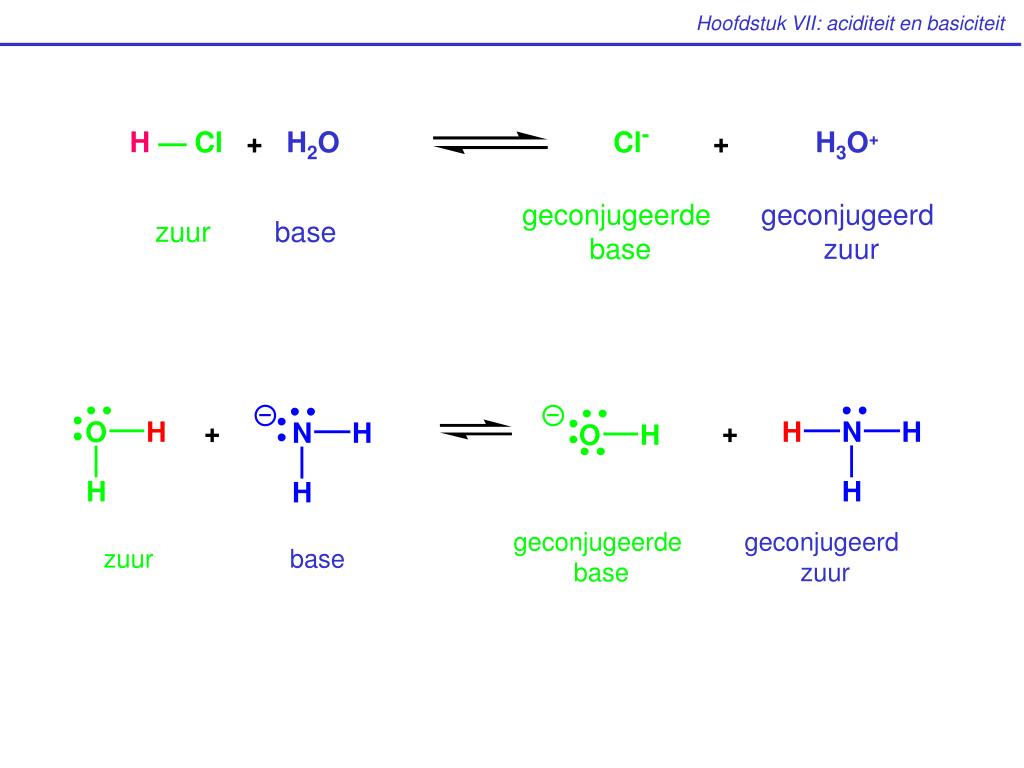
In dit geval is A- de geconjugeerde base van HA, en BH+ is het geconjugeerde zuur van B.
Snap je het? Het is een heen-en-weer spel. Zuur geeft een proton weg en wordt een geconjugeerde base. Base neemt een proton op en wordt een geconjugeerd zuur.
Conclusie: Het is allemaal een kwestie van perspectief!
Dus, wat hebben we geleerd? Een geconjugeerde base is wat er overblijft van een zuur, nadat het een proton heeft afgestaan. Het is een cruciale speler in zuur-base reacties, en de stabiliteit ervan is gerelateerd aan de sterkte van het oorspronkelijke zuur. Het is eigenlijk allemaal een kwestie van perspectief. Wat is een zuur? Wat is een base? Het hangt er maar net vanaf of je protonen aan het afstaan of aan het opnemen bent.
En weet je wat het mooiste is? Nu weet ik, en jij, dat als we in de toekomst een zuurdesembrood bakken, en er staat iets over geconjugeerde basen in het recept... dan snappen we het gewoon. Geen paniek meer! Missie geslaagd!
Oké, ik ga nu verder met mijn brood. Hopelijk heb je er wat van opgestoken! En onthoud: scheikunde is niet eng, het is gewoon... een beetje zuur (en basisch!). Tot de volgende keer!





![Verhouding [zwak zuur] : [ geconjugeerde base] berekenen - YouTube](https://i.ytimg.com/vi/Uaz6COWWgEw/maxresdefault.jpg)