Wat Is De Osmotische Waarde
Hallo allemaal! Zit je weer eens te zwoegen op je biologie huiswerk en kom je het begrip "osmotische waarde" tegen? Geen zorgen, je bent niet de enige! Veel leerlingen vinden dit een lastig onderwerp. Maar geloof me, met de juiste uitleg is het echt te begrijpen. We gaan het stap voor stap aanpakken, zodat je straks met vertrouwen je toets in gaat!
We begrijpen dat biologie soms overweldigend kan zijn. Al die nieuwe termen en processen… het is alsof je een compleet nieuwe taal leert! Daarom gaan we de osmotische waarde ontleden in hapklare brokken. Geen ingewikkelde formules meteen, maar eerst een goede basis.
Wat is Osmose Eigenlijk?
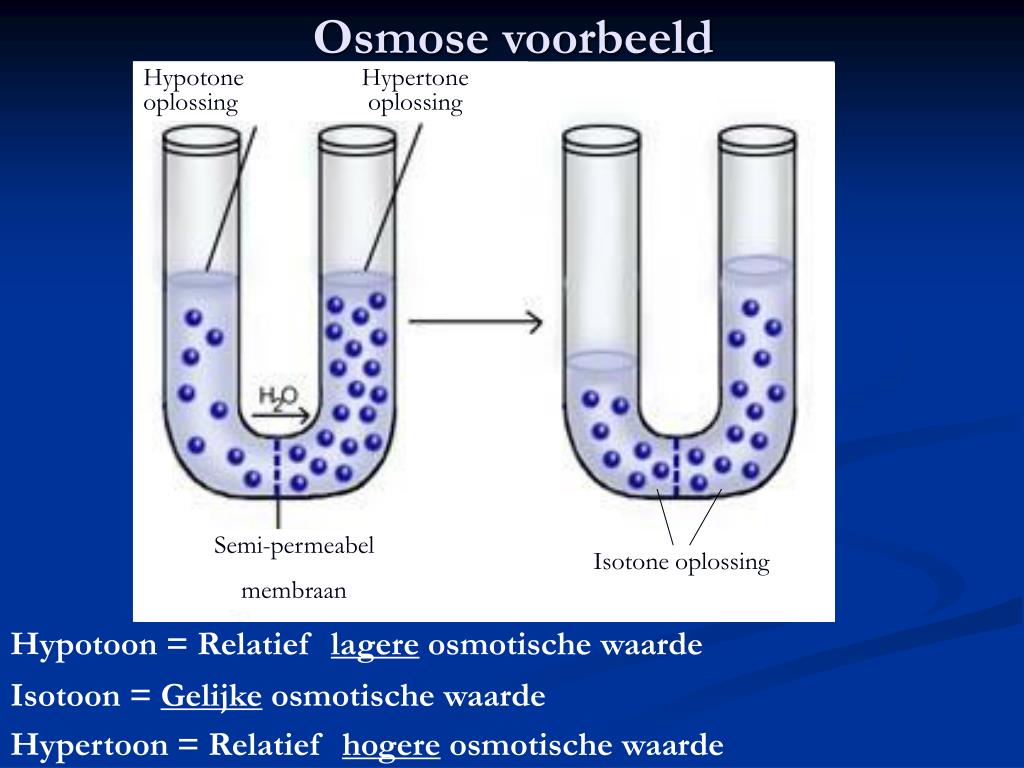
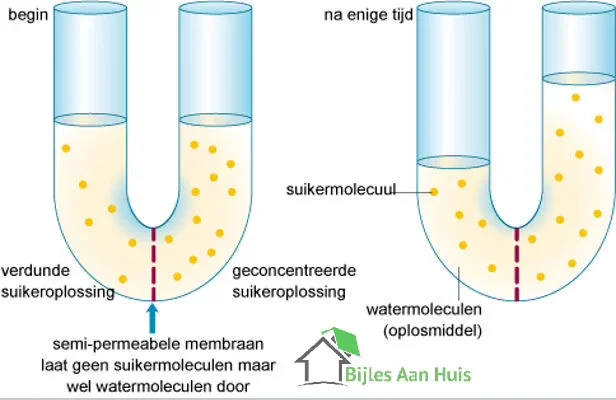
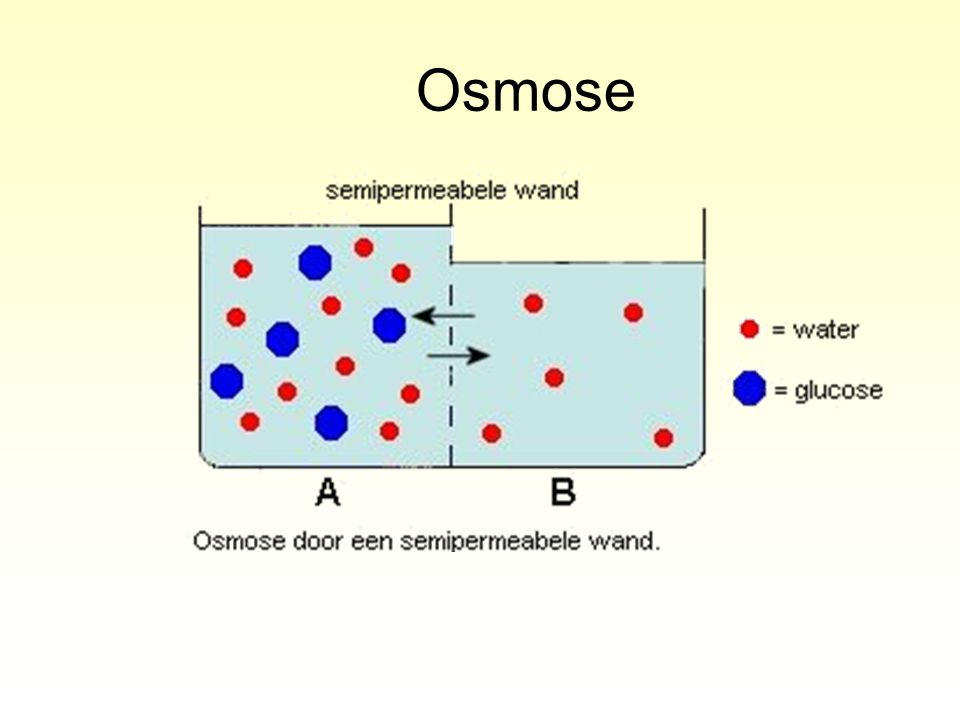
Laten we beginnen bij het begin: osmose. Stel je voor: je hebt een bak met water, en in het midden, gescheiden door een semipermeabel membraan (een soort filter met hele kleine gaatjes), heb je een oplossing met bijvoorbeeld zout. Dat membraan laat wel water door, maar geen zout.
Must Read
Wat er gebeurt is dat het water van de kant met de laagste zoutconcentratie (waar dus meer "puur" water is) naar de kant met de hogere zoutconcentratie gaat. Dit gebeurt omdat de natuur streeft naar evenwicht. Het water probeert de zoutconcentratie aan beide kanten gelijk te maken. Dit proces, de verplaatsing van water door een semipermeabel membraan, noemen we osmose.
Waarom is dit belangrijk?
Osmose is cruciaal voor het leven, zowel bij planten als bij dieren (en dus ook bij ons!). Denk bijvoorbeeld aan:
- Planten: Planten nemen water op via hun wortels door osmose. Zonder osmose zouden ze uitdrogen!
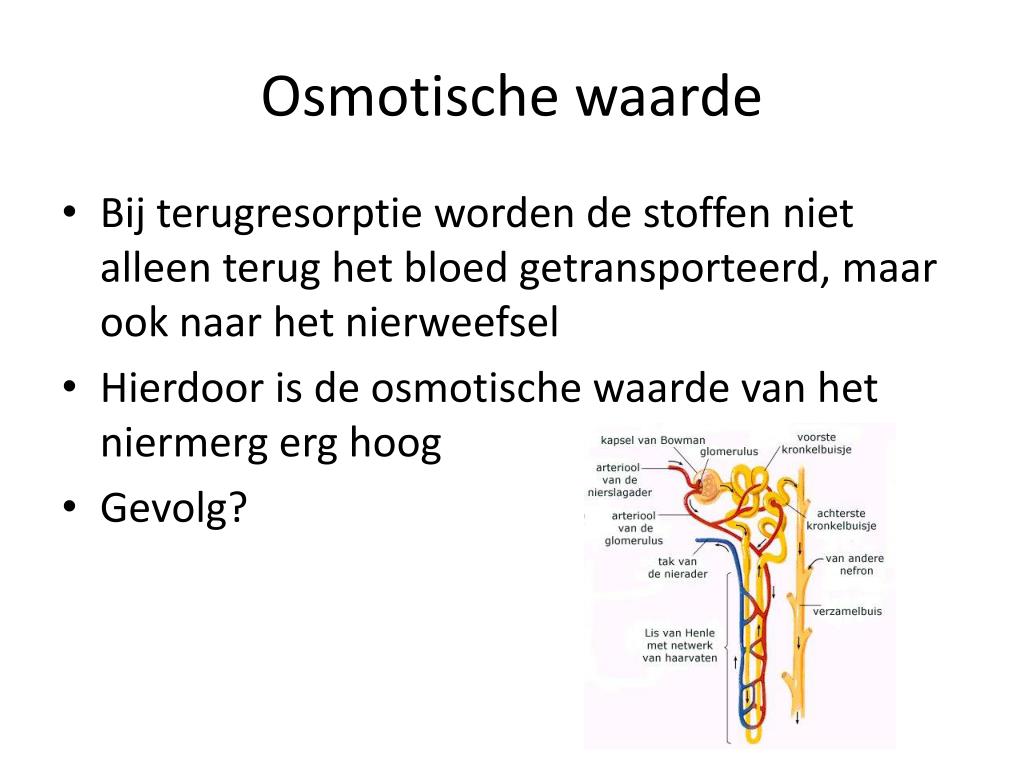
- Dieren: Osmose speelt een belangrijke rol bij het reguleren van de waterhuishouding in ons lichaam. Onze nieren gebruiken osmose om afvalstoffen uit ons bloed te filteren.
De Osmotische Waarde: Een Krachtmeting
Nu komt de osmotische waarde om de hoek kijken. De osmotische waarde is een maat voor de concentratie opgeloste stoffen (zoals zout, suiker, of andere ionen) in een oplossing. Hoe hoger de concentratie opgeloste stoffen, hoe hoger de osmotische waarde, en hoe sterker de oplossing water "aanzuigt" door osmose.
Je kunt het zien als een soort "zuigkracht" van het water. Een oplossing met een hoge osmotische waarde heeft een sterke zuigkracht, omdat het veel water wil aantrekken om de concentratie opgeloste stoffen te verdunnen.

Simpel gezegd:
- Hoge osmotische waarde: Veel opgeloste stoffen, sterke zuigkracht voor water.
- Lage osmotische waarde: Weinig opgeloste stoffen, zwakke zuigkracht voor water.
Voorbeeld: Een Vergelijking
Stel, je hebt twee bekers. In de ene beker zit kraanwater (lage osmotische waarde), en in de andere beker zit een zoutoplossing (hoge osmotische waarde). Als je een cel (bijvoorbeeld een rode bloedcel) in kraanwater legt, zal er water de cel in stromen, omdat het water buiten de cel een lagere osmotische waarde heeft dan de inhoud van de cel. De cel kan opzwellen en zelfs barsten.
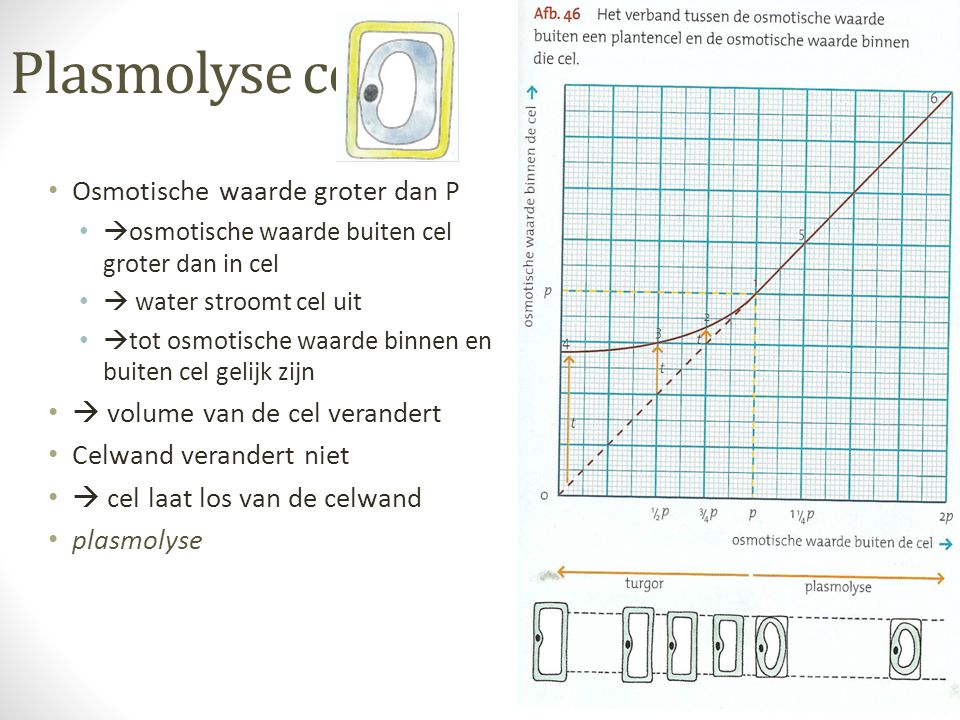
Leg je dezelfde cel in de zoutoplossing, dan zal er water uit de cel stromen, omdat de zoutoplossing een hogere osmotische waarde heeft dan de inhoud van de cel. De cel zal krimpen en verschrompelen.
Waarom is de Osmotische Waarde Zo Belangrijk?
De osmotische waarde is essentieel voor het in stand houden van de celstructuur en -functie. Cellen moeten in een omgeving leven met de juiste osmotische waarde, anders kunnen ze beschadigd raken of zelfs afsterven. Dit geldt niet alleen voor individuele cellen, maar ook voor hele organismen.

Denk aan:
- Intraveneuze vloeistoffen (infuus): In het ziekenhuis krijgen patiënten vaak een infuus. De vloeistof in het infuus moet de juiste osmotische waarde hebben, anders kan het schade aanrichten aan de bloedcellen.
- Landbouw: Boeren moeten rekening houden met de osmotische waarde van de bodem. Als de bodem te zout is (hoge osmotische waarde), kunnen planten geen water opnemen en zullen ze verdorren.
- Conserveren van voedsel: Door bijvoorbeeld zout of suiker toe te voegen aan voedsel (zoals bij het maken van jam of het pekelen van vlees) verhoog je de osmotische waarde. Hierdoor wordt het water uit de bacteriën getrokken, waardoor ze niet kunnen groeien en het voedsel langer houdbaar is.
Praktische Toepassingen en Oefeningen
Oké, genoeg theorie! Laten we eens kijken hoe je deze kennis in de praktijk kunt brengen:
Oefening 1: De Slinkende Komkommer
Benodigdheden: Een komkommer, zout, een mes, een schaal.
Stappen:

- Snijd de komkommer in plakjes.
- Leg een paar plakjes in een schaal met zout.
- Leg een paar plakjes in een schaal zonder zout.
- Wacht een half uur en observeer.
Wat gebeurt er? De komkommerplakjes in de schaal met zout zullen slinken en zachter worden. Dit komt doordat het zout de osmotische waarde van de omgeving verhoogt, waardoor water uit de komkommercellen wordt getrokken.
Oefening 2: De Aardappeltest
Benodigdheden: Twee glazen, water, zout, twee stukjes aardappel van gelijke grootte.
Stappen:
- Vul één glas met kraanwater.
- Vul het andere glas met een zoutoplossing.
- Leg in elk glas een stukje aardappel.
- Wacht een paar uur en voel aan de stukjes aardappel.
Wat gebeurt er? De aardappel in het zoute water zal slapper worden. De aardappel in het kraanwater blijft steviger.

Daily Application: Denk aan Je Hydratatie!
Nu je weet wat de osmotische waarde is, kun je er ook in je dagelijks leven op letten. Als je bijvoorbeeld veel zout eet, heeft je lichaam meer water nodig om de osmotische waarde in je bloed op peil te houden. Daarom is het belangrijk om voldoende water te drinken, vooral als je veel zout of suiker hebt gegeten. Kies liever water boven gezoete drankjes, omdat die de osmotische waarde van je bloed nog verder verhogen. Probeer ook eens te letten op de ingrediëntenlijst van voedingsmiddelen. Veel bewerkte voedingsmiddelen bevatten verborgen zouten.
Tips voor het Leren en Onthouden
Hier zijn nog een paar tips om de osmotische waarde beter te begrijpen en te onthouden:
- Visualiseer: Maak een tekening of een schema om het proces van osmose te visualiseren.
- Verbind: Probeer de concepten te verbinden met voorbeelden uit het dagelijks leven.
- Leg het uit: Leg de osmotische waarde uit aan iemand anders. Door het uit te leggen, dwing je jezelf om de stof echt te begrijpen.
- Oefen: Maak oefenopgaven en vraag je docent om hulp als je vastloopt.
Conclusie
De osmotische waarde is misschien een ingewikkeld concept, maar met de juiste uitleg en een beetje oefening is het zeker te begrijpen. Onthoud dat het gaat om de concentratie opgeloste stoffen in een oplossing en de "zuigkracht" die dit veroorzaakt. Het is een cruciaal concept voor het begrijpen van veel biologische processen, van het opnemen van water door planten tot het reguleren van de waterhuishouding in ons lichaam.
Dus, de volgende keer dat je over de osmotische waarde leest, denk dan aan de slinkende komkommer en de aardappeltest. Je weet nu hoe het werkt! Blijf leren, blijf vragen stellen, en je zult zien dat biologie steeds leuker wordt!
Succes met je studie!









+heeft+dan+binnen+in+de+cel+(hypertoon)%2C+dan+zal+er+een+netto+waterverplaatsing+zijn+de+cel+in..jpg)