Wat Is De Molecuulformule Van Zuurstof

Heb je je ooit afgevraagd welke onzichtbare kracht ons in leven houdt, elk moment van de dag? Het antwoord is simpel: zuurstof. Maar zuurstof is meer dan alleen een woord; het is een essentieel element met een specifieke molecuulformule. In dit artikel gaan we dieper in op de molecuulformule van zuurstof, zodat je precies weet waar we het over hebben. Dit artikel is bedoeld voor iedereen die geïnteresseerd is in scheikunde, wetenschap of gewoon meer wil weten over de wereld om ons heen. Geen voorkennis vereist!
Wat is een Molecuulformule?
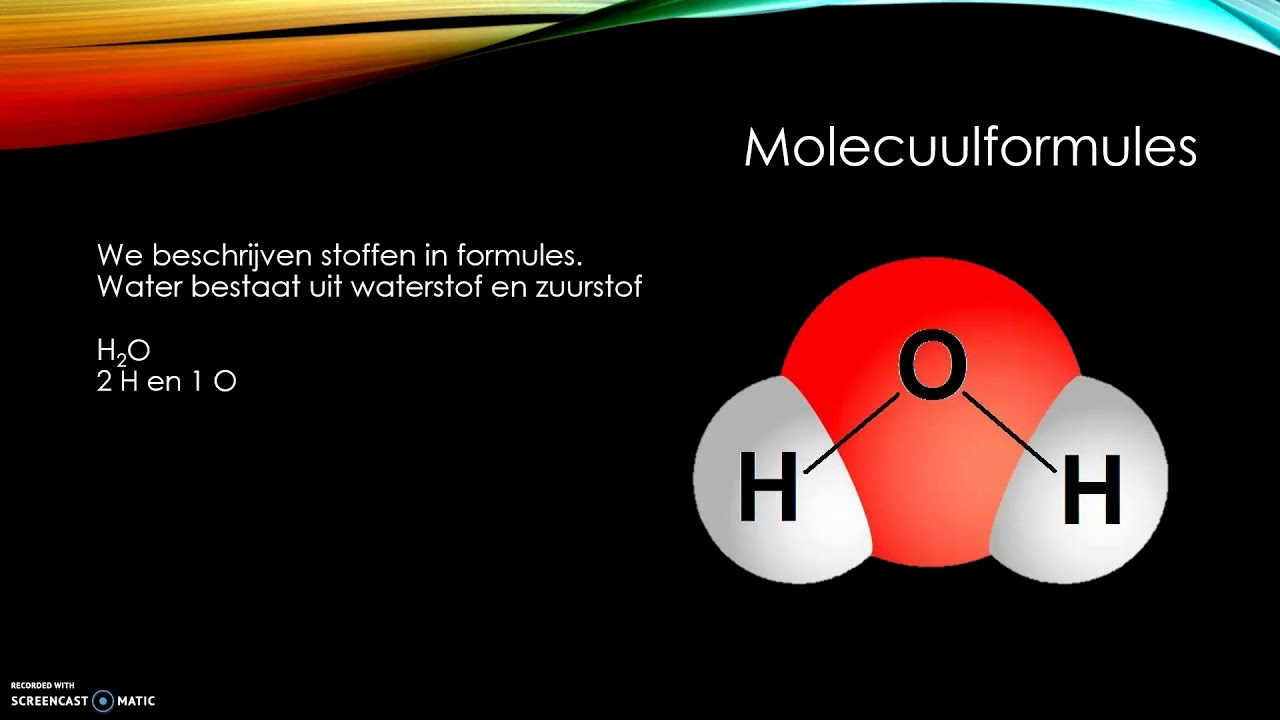
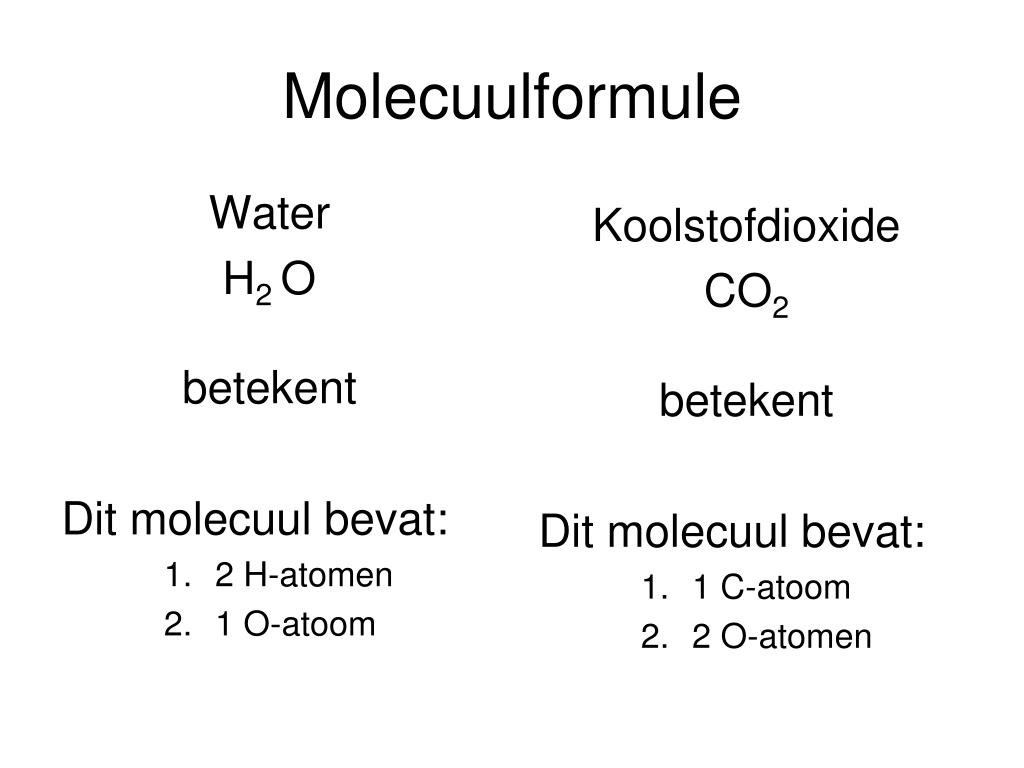
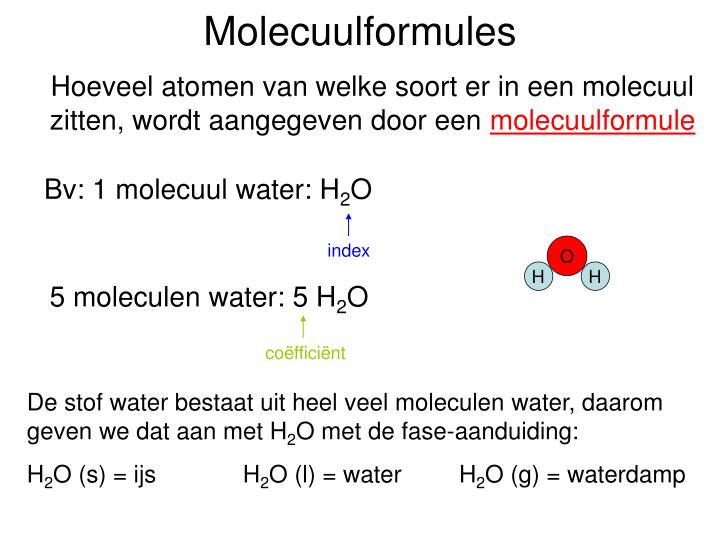
Laten we beginnen met de basis. Een molecuulformule is een manier om aan te geven welke elementen er in een molecuul zitten en hoeveel atomen van elk element er aanwezig zijn. Het is als een soort recept voor een molecuul. Bijvoorbeeld, de molecuulformule voor water is H2O. Dit betekent dat een watermolecuul bestaat uit twee waterstofatomen (H) en één zuurstofatoom (O).
De Molecuulformule van Zuurstof: O2
Nu komen we bij de kern van dit artikel: de molecuulformule van zuurstof. Die is niet simpelweg O, maar O2. Waarom die 2? Dat heeft te maken met de stabiliteit van het zuurstofatoom. Een enkel zuurstofatoom is erg reactief en wil graag een binding aangaan met een ander atoom. In de natuur komt zuurstof daarom bijna nooit als enkel atoom voor, maar juist als een molecuul bestaande uit twee zuurstofatomen.
Must Read
Waarom O2 in plaats van O?
Om dit te begrijpen, moeten we een beetje duiken in de elektronenconfiguratie van zuurstof. Een zuurstofatoom heeft zes valentie-elektronen, dat zijn de elektronen in de buitenste schil. Het streeft naar een volle buitenste schil met acht elektronen (de zogenaamde octetregel). Door een binding aan te gaan met een ander zuurstofatoom delen ze elektronen en vullen ze elkaars buitenste schillen aan. Dit resulteert in een stabiele diatomaire molecule, oftewel O2.
Verschillende Vormen van Zuurstof
Hoewel O2 de meest voorkomende vorm van zuurstof is, bestaan er ook andere vormen. De bekendste is wellicht ozon (O3). Ozon ontstaat wanneer ultraviolette straling van de zon zuurstofmoleculen splitst in losse zuurstofatomen. Deze atomen kunnen zich vervolgens binden aan andere zuurstofmoleculen en zo ozon vormen. Ozon is belangrijk omdat het een beschermende laag in de atmosfeer vormt die ons beschermt tegen schadelijke UV-straling.

- O2: De meest voorkomende vorm, essentieel voor de ademhaling.
- O3: Ozon, een beschermende laag in de atmosfeer.
- Enkel zuurstofatoom (O): Zeer reactief en komt zelden vrij voor.
Het Belang van Zuurstof voor het Leven
Zuurstof is cruciaal voor het leven zoals wij dat kennen. Het speelt een essentiële rol in de ademhaling van de meeste organismen, inclusief mensen. Tijdens de ademhaling nemen we zuurstof in, dat vervolgens wordt gebruikt om energie te produceren in een proces dat celademhaling wordt genoemd. Hierbij wordt glucose (een suiker) afgebroken in aanwezigheid van zuurstof, waarbij energie vrijkomt, samen met koolstofdioxide en water.
De reactievergelijking voor celademhaling is als volgt:

C6H12O6 + 6O2 → 6CO2 + 6H2O + Energie
Zonder zuurstof zou dit proces niet kunnen plaatsvinden en zouden we geen energie kunnen produceren om te bewegen, denken en functioneren. Planten produceren zuurstof via fotosynthese, waarbij ze zonlicht, water en koolstofdioxide gebruiken om glucose en zuurstof te maken.

Toepassingen van Zuurstof in de Industrie en Geneeskunde
Naast de fundamentele rol in het leven, heeft zuurstof talloze toepassingen in de industrie en de geneeskunde. Hier zijn enkele voorbeelden:
- Medische toepassingen: In ziekenhuizen wordt zuurstof gebruikt voor patiënten met ademhalingsproblemen, zoals longontsteking of COPD. Ook wordt het gebruikt tijdens operaties en bij reanimatie.
- Industriële toepassingen: Zuurstof wordt gebruikt bij de productie van staal, in lasprocessen en bij de verbranding van brandstoffen in raketmotoren.
- Waterzuivering: Zuurstof kan worden gebruikt om water te zuiveren door organische stoffen af te breken.
- Duiken: Duikers gebruiken speciale mengsels van gassen, waaronder zuurstof, om onder water te kunnen ademen.
Zuurstof in het Dagelijks Leven
Zuurstof is niet alleen iets voor scheikundigen en artsen; het is overal om ons heen en beïnvloedt ons dagelijks leven. Denk maar aan de volgende situaties:

- Ademhaling tijdens het sporten: Tijdens het sporten hebben je spieren meer zuurstof nodig om energie te produceren. Je ademt sneller om aan deze verhoogde behoefte te voldoen.
- Het branden van een kaars: Een kaars kan alleen branden als er voldoende zuurstof aanwezig is. Als je een glas over een brandende kaars zet, dooft de vlam omdat de zuurstof opraakt.
- Roesten van metaal: Roest is het resultaat van een chemische reactie tussen ijzer, zuurstof en water.
- Het rijpingsproces van fruit: Zuurstof speelt een rol bij het rijpingsproces van fruit. Door fruit in een afgesloten zak te bewaren, kun je het rijpingsproces vertragen.
Conclusie: Zuurstof, Meer dan Alleen een Ademteug
Hopelijk heb je nu een beter begrip van de molecuulformule van zuurstof (O2) en de cruciale rol die het speelt in ons leven en de wereld om ons heen. Van de ademhaling die ons in leven houdt tot de industriële processen die onze samenleving draaiende houden, zuurstof is een essentieel element. De diatomaire structuur (O2) is de meest voorkomende en stabiele vorm, waardoor het de levensader is van onze planeet.
Denk de volgende keer dat je een diepe adem haalt aan de complexe chemie achter deze eenvoudige handeling. Zuurstof is niet alleen een gas dat we inademen; het is een fundamentele bouwsteen van het leven zelf. Door meer te leren over de wereld om ons heen, kunnen we de wonderen van de wetenschap beter waarderen en de rol begrijpen die ze spelen in ons dagelijks leven. Blijf nieuwsgierig en blijf leren!
We hopen dat dit artikel je geholpen heeft om de molecuulformule van zuurstof en het belang ervan te begrijpen. Deel dit artikel gerust met vrienden en familie die ook geïnteresseerd zijn in wetenschap en de wonderen van de natuur!




.jpg)