Wat Is De Molaire Massa

Heb je ooit naar een recept gekeken en gedacht: "Hoeveel heb ik nu van elk ingrediënt nodig?" In de scheikunde voelen we ons soms net zo. We weten wat we willen maken (een molecuul), maar de juiste hoeveelheden van elk atoom bepalen, kan een behoorlijke uitdaging zijn. Hier komt de molaire massa om de hoek kijken! Het is een cruciaal concept dat je helpt de juiste "dosering" van elk element te bepalen om een succesvolle chemische reactie te bewerkstelligen.
Wat is Molaire Massa Eigenlijk?
Simpel gezegd, de molaire massa is de massa van één mol van een bepaalde stof. Een mol is een specifieke hoeveelheid, net zoals een dozijn (12) of een gros (144). In de scheikunde is één mol gelijk aan 6.022 x 1023 deeltjes (atomen, moleculen, ionen, etc.). Dit getal staat bekend als het getal van Avogadro, vernoemd naar de Italiaanse wetenschapper Amedeo Avogadro.
Zoals Prof. Dr. Ingrid Hollemans, chemicus aan de Universiteit van Amsterdam, het uitlegt: "De molaire massa is de brug tussen de macroscopische wereld, die we kunnen wegen op een weegschaal, en de microscopische wereld van atomen en moleculen. Het stelt ons in staat om voorspellingen te doen over hoeveel reactanten we nodig hebben om een bepaalde hoeveelheid product te maken."
Must Read
Dus, hoe bereken je de molaire massa?
Het Periodiek Systeem: Je Beste Vriend
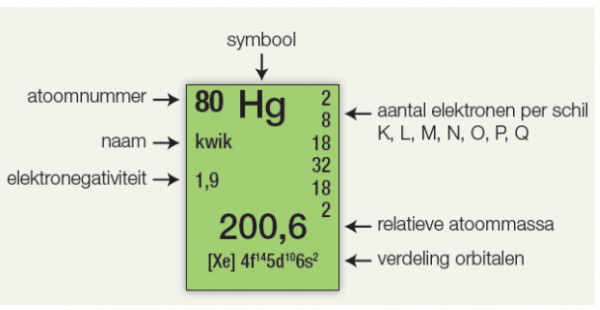
Het periodiek systeem der elementen is je grootste hulp bij het berekenen van molaire massa. Onder elk symbool van een element staat een getal – dit is de atoomgewicht of relatieve atoommassa. Meestal staat deze aangegeven in u (atomaire massa-eenheden). Om de molaire massa in gram per mol (g/mol) te krijgen, vervang je gewoon de "u" door "g/mol".
Voorbeeld:
+%EF%83%A0+getalwaarde+gelijk+aan+de+molecuulmassa+of+atoommassa+van+de+stof..jpg)
- Kijk in het periodiek systeem naar Waterstof (H). Je zult zien dat het atoomgewicht ongeveer 1.008 u is. Dit betekent dat de molaire massa van waterstof 1.008 g/mol is.
- Voor Zuurstof (O) is het atoomgewicht ongeveer 16.00 u. Dus de molaire massa van zuurstof is 16.00 g/mol.
Molaire Massa van Verbindingen Berekenen
Nu wordt het iets interessanter! Om de molaire massa van een verbinding (een molecuul dat uit meerdere atomen bestaat) te berekenen, tel je simpelweg de molaire massa's van alle atomen in de formule bij elkaar op, rekening houdend met het aantal van elk atoom.
Voorbeeld: Water (H2O)
- Water bestaat uit 2 waterstofatomen (H) en 1 zuurstofatoom (O).
- Molaire massa van 2 H atomen: 2 x 1.008 g/mol = 2.016 g/mol
- Molaire massa van 1 O atoom: 1 x 16.00 g/mol = 16.00 g/mol
- Totale molaire massa van H2O: 2.016 g/mol + 16.00 g/mol = 18.016 g/mol
Dus, de molaire massa van water is ongeveer 18.016 g/mol.

Nog een voorbeeld: Glucose (C6H12O6)
- Glucose bestaat uit 6 koolstofatomen (C), 12 waterstofatomen (H) en 6 zuurstofatomen (O).
- Molaire massa van 6 C atomen: 6 x 12.01 g/mol = 72.06 g/mol
- Molaire massa van 12 H atomen: 12 x 1.008 g/mol = 12.096 g/mol
- Molaire massa van 6 O atomen: 6 x 16.00 g/mol = 96.00 g/mol
- Totale molaire massa van C6H12O6: 72.06 g/mol + 12.096 g/mol + 96.00 g/mol = 180.156 g/mol
De molaire massa van glucose is ongeveer 180.156 g/mol.
Waarom is Molaire Massa Belangrijk?
Molaire massa is cruciaal in de scheikunde, met name bij:

- Stoichiometrie: Het berekenen van de hoeveelheden reactanten en producten in chemische reacties. Je kunt bepalen hoeveel gram van een bepaalde stof je nodig hebt om een bepaalde hoeveelheid product te maken.
- Oplossingen Bereiden: Het bepalen van de juiste hoeveelheid solute (opgeloste stof) om een oplossing met een bepaalde concentratie te maken (molariteit).
- Formulebepaling: Het bepalen van de empirische en moleculaire formule van een onbekende stof.
- Gaswetten: Het berekenen van de dichtheid van gassen bij een bepaalde temperatuur en druk.
Volgens een studie gepubliceerd in het Journal of Chemical Education (2018) getiteld "Addressing Student Difficulties with Stoichiometry Through Conceptual Change Strategies", is een goed begrip van molaire massa essentieel voor succes in de algemene scheikunde. Studenten die moeite hebben met dit concept, ondervinden vaak problemen met complexere stoichiometry-problemen.
Praktische Tips en Tools
Hier zijn enkele manieren om je begrip van molaire massa te verbeteren:
- Oefen, oefen, oefen! Maak zo veel mogelijk oefenopgaven. Begin met simpele moleculen en werk naar complexere toe.
- Gebruik online calculators: Er zijn veel gratis online molaire massa calculators beschikbaar. Deze zijn handig om je antwoorden te controleren en tijd te besparen. Zoek op "Molaire Massa Calculator" in je favoriete zoekmachine.
- Maak flashcards: Maak flashcards met de symbolen en atoomgewichten van de meest voorkomende elementen. Dit helpt je ze te onthouden.
- Visualiseer: Stel je voor dat je de atomen in een molecuul letterlijk aan het wegen bent. Dit kan helpen om het concept tastbaarder te maken.
- Gebruik een periodiek systeem app: Er zijn handige apps voor je smartphone die een periodiek systeem bevatten met de atoomgewichten van alle elementen.
Voorbeeld Oefening:
Bereken de molaire massa van zwavelzuur (H2SO4).
- Zoek de atoomgewichten van H, S en O op in het periodiek systeem.
- H: 1.008 g/mol
- S: 32.07 g/mol
- O: 16.00 g/mol
- Bereken de totale molaire massa: (2 x 1.008 g/mol) + (1 x 32.07 g/mol) + (4 x 16.00 g/mol) = 98.086 g/mol
Dus de molaire massa van zwavelzuur (H2SO4) is ongeveer 98.086 g/mol.
Veelgemaakte Fouten om te Vermijden
Let op deze veelgemaakte fouten bij het berekenen van molaire massa:
- Het vergeten van de indices: Vergeet niet dat de indices (de kleine getallen rechtsonder een element symbool) aangeven hoeveel atomen van dat element er in het molecuul zitten. Vermenigvuldig de molaire massa van dat element met de index.
- Het verkeerd aflezen van het periodiek systeem: Zorg ervoor dat je de juiste atoomgewicht afleest. Sommige periodieke systemen hebben afgeronde waarden, terwijl andere meer precieze waarden geven.
- Eenheden vergeten: Vergeet niet om de juiste eenheid (g/mol) te vermelden.
Zoals Linus Pauling, een tweevoudig Nobelprijswinnaar (Chemie en Vrede), ooit zei: "De beste manier om ideeën te hebben, is om veel ideeën te hebben." Dus blijf oefenen, experimenteren en nieuwe benaderingen proberen om de concepten in de scheikunde onder de knie te krijgen. Het begrijpen van de molaire massa is een fundamentele stap op weg naar chemisch succes.





.jpg)
+van+een+stof+is+in+getalwaarde+gelijk+aan+de+molecuulmassa+of+atoommassa+van+de+stof..jpg)



![Molariteit Molariteit concentratie van stof X [X] = Eenheid molair M](https://slideplayer.nl/slide/17168099/99/images/2/Molariteit+Voorbeeld+[C6H12O6]+%3D+%3D+%3D+0%2C42+M.jpg)




