Verschil Verzadigd En Onverzadigd Vet Scheikunde

Lieve studenten, sta even stil bij de wonderen van de chemie. Het is meer dan alleen formules en reacties; het is een venster op de complexiteit van de wereld om ons heen, van de kleinste atomen tot de meest complexe levensvormen. Vandaag duiken we in een fascinerend aspect: het verschil tussen verzadigde en onverzadigde vetten.
Misschien denk je direct aan voeding, en dat is niet gek! Vetten spelen een cruciale rol in onze gezondheid. Maar laten we de lens even verleggen en ons focussen op de chemische structuur. Want daar, in de moleculaire wereld, ligt de sleutel tot het begrijpen van het verschil en de consequenties daarvan.
De basis: Koolstof en Waterstof
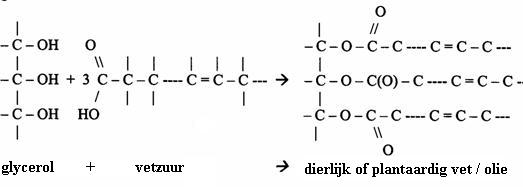
Alles begint met koolstof (C). Koolstof is een echte verbinder, een bouwsteen van het leven. Het kan tot vier bindingen aangaan met andere atomen, waaronder waterstof (H). In vetzuren, de basiscomponenten van vetten, vormen koolstofatomen lange ketens.
Must Read
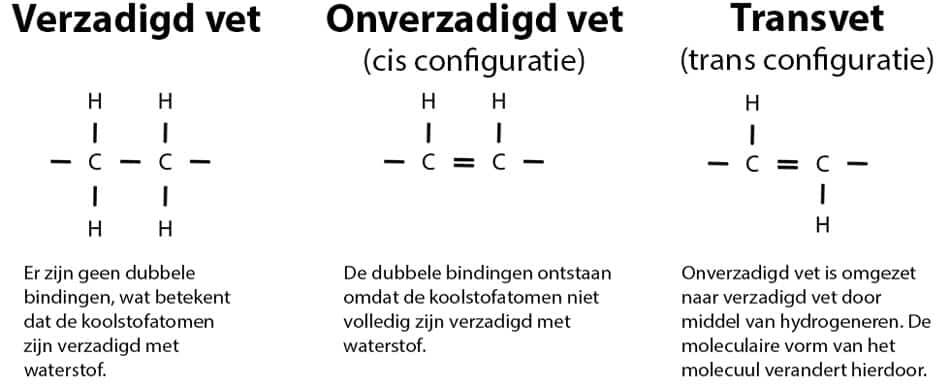
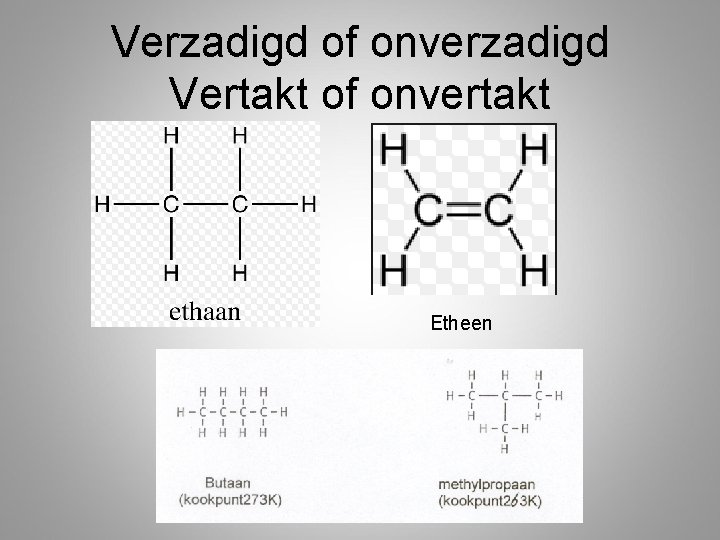
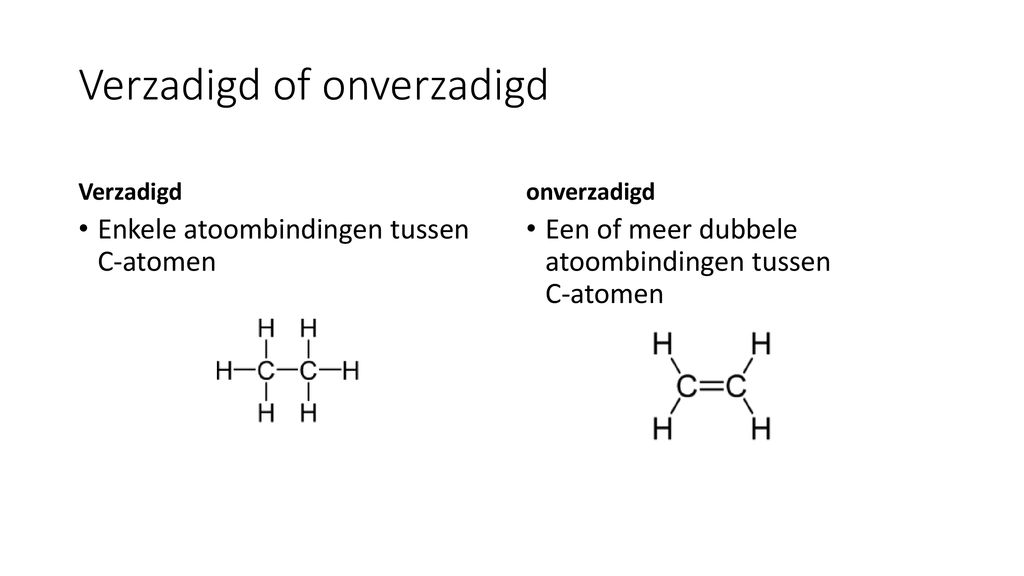
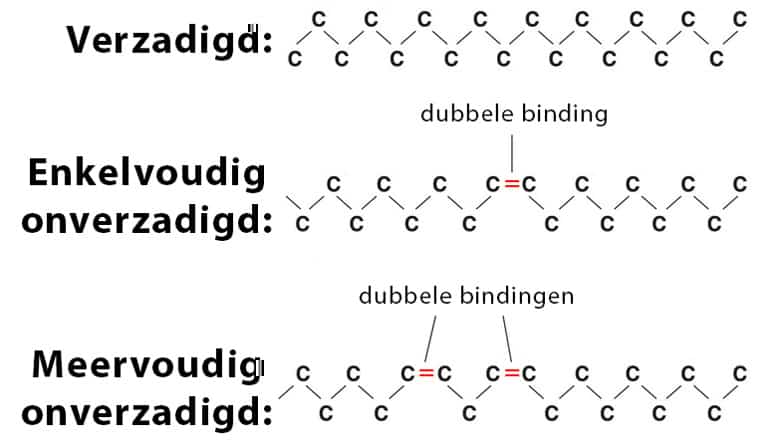
Stel je nu een simpele ketting voor, volledig gevuld met waterstofatomen. Elk koolstofatoom heeft het maximale aantal waterstofatomen waaraan het kan binden. Dát, lieve studenten, is de essentie van een verzadigd vetzuur. Het is 'verzadigd' met waterstof. De structuur is recht en compact.
De wending: Dubbele bindingen
Nu komt de magie! Wat gebeurt er als twee koolstofatomen een dubbele binding met elkaar aangaan? Plotseling kunnen ze niet meer het maximale aantal waterstofatomen vasthouden. Ze zijn onverzadigd geworden.
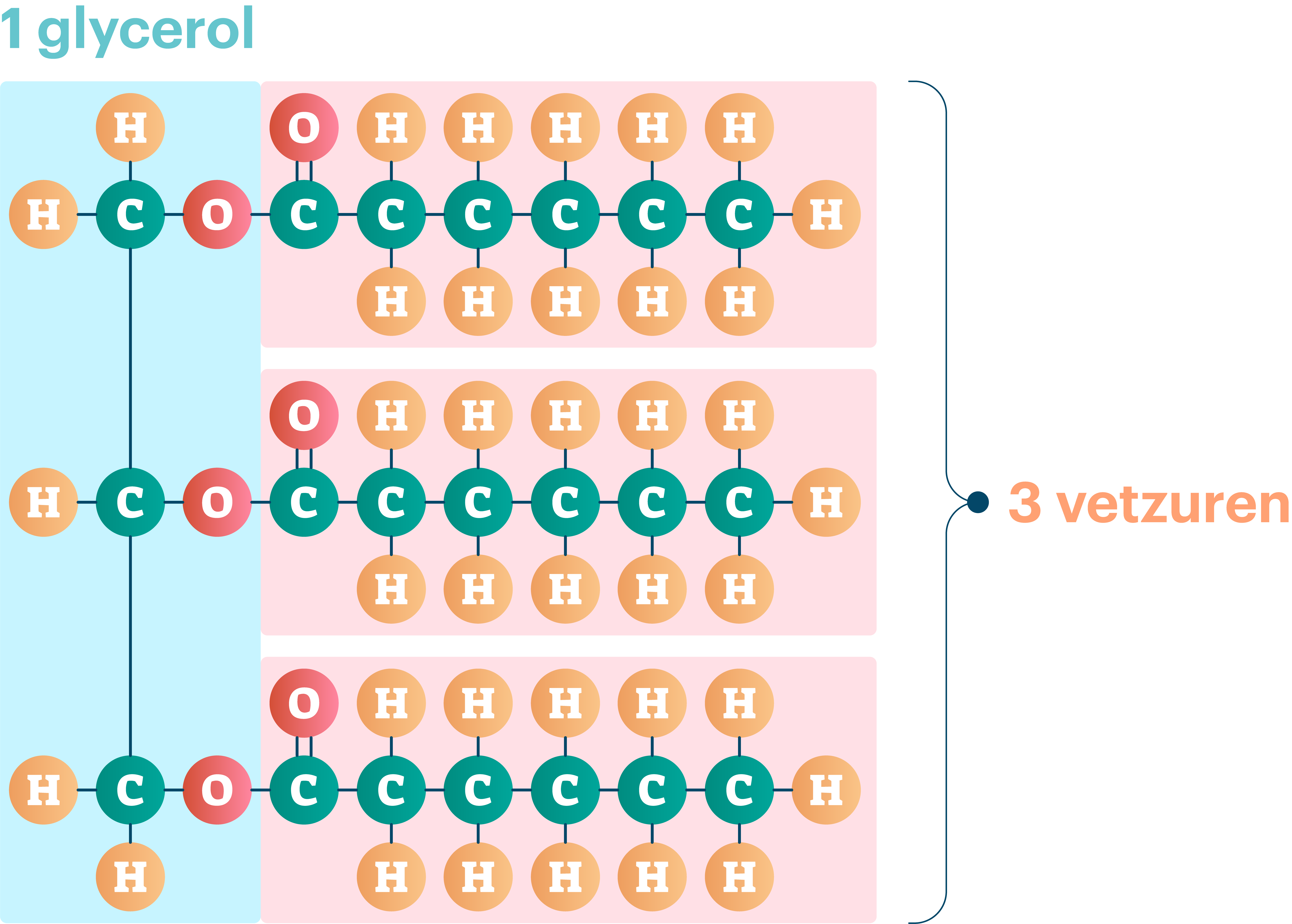
Die dubbele binding heeft grote gevolgen voor de vorm van de vetzuurketen. De keten buigt af op de plek van de dubbele binding, waardoor er een knik ontstaat. Hoe meer dubbele bindingen, hoe meer knikken. En die knikken hebben invloed op hoe de vetzuren zich tot elkaar verhouden.
De Gevolgen van de Vorm
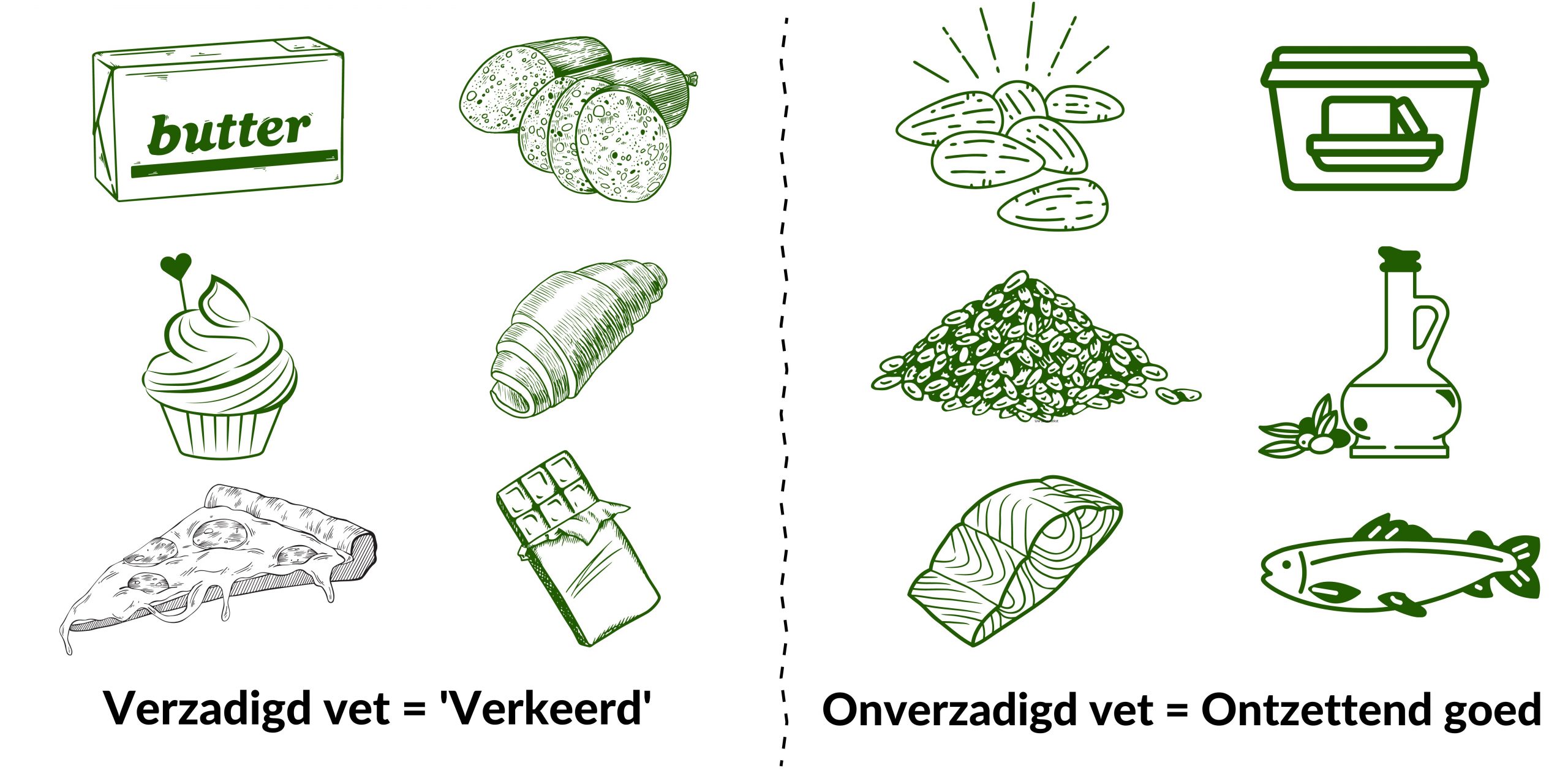
Verzadigde vetten, met hun rechte ketens, kunnen zich makkelijk dicht op elkaar pakken. Denk aan boter, die bij kamertemperatuur vast is. Onverzadigde vetten, met hun knikken, kunnen dat minder goed. Ze blijven 'vloeibaarder', zoals olijfolie. De interacties tussen moleculen worden beïnvloed door de vorm, wat resulteert in verschillen in smelttemperatuur en andere fysische eigenschappen.
Denk erover na: een simpele dubbele binding kan de hele structuur en eigenschappen van een molecuul veranderen! Dit is de kracht van de chemie: kleine veranderingen kunnen grote effecten hebben.
Meer dan alleen Chemie
Maar wat kunnen we leren van dit alles? Het gaat verder dan het onthouden van het verschil tussen verzadigd en onverzadigd vet. Het gaat om het ontwikkelen van een nieuwsgierige geest. Om vragen te durven stellen. Om de diepere verbanden te zien tussen structuur en functie.

De humiliteit om te erkennen dat we nog lang niet alles weten, maar ook de perseverantie om te blijven zoeken. En de vreugde om nieuwe kennis te ontdekken!
Elk experiment, elke formule, elke les is een stap op een levenslange reis van leren en ontdekken. Omarm de complexiteit, verwonder je over de details, en blijf altijd nieuwsgierig. Wie weet welke verborgen geheimen de chemie nog voor je in petto heeft! Laat de namen van grote geesten zoals Linus Pauling of Dorothy Hodgkin, pioniers op het gebied van structuurbepaling, je inspireren om door te zetten.



.png?format=1000w)