Symbool H En Atoomnummer 1

Voel je je soms ook overweldigd door al die scheikundige symbolen en getallen? Ben je een ouder die probeert je kind te helpen met huiswerk, een leerling die worstelt om de basis te begrijpen, of misschien wel een docent die op zoek is naar nieuwe manieren om de materie uit te leggen? Je bent zeker niet de enige! Chemie kan in het begin intimiderend lijken, maar geloof me, de basisprincipes zijn verrassend logisch en leuk als je ze eenmaal doorhebt. Laten we daarom samen een duik nemen in de wereld van waterstof, gesymboliseerd door H en met atoomnummer 1. We maken het helder, stap voor stap.
Wat is een chemisch element?
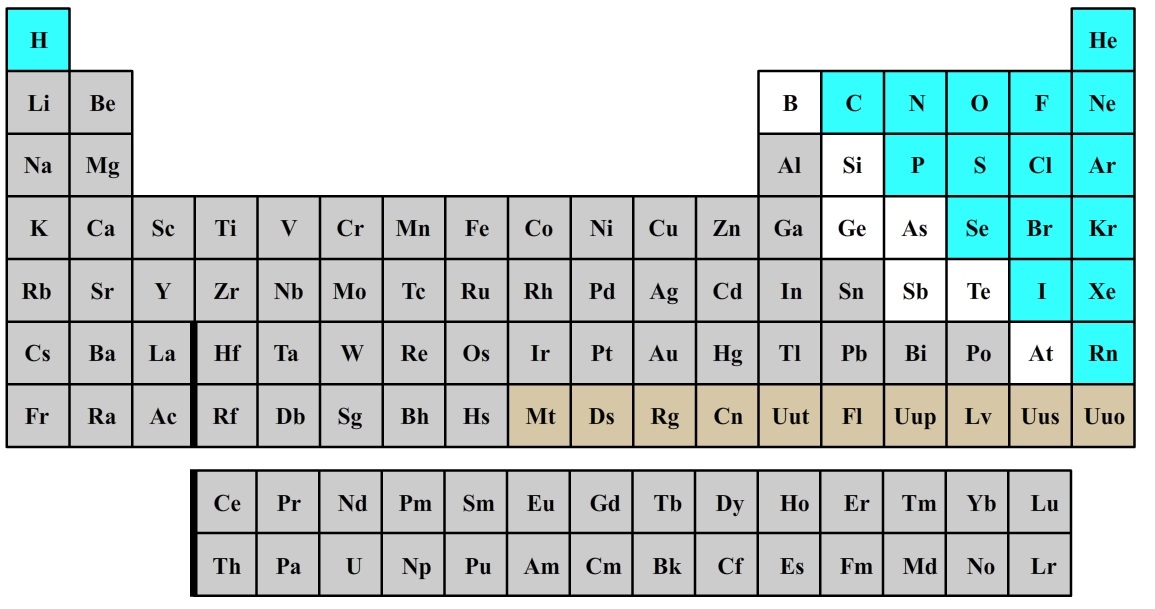
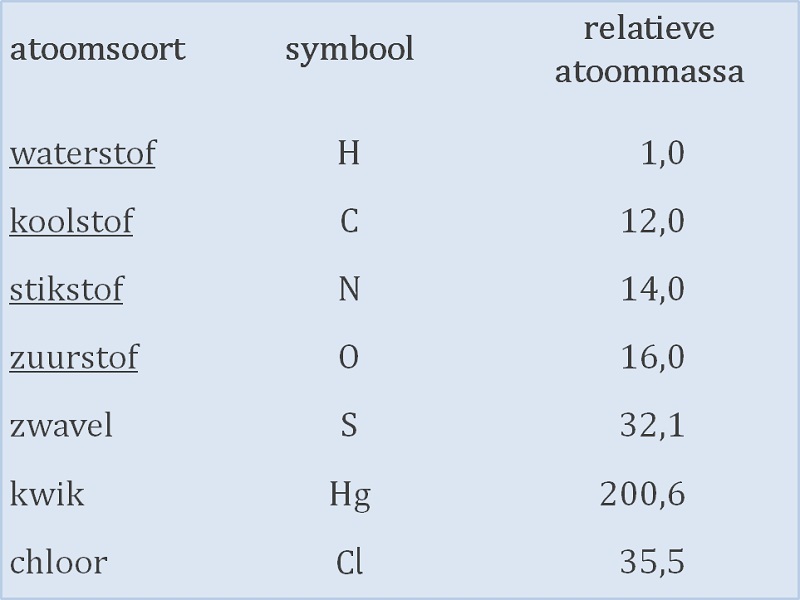
Laten we beginnen bij het begin. Een chemisch element is een stof die niet verder kan worden opgedeeld in eenvoudigere stoffen door chemische middelen. Denk aan goud (Au), zilver (Ag), of zuurstof (O). Elk element heeft een uniek symbool en een uniek atoomnummer. Deze informatie vind je terug in het periodiek systeem der elementen, een soort landkaart van alle bekende elementen.
Het periodiek systeem is niet zomaar een willekeurige lijst. De elementen zijn geordend op basis van hun atoomnummer en hun chemische eigenschappen. Elementen met vergelijkbare eigenschappen staan in dezelfde kolom (groep) van het periodiek systeem. Dit maakt het periodiek systeem een ongelooflijk handig hulpmiddel om voorspellingen te doen over hoe elementen zich gedragen.
Must Read
Waterstof (H): Het Lichtste en Meest Voorkomende Element
Nu specifiek over waterstof. Waterstof is het eerste element in het periodiek systeem. Dat betekent dat het het kleinste atoomnummer heeft: 1. Het chemische symbool voor waterstof is H.
Waarom is waterstof zo bijzonder? Ten eerste, het is het meest voorkomende element in het universum. Sterren zoals onze zon bestaan voornamelijk uit waterstof. Ten tweede is het lichtste element, wat het unieke eigenschappen geeft.
Waarom de 'H'? De 'H' komt van de Latijnse naam voor waterstof, Hydrogenium. Dus, H staat voor Hydrogenium en 1 staat voor het atoomnummer.
Atoomnummer 1: Wat betekent dat?
Het atoomnummer van een element geeft aan hoeveel protonen er in de kern van een atoom van dat element zitten. In het geval van waterstof betekent atoomnummer 1 dus dat een waterstofatoom één proton in de kern heeft.
Protonen zijn positief geladen deeltjes in de atoomkern. De kern bevat ook neutronen (neutraal geladen deeltjes), maar het aantal neutronen kan variëren (wat leidt tot isotopen, waar we later op terugkomen). Rondom de kern cirkelen elektronen, die negatief geladen zijn. Een neutraal atoom heeft evenveel protonen als elektronen.
Dus, een neutraal waterstofatoom heeft:
- 1 proton (in de kern)
- Meestal geen neutronen (de meest voorkomende isotoop heeft geen neutronen, maar er zijn isotopen met neutronen)
- 1 elektron (dat rond de kern cirkelt)
Belangrijk om te onthouden: Het aantal protonen bepaalt welk element het is. Als een atoom één proton heeft, is het waterstof. Als het twee protonen heeft, is het helium, enzovoort.
Waterstof in het dagelijks leven
Je vraagt je misschien af: waar kom ik waterstof tegen in het dagelijks leven? Overal!

- Water (H2O): Waterstof is een essentieel onderdeel van water. Elke watermolecuul bestaat uit twee waterstofatomen en één zuurstofatoom.
- Organische stoffen: Waterstof komt voor in vrijwel alle organische stoffen, zoals koolhydraten, vetten en eiwitten. Deze stoffen vormen de basis van al het leven op aarde.
- Brandstoffen: Waterstof wordt steeds meer gebruikt als brandstof, bijvoorbeeld in brandstofcellen. Een brandstofcel zet waterstof om in elektriciteit, met als enige bijproduct water.
- Ammoniak (NH3): Waterstof is cruciaal voor de productie van ammoniak, een belangrijke grondstof voor kunstmest.
Een voorbeeld voor in de klas of thuis: Laat leerlingen een lijst maken van alle dingen in hun omgeving waarvan ze denken dat er waterstof in zit. Bespreek vervolgens de antwoorden en leg uit waar waterstof precies voorkomt.
Isotopen van Waterstof
We hebben het al even aangestipt, maar het is belangrijk om te begrijpen dat waterstof isotopen heeft. Isotopen zijn atomen van hetzelfde element (dus met hetzelfde aantal protonen) die een verschillend aantal neutronen in hun kern hebben.
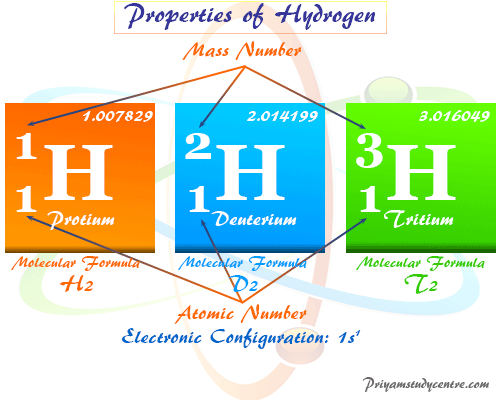
Waterstof heeft drie bekende isotopen:
- Protium (1H): De meest voorkomende isotoop, met 1 proton en geen neutronen.
- Deuterium (2H of D): Bevat 1 proton en 1 neutron. Wordt ook wel zware waterstof genoemd.
- Tritium (3H of T): Bevat 1 proton en 2 neutronen. Tritium is radioactief.
Hoewel isotopen van hetzelfde element verschillende massa's hebben, gedragen ze zich chemisch bijna identiek. Het verschil in massa kan echter wel invloed hebben op de reactiesnelheid.
Een leuk experiment (onder begeleiding): Laat leerlingen een model maken van de drie isotopen van waterstof. Gebruik bijvoorbeeld gekleurde knikkers om protonen, neutronen en elektronen voor te stellen. Dit helpt hen om het verschil tussen de isotopen visueel te begrijpen.
Waarom is dit belangrijk om te leren?
Het begrijpen van elementen zoals waterstof, hun symbolen en atoomnummers is cruciaal voor het begrijpen van de chemie in het algemeen. Het is de basis waarop je verder bouwt. Zonder deze basiskennis is het moeilijk om complexere concepten zoals chemische reacties, moleculen en verbindingen te begrijpen.
Bovendien is chemie overal om ons heen. Het begrijpen van de basisprincipes kan je helpen om de wereld om je heen beter te begrijpen. Van het koken van een ei tot de werking van medicijnen, chemie speelt een rol.
Statistieken laten zien dat leerlingen die een sterke basis in scheikunde hebben, beter presteren in vervolgopleidingen in de wetenschap, technologie, engineering en wiskunde (STEM). Een goed begrip van waterstof en het periodiek systeem is dus een belangrijke stap op weg naar succes in deze vakgebieden.

Tips voor het leren en onthouden
Het leren van scheikunde kan soms lastig zijn, maar er zijn manieren om het makkelijker en leuker te maken:
- Maak gebruik van ezelsbruggetjes: Bedenk bijvoorbeeld een grappig zinnetje om de symbolen en atoomnummers te onthouden.
- Gebruik visuele hulpmiddelen: Bekijk video's, afbeeldingen en animaties om de concepten visueel te begrijpen.
- Oefen regelmatig: Maak oefenopgaven en tests om je kennis te testen en te versterken.
- Werk samen met anderen: Bespreek de stof met medeleerlingen of studiegroepen.
- Zoek hulp als je vastloopt: Vraag je docent, ouders of een tutor om hulp.
- Wees niet bang om fouten te maken: Fouten maken is een natuurlijk onderdeel van het leerproces. Leer van je fouten en probeer het opnieuw.
Een praktische tip: Download een interactief periodiek systeem app op je telefoon of tablet. Deze apps bevatten vaak extra informatie en leuke quizzen om je kennis te testen.
Conclusie
We hebben nu de basisprincipes van waterstof (H) met atoomnummer 1 behandeld. Hopelijk voel je je nu wat zekerder over dit onderwerp. Onthoud: chemie hoeft niet eng te zijn. Met een beetje inspanning en de juiste hulpmiddelen kan iedereen het leren. Blijf vragen stellen, blijf ontdekken en blijf nieuwsgierig!
Dus de volgende keer dat je een watermolecuul ziet, denk dan aan de twee kleine waterstofatomen (H) met elk slechts één proton (atoomnummer 1) die samenwerken met zuurstof om het leven op aarde mogelijk te maken. Het is fascinerend, toch?