Reactiewarmte Berekenen Met Vormingswarmte Scheikunde

Hé, scheikunde student! Zit je te worstelen met het berekenen van reactiewarmtes met behulp van vormingswarmtes? Je bent zeker niet de enige! Het kan een lastig onderwerp zijn, maar geloof me, met een beetje uitleg en oefening krijg je het onder de knie. Laten we samen kijken hoe we dit kunnen aanpakken.
Wat is Reactiewarmte eigenlijk?
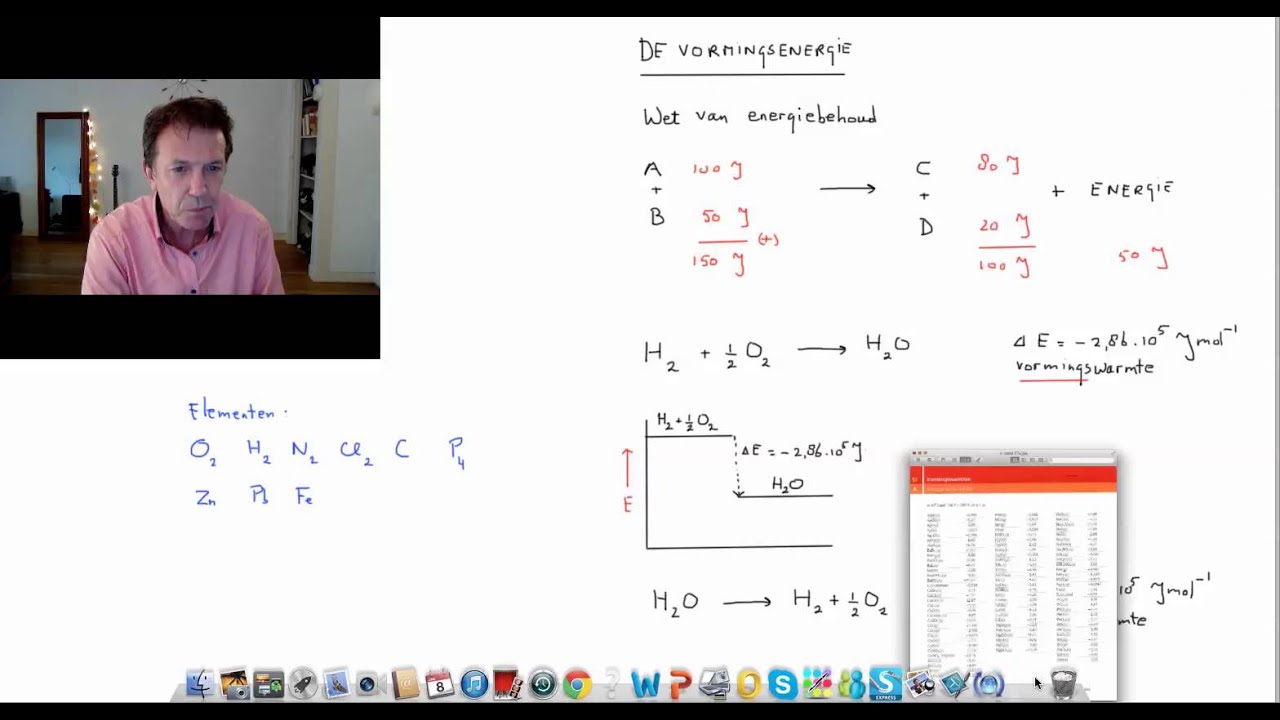
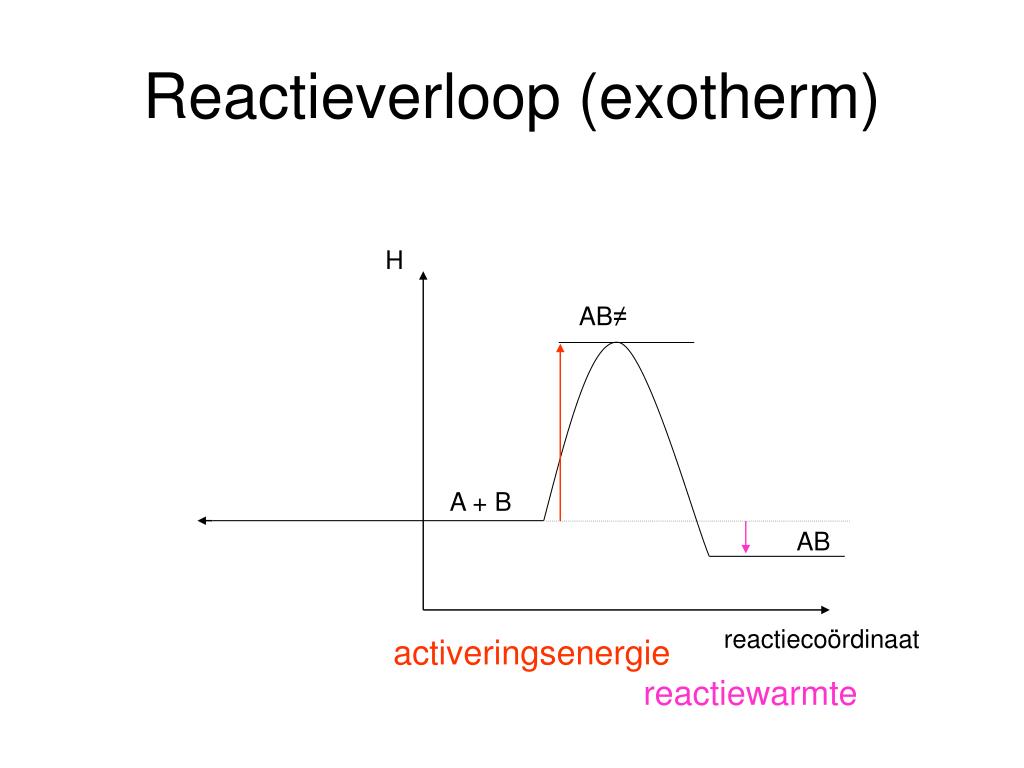
De reactiewarmte is de warmte die vrijkomt of opgenomen wordt tijdens een chemische reactie. Of een reactie warmte afgeeft (exotherm) of warmte nodig heeft (endotherm) is belangrijk om te weten. We kunnen dit berekenen!
Vormingswarmte: De Bouwstenen
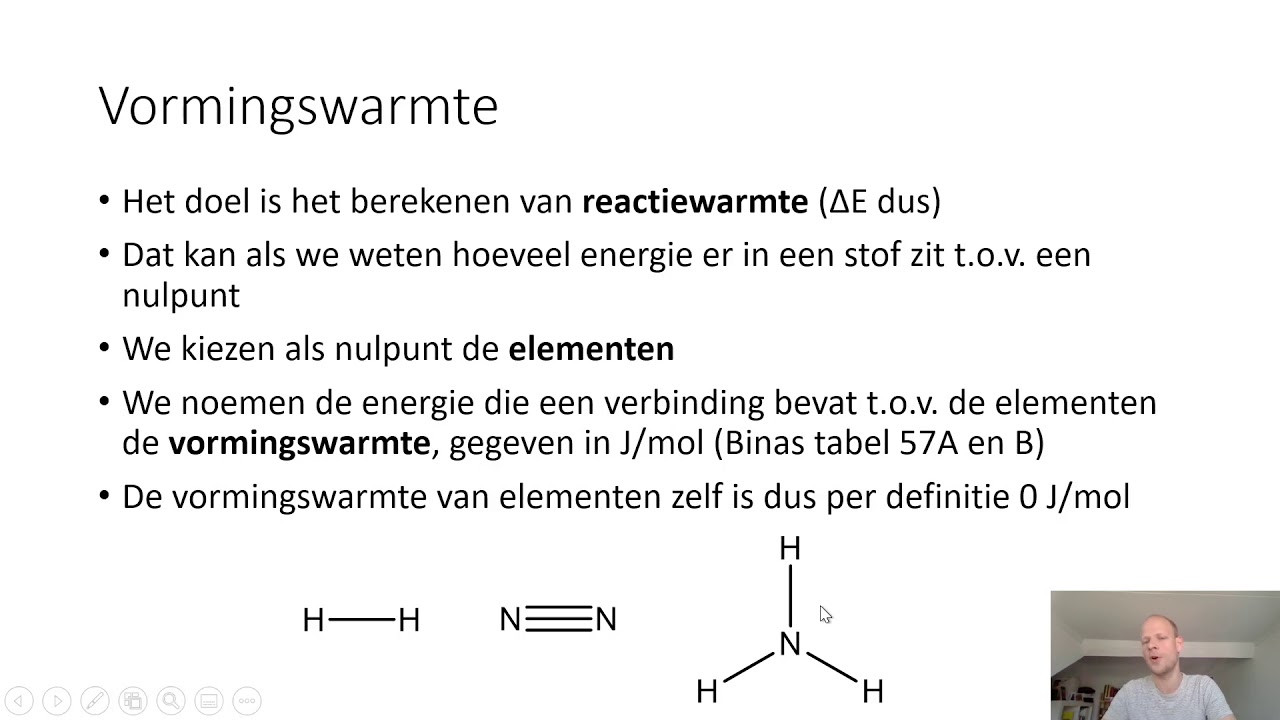
Voordat we reactiewarmte kunnen berekenen, moeten we eerst de vormingswarmte begrijpen. De vormingswarmte is de warmte die vrijkomt of nodig is bij de vorming van één mol van een stof uit zijn elementen in hun standaardtoestand. De standaardtoestand is de meest stabiele vorm van een element bij 298 K (25°C) en 1 atm druk. Een paar voorbeelden zijn:
Must Read
- Zuurstof (O2)
- Koolstof (C, grafiet)
- Waterstof (H2)
Belangrijk: de vormingswarmte van een element in zijn standaardtoestand is 0! Deze waarde vind je vaak in tabellen in je scheikundeboek of online.
De Formule voor Reactiewarmte
Nu komt het belangrijkste: de formule om de reactiewarmte (ΔHreactie) te berekenen met behulp van vormingswarmtes (ΔHf):

ΔHreactie = Σ ΔHf(producten) - Σ ΔHf(reactanten)
Wat betekent dit? Het is eigenlijk best simpel:
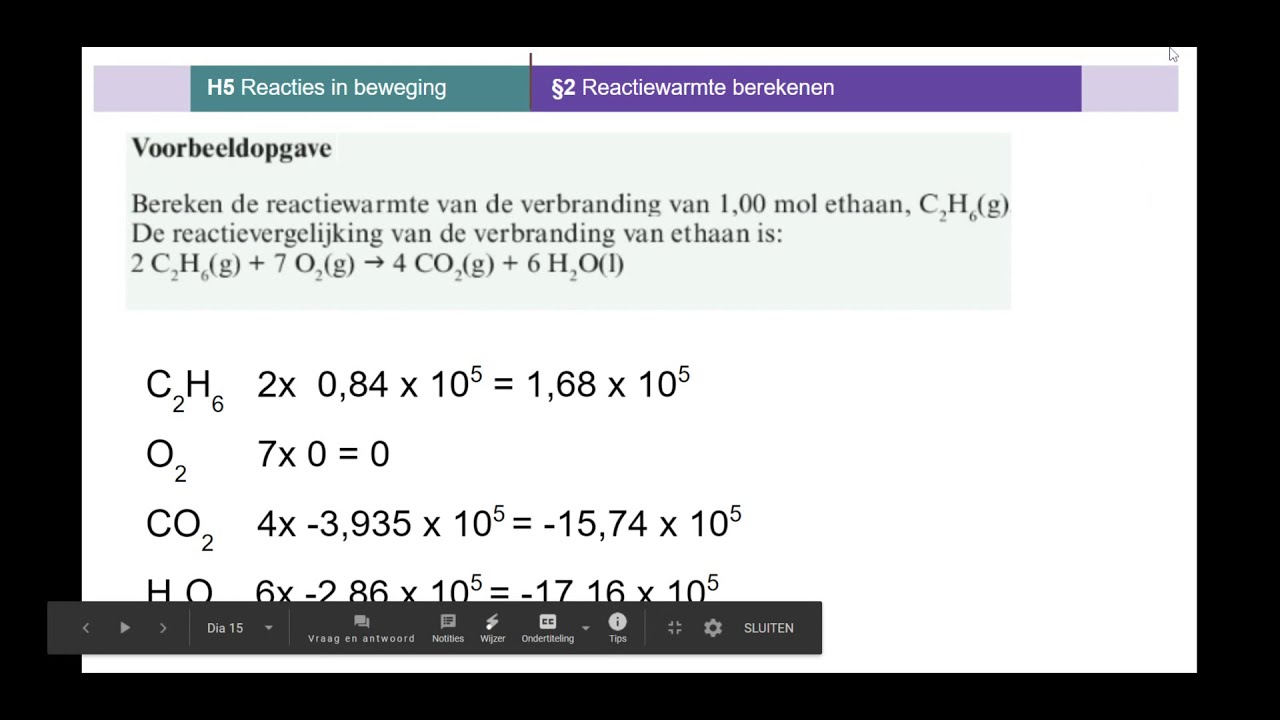
- Σ ΔHf(producten): Tel alle vormingswarmtes van de producten (rechterkant van de reactievergelijking) bij elkaar op. Denk eraan dat je de vormingswarmte van elk product moet vermenigvuldigen met zijn coëfficiënt (het getal voor de chemische formule) in de reactievergelijking.
- Σ ΔHf(reactanten): Tel alle vormingswarmtes van de reactanten (linkerkant van de reactievergelijking) bij elkaar op. Ook hier vermenigvuldig je de vormingswarmte van elke reactant met zijn coëfficiënt.
- Trek de som van de vormingswarmtes van de reactanten af van de som van de vormingswarmtes van de producten.
Voorbeeld: De Verbranding van Methaan (CH4)
Laten we dit toepassen op een concreet voorbeeld: de verbranding van methaan (CH4).
De reactievergelijking is:

CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Stel, de vormingswarmtes zijn:
- ΔHf(CH4(g)) = -74.8 kJ/mol
- ΔHf(O2(g)) = 0 kJ/mol (want O2 is een element in zijn standaardtoestand)
- ΔHf(CO2(g)) = -393.5 kJ/mol
- ΔHf(H2O(l)) = -285.8 kJ/mol
Nu vullen we de formule in:

ΔHreactie = [1 * (-393.5 kJ/mol) + 2 * (-285.8 kJ/mol)] - [1 * (-74.8 kJ/mol) + 2 * (0 kJ/mol)]
ΔHreactie = [-393.5 - 571.6] - [-74.8 + 0]
ΔHreactie = -965.1 + 74.8

ΔHreactie = -890.3 kJ/mol
De reactiewarmte voor de verbranding van methaan is -890.3 kJ/mol. Dit betekent dat de reactie exotherm is, er komt warmte vrij!
Tips voor Succes
- Zorg dat je reactievergelijking klopt. Een verkeerde reactievergelijking leidt tot een verkeerde uitkomst.
- Let op de aggregatietoestand. De vormingswarmte van H2O(l) is anders dan H2O(g).
- Gebruik de juiste eenheden. Vormingswarmtes worden meestal gegeven in kJ/mol.
- Oefen, oefen, oefen! Hoe meer je oefent, hoe beter je het zult begrijpen.
Reactiewarmte berekenen met vormingswarmtes kan in het begin lastig lijken, maar met de juiste aanpak is het echt te leren. Onthoud de formule, wees nauwkeurig met je gegevens en oefen veel. Succes!





+-+Σ+U+stoffen(voor+reactie).jpg)