Met Welk Apparaat Kan Een Stof Zoals Water Geëlektrolyseerd Worden
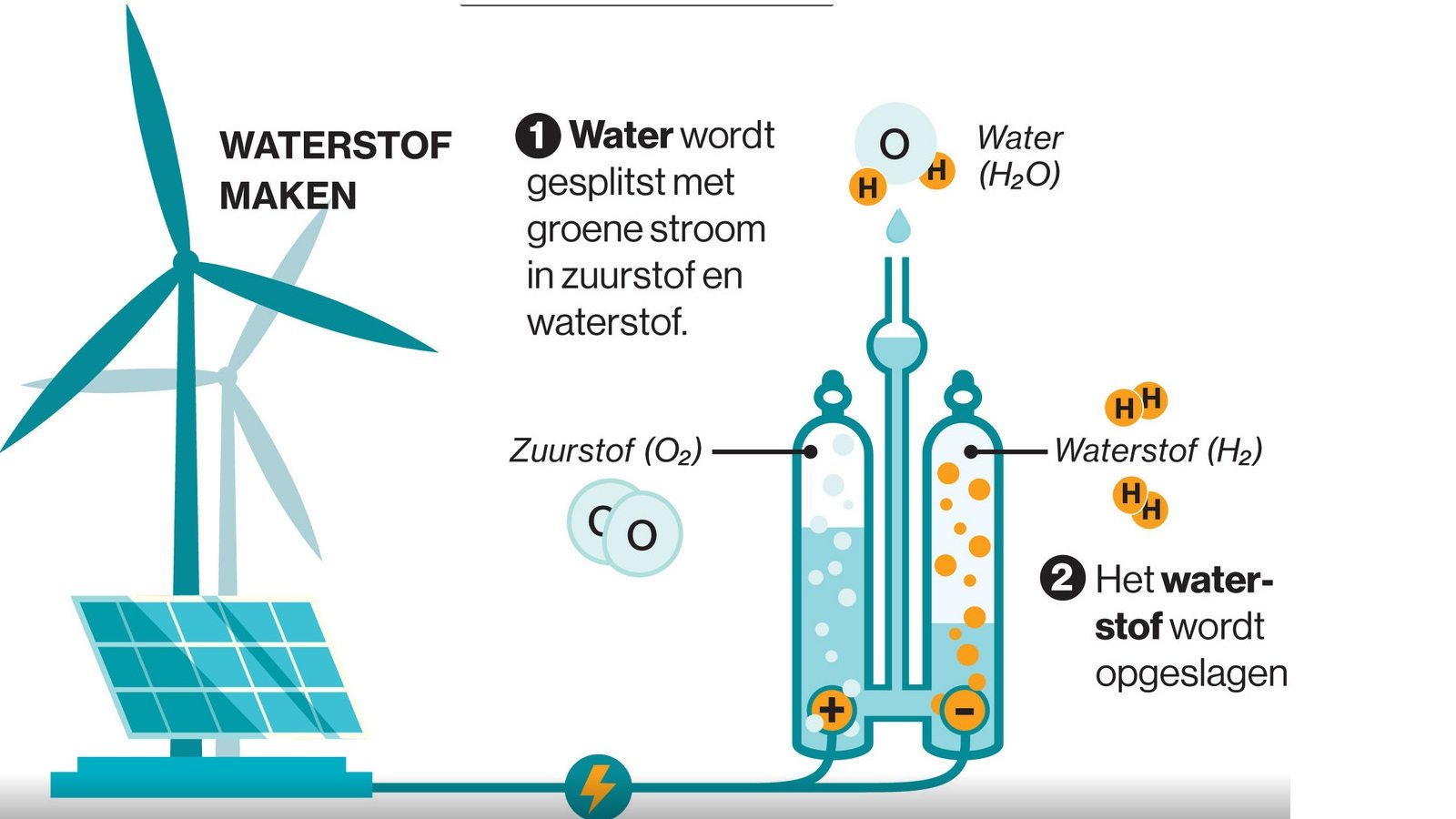
Heeft u zich ooit afgevraagd hoe we water, een stof die zo alledaags is, kunnen opsplitsen in zijn basiselementen: waterstof en zuurstof? Het proces, elektrolyse, is fascinerend en heeft een enorme potentie voor de toekomst van energie. Maar welk apparaat is eigenlijk nodig om dit te bewerkstelligen? Laten we deze vraag eens dieper onderzoeken.
Wat is Elektrolyse?
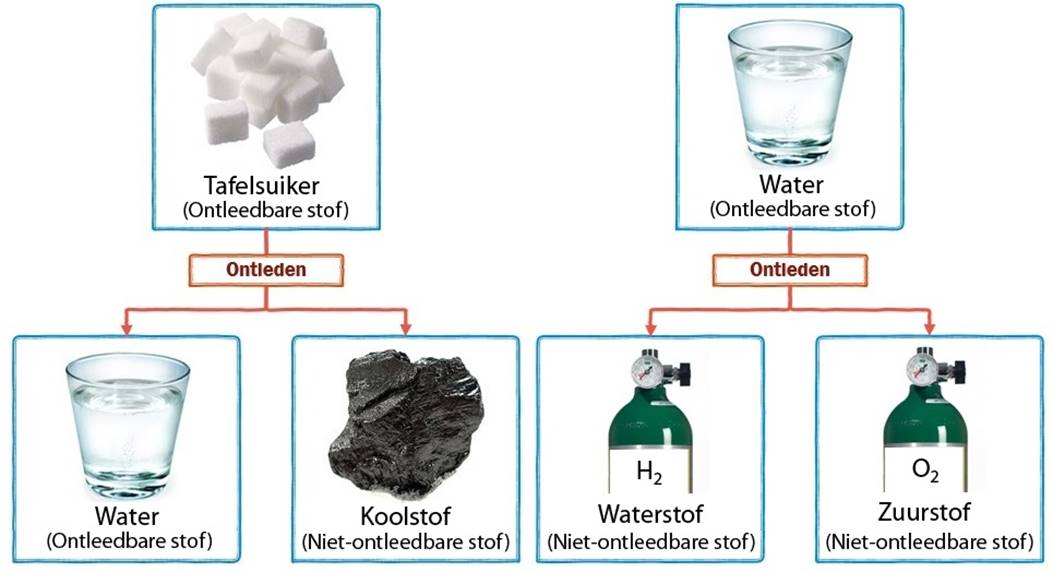
Voordat we naar de specifieke apparatuur kijken, is het belangrijk om het principe van elektrolyse te begrijpen. Elektrolyse is het proces waarbij een elektrische stroom wordt gebruikt om een chemische reactie te veroorzaken die anders niet spontaan zou plaatsvinden. In het geval van water resulteert dit in de ontleding van water (H2O) in waterstof (H2) en zuurstof (O2).
Denk aan een batterij die een lampje laat branden. De batterij levert elektrische energie die een chemische reactie aandrijft. Elektrolyse is eigenlijk het omgekeerde: we gebruiken elektrische energie om een chemische reactie te laten plaatsvinden.
Must Read
De Elektrolyse-cel: Het Centrale Apparaat
Het apparaat dat gebruikt wordt voor elektrolyse, in het bijzonder voor de elektrolyse van water, wordt een elektrolyse-cel genoemd. Dit is geen ingewikkeld, futuristisch apparaat; de basisprincipes zijn relatief eenvoudig, maar de optimalisatie en efficiëntie ervan vereisen geavanceerde technologie.
De Basiscomponenten van een Elektrolyse-cel
Een typische elektrolyse-cel bestaat uit de volgende componenten:
- Elektrolyt: Dit is een stof die ionen bevat en elektriciteit geleidt. Bij water is het belangrijk dat er een elektrolyt aanwezig is omdat puur water een slechte geleider is. Meestal wordt er een kleine hoeveelheid zuur (zoals zwavelzuur) of een base (zoals natriumhydroxide) toegevoegd. Soms wordt een vast polymere elektrolyt gebruikt, zoals in PEM elektrolysers.
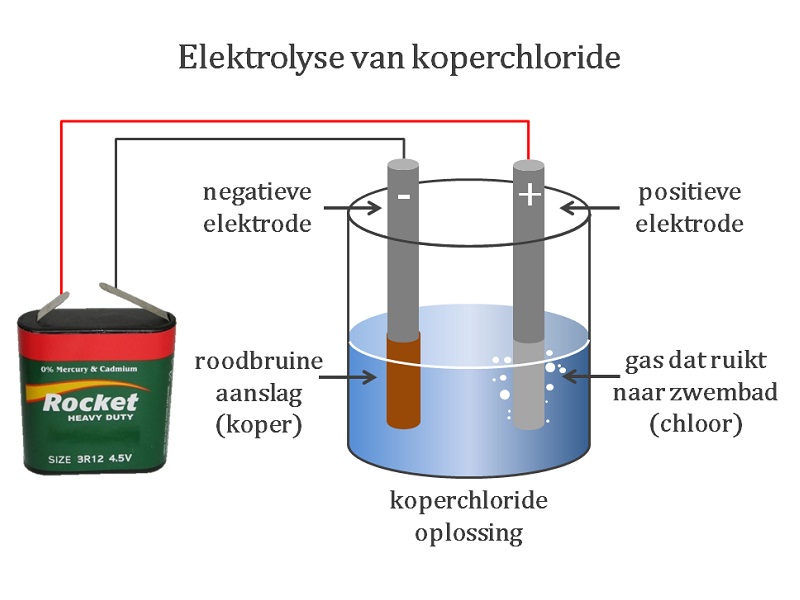
- Anode: Dit is de positief geladen elektrode waar oxidatie plaatsvindt. Bij de elektrolyse van water worden watermoleculen geoxideerd, waardoor zuurstofgas en positieve ionen (protonen of hydroxide-ionen, afhankelijk van de elektrolyt) ontstaan.
- Kathode: Dit is de negatief geladen elektrode waar reductie plaatsvindt. Hier worden de positieve ionen (protonen of hydroxide-ionen) gereduceerd, waardoor waterstofgas ontstaat.
- Elektrodenmateriaal: De elektroden zijn gemaakt van een geleidend materiaal dat bestand is tegen corrosie. Platina was vroeger de standaard, maar tegenwoordig worden er ook andere materialen gebruikt, zoals nikkel, roestvrij staal en verschillende oxiden, afhankelijk van de specifieke toepassing en de kosten.
- Membraan (optioneel): In sommige elektrolyse-cellen, zoals PEM elektrolysers, wordt een membraan gebruikt om te voorkomen dat de waterstof en zuurstof gassen zich vermengen. Dit is cruciaal voor de veiligheid en de zuiverheid van de geproduceerde gassen.
Verschillende Types Elektrolyse-cellen
Er zijn verschillende types elektrolyse-cellen die elk hun eigen voor- en nadelen hebben. De meest voorkomende types zijn:
- Alkalische Elektrolyse: Dit is de meest volwassen en wijdverspreide technologie. Het maakt gebruik van een alkalische elektrolyt, zoals kaliumhydroxide (KOH), en is relatief goedkoop. Het nadeel is dat het minder efficiënt is dan andere types en minder goed reageert op fluctuerende energiebronnen, zoals zonne-energie.
- PEM Elektrolyse (Proton Exchange Membrane): Deze technologie gebruikt een vast polymere elektrolyt membraan dat alleen protonen doorlaat. PEM elektrolysers zijn efficiënter dan alkalische elektrolysers en kunnen beter omgaan met fluctuerende energiebronnen. Ze zijn echter duurder vanwege de noodzaak voor edelmetaal katalysatoren.
- Solid Oxide Elektrolyse (SOEC): Deze technologie werkt bij hoge temperaturen (500-850 °C) en kan zeer efficiënt zijn. SOEC elektrolysers kunnen niet alleen water, maar ook stoom elektrolyseren, wat de efficiëntie verder verhoogt. Ze zijn echter complexer en vereisen materialen die bestand zijn tegen hoge temperaturen.
- Anion Exchange Membrane (AEM) Elektrolyse: Dit is een relatief nieuwe technologie die de voordelen van alkalische en PEM elektrolyse probeert te combineren. AEM elektrolysers gebruiken een anion exchange membraan dat hydroxide-ionen doorlaat. Ze zijn potentieel goedkoper dan PEM elektrolysers en efficiënter dan alkalische elektrolysers.
Hoe Werkt het in de Praktijk?
Stel je voor dat je een simpel experiment wilt uitvoeren om de elektrolyse van water te demonstreren. Je zou het volgende nodig hebben:
- Twee elektroden (bijvoorbeeld koolstofstaven).
- Een bekerglas gevuld met water en een kleine hoeveelheid natriumcarbonaat (soda, om de geleidbaarheid te verhogen).
- Een batterij (bijvoorbeeld een 9V batterij).
- Twee reageerbuizen om de geproduceerde gassen op te vangen.
- Twee krokodillenklemmen met draden om de elektroden met de batterij te verbinden.
Dompel de elektroden in het water en verbind ze met de batterij. Je zult bubbels zien ontstaan bij beide elektroden. De reageerbuis die boven de anode is geplaatst, zal zuurstofgas opvangen, en de reageerbuis boven de kathode zal waterstofgas opvangen. Let op: er zal tweemaal zoveel waterstofgas worden geproduceerd als zuurstofgas (dit komt overeen met de chemische formule van water: H2O).
De Impact van Elektrolyse op de Wereld
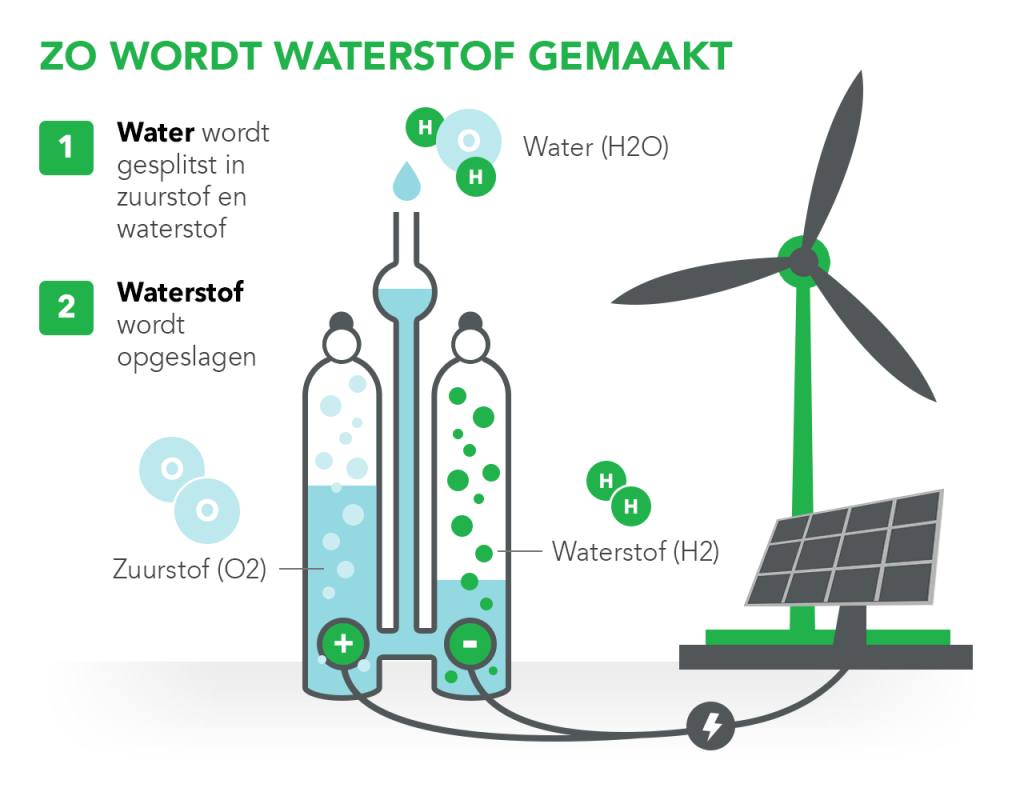
De elektrolyse van water is niet alleen een interessant wetenschappelijk experiment; het heeft een enorme impact op onze samenleving en de toekomst van energie. Een van de belangrijkste toepassingen is de productie van groene waterstof. Groene waterstof wordt geproduceerd met behulp van elektrolyse aangedreven door hernieuwbare energiebronnen, zoals zonne- en windenergie.
Waterstof kan worden gebruikt als brandstof voor auto's, bussen en vrachtwagens, als grondstof voor de chemische industrie, en als energieopslagmedium. Door waterstof te produceren met behulp van elektrolyse, kunnen we de afhankelijkheid van fossiele brandstoffen verminderen en de uitstoot van broeikasgassen terugdringen.
Tegenargumenten en Uitdagingen
Hoewel elektrolyse veel potentie heeft, zijn er ook uitdagingen en tegenargumenten. Een van de belangrijkste uitdagingen is de kosten. Elektrolyse is momenteel nog duurder dan de productie van waterstof uit aardgas (stoomreforming). Daarnaast is er veel energie nodig om water te elektrolyseren. Het is dus cruciaal dat de elektriciteit afkomstig is van hernieuwbare bronnen om de CO2-voetafdruk te minimaliseren.
Sommige critici beweren dat waterstof inefficiënt is als energieopslagmedium, omdat er energie verloren gaat bij de conversie van elektriciteit naar waterstof en weer terug. Anderen wijzen op de veiligheidsrisico's die verbonden zijn aan de opslag en het transport van waterstofgas.
Ondanks deze uitdagingen wordt er volop geïnvesteerd in onderzoek en ontwikkeling om de kosten van elektrolyse te verlagen, de efficiëntie te verhogen en de veiligheid te waarborgen. Met de toenemende druk om de klimaatverandering aan te pakken, zal de rol van elektrolyse in de energievoorziening van de toekomst alleen maar groter worden.
Oplossingen en Toekomstperspectieven
Om de potentie van elektrolyse volledig te benutten, zijn er verschillende oplossingen nodig:
- Verlaging van de kosten: Dit kan worden bereikt door de ontwikkeling van goedkopere materialen voor de elektroden en membranen, en door de schaalvoordelen van grootschalige productie.
- Verhoging van de efficiëntie: Dit kan worden bereikt door het optimaliseren van het ontwerp van de elektrolyse-cellen en door het gebruik van geavanceerde katalysatoren.
- Integratie met hernieuwbare energiebronnen: Dit is cruciaal om groene waterstof te produceren. Elektrolyse-installaties moeten worden gekoppeld aan zonne- en windparken om optimaal gebruik te maken van de beschikbare hernieuwbare energie.
- Infrastructuur voor waterstof: Er moet een infrastructuur worden aangelegd voor de opslag en het transport van waterstofgas, zodat het veilig en efficiënt kan worden gebruikt in verschillende toepassingen.
De toekomst van elektrolyse ziet er rooskleurig uit. Met de juiste investeringen en innovaties kan elektrolyse een cruciale rol spelen in de transitie naar een duurzame energievoorziening. Groene waterstof kan een belangrijke brandstof worden voor de transportsector, de industrie en de energiesector, en kan bijdragen aan een schonere en duurzamere wereld.
Kortom, het apparaat waarmee een stof zoals water geëlektrolyseerd kan worden is de elektrolyse-cel, in al zijn verschillende vormen en met alle daarbij horende nuances. Het is een cruciale technologie om een duurzame toekomst mogelijk te maken.
Nu u meer weet over de elektrolyse van water, wat zijn uw gedachten over de rol van waterstof in de toekomstige energievoorziening? Bent u optimistisch over de mogelijkheden, of ziet u nog te veel obstakels?