Lost Zout Op In Water

Hé, heb je je ooit afgevraagd waar het zout naartoe gaat als je het in een glas water roert? Het is net een goocheltruc, hè? Poef! Weg! Maar geen paniek, het is niet verdwenen in een andere dimensie. Het is gewoon… opgelost. En geloof me, dat oplossen van zout is veel interessanter dan het lijkt.
Laten we eerlijk zijn, scheikunde klinkt voor velen als een droge boterham. Maar wat als ik je vertel dat het oplossen van zout in water een mini-scheikundeles is die je elke dag ziet? Denk maar aan het koken van pasta. Je gooit een handje zout in het kokende water, en hop, het water smaakt meteen beter. Maar waar is dat zout gebleven?
Wat betekent "oplossen" eigenlijk?
Het woord "oplossen" klinkt misschien vanzelfsprekend, maar er gebeurt meer dan je denkt. Stel je voor: zout is als een stel super-sociale kleine blokjes (moleculen). Water is een groep hyperactieve mini-wervelwinden (watermoleculen).
Must Read
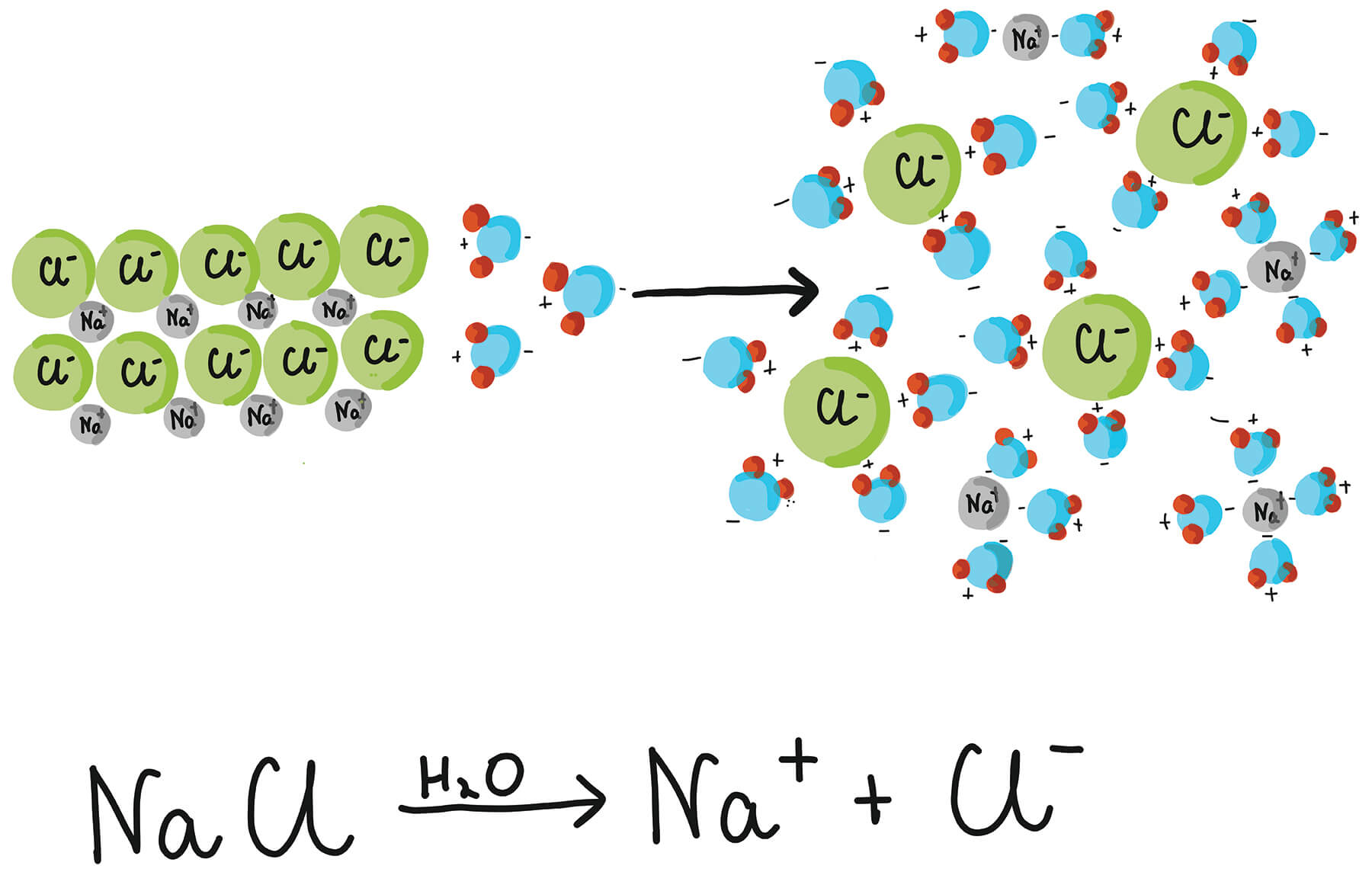
Wanneer je zout in water gooit, beginnen die wervelwinden (watermoleculen) de zoutblokjes te bombarderen. Ze trekken aan de zoutblokjes en trekken ze als het ware uit elkaar. Elk zoutblokje wordt nu omringd door een horde watermoleculen. Ze houden het zoutblokje vast en zorgen ervoor dat het niet meer terug kan keren naar zijn oorspronkelijke, solide vorm.
Het resultaat? Het zout is gelijkmatig verspreid door het water. Je kunt het zout niet meer zien, omdat de individuele zoutmoleculen nu tussen de watermoleculen zitten. Alsof ze een onzichtbare camouflage hebben gekregen!

Waarom is dit belangrijk?
Oké, oké, je denkt misschien: "Leuk verhaal, maar waarom zou ik me hier druk over maken?" Nou, er zijn heel veel redenen! Hier zijn er een paar, verpakt in kleine verhaaltjes:
- Koken is scheikunde in de praktijk: Denk aan soep. Zonder zout is soep vaak flauw. Het zout, opgelost in de bouillon, versterkt de smaak van alle andere ingrediënten. Het is de magie van de chef!
- Het leven in de oceaan: Wist je dat de oceaan zo zout is, doordat zout en mineralen uit rivieren continu oplossen in het water en naar zee stromen? Zonder opgelost zout, zou het leven in de oceaan er heel anders uitzien. Denk aan alle vissen en zeedieren die van dat zout afhankelijk zijn!
- Jouw lichaam heeft het nodig: Natrium, een belangrijk bestanddeel van zout, is essentieel voor je zenuwen en spieren. Het helpt je lichaam om vocht vast te houden en je bloeddruk op peil te houden. Natuurlijk, niet te veel zout, want dat is weer niet goed. Maar een beetje zout is noodzakelijk.
En denk eens aan het maken van limonade. Je roert suiker in het water, en het verdwijnt. Hetzelfde principe! Oplossen is een fundamenteel proces dat overal om ons heen gebeurt.

Wat beïnvloedt het oplossen?
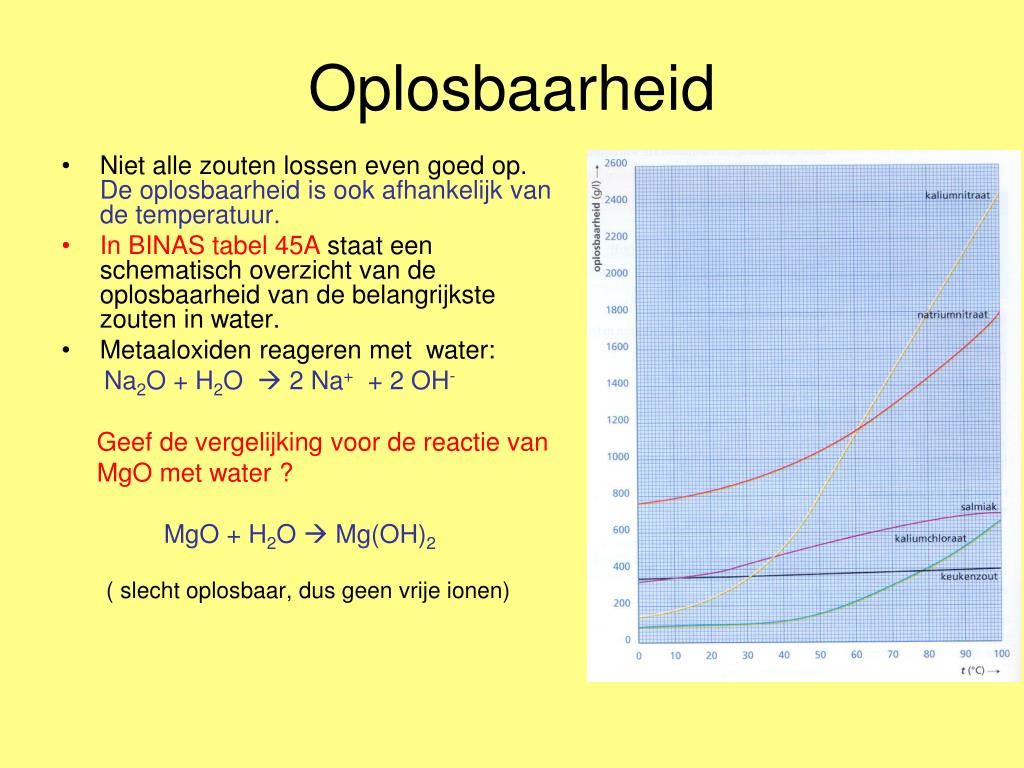
Niet elk zout lost even snel op in water. Er zijn een paar belangrijke factoren die een rol spelen:
- Temperatuur: Warm water is een turbo voor het oplossen. De watermoleculen bewegen sneller, waardoor ze de zoutblokjes agressiever aanvallen en sneller uit elkaar trekken. Denk aan ijskoffie met suiker. In koude koffie lost de suiker veel langzamer op dan in warme koffie.
- Roeren: Roeren is als het aanzetten van een feestje in het water. Het zorgt ervoor dat de watermoleculen de zoutblokjes continu blijven bombarderen.
- De grootte van de korrels: Fijn zout lost sneller op dan grof zout. Dat komt omdat fijn zout een groter oppervlak heeft dat in contact komt met het water. Stel je voor dat je een grote ijsklont in een glas water doet. Die smelt langzaam. Maar als je dezelfde ijsklont vermaalt tot kleine stukjes, smelt hij veel sneller!
Experimenteer zelf eens! Neem twee glazen water, één koud en één warm. Doe in beide glazen evenveel zout en roer. Je zult zien dat het zout in het warme water veel sneller oplost.
Meer dan alleen zout
Het oplossen van zout is slechts één voorbeeld van een veel groter fenomeen. Er zijn talloze stoffen die in water of andere vloeistoffen kunnen oplossen. Suiker, kleurstoffen, zelfs sommige gassen (zoals zuurstof, wat essentieel is voor vissen!) kunnen oplossen.
De mogelijkheden zijn eindeloos! Denk aan het maken van thee. De smaakstoffen uit de theeblaadjes lossen op in het hete water, waardoor je die heerlijke kop thee krijgt. Of denk aan de medicijnen die je slikt. De actieve ingrediënten moeten oplossen in je lichaam om hun werk te kunnen doen.

Oplossen is een essentiële chemische reactie die ons leven op ontelbaar veel manieren beïnvloedt. Van het koken van een simpele maaltijd tot het functioneren van ons eigen lichaam, het is er allemaal!
Dus, de volgende keer dat je zout in water roert, neem even een moment om stil te staan bij wat er echt gebeurt. Je bent getuige van een kleine chemische wonder, een fundamenteel proces dat de wereld om ons heen vormgeeft. En wie weet, misschien inspireert het je wel om meer te leren over de fascinerende wereld van de scheikunde!
En onthoud, de volgende keer dat je iemand ziet stuntelen met het oplossen van suiker in ijskoffie, kun je ze uitleggen waarom het zo lang duurt. Je bent nu een oplos-expert!