Hoeveel Bindingen Kan N Aangaan

Hoi! Laten we het eens hebben over stikstof (N). Ja, dat element dat zo'n 78% van de lucht die we inademen uitmaakt. Klinkt misschien saai, maar geloof me, stikstof is eigenlijk een best wel sociaal atoom. Het heeft namelijk een bepaalde 'binding-drang', en we gaan eens kijken hoeveel vrienden (lees: andere atomen) het tegelijkertijd aan de haak kan slaan. Denk aan een super enthousiaste gast op een feestje die iedereen wil begroeten en een high-five geven. Alleen heeft stikstof geen handen, maar elektronen.
Dus, hoeveel high-fives kan stikstof eigenlijk uitdelen? Laten we daar eens induiken! Het antwoord is: meestal drie. Maar zoals met alles in het leven, zijn er uitzonderingen op de regel. Denk aan je tante die altijd net even anders is dan de rest van de familie.
Waarom precies drie?
Om dit te begrijpen, moeten we heel even terug naar de scheikundeles. Geen zorgen, ik beloof je geen moeilijke formules. Stikstof heeft namelijk vijf valentie-elektronen. Dat zijn de elektronen in de buitenste schil van het atoom, en die zijn cruciaal voor het vormen van bindingen. Atomen willen het liefst een volle buitenste schil hebben, net als wij een volle maag na een heerlijke maaltijd. Een volle schil betekent stabiliteit en geluk (voor atomen dan, hè). Voor stikstof is dat 8 elektronen (de zogenaamde octetregel).
Must Read
Dus, stikstof heeft 5 elektronen, en wil er graag 8. 5 + 3 = 8! Bingo! Daarom vormt stikstof het liefst drie bindingen om dat octet te bereiken. Denk erover na als een legpuzzel. Stikstof heeft 5 stukjes liggen en heeft 3 extra stukjes nodig om de puzzel af te maken.
Het is net als dat ene vriendenpaar dat altijd naar je toe komt op verjaardagen. Ze zijn superleuk, maar het zijn er maar twee. Stikstof wil er nog eentje meer, dan is het feest compleet!
De bekende voorbeelden: Ammoniak en Stikstofgas
Laten we eens kijken naar een paar bekende voorbeelden om het wat duidelijker te maken. De meest bekende is waarschijnlijk ammoniak (NH3). Hier zie je stikstof (N) gebonden aan drie waterstofatomen (H). Perfect! Elke waterstofatoom brengt één elektron mee, en stikstof levert er drie. 5 (van stikstof) + 3 (van de waterstof) = 8. Iedereen happy!

Denk hieraan als stikstof die drie beste vrienden heeft gevonden om mee te chillen. Ze hangen samen, delen een zak chips (elektronen), en alles is pais en vree.
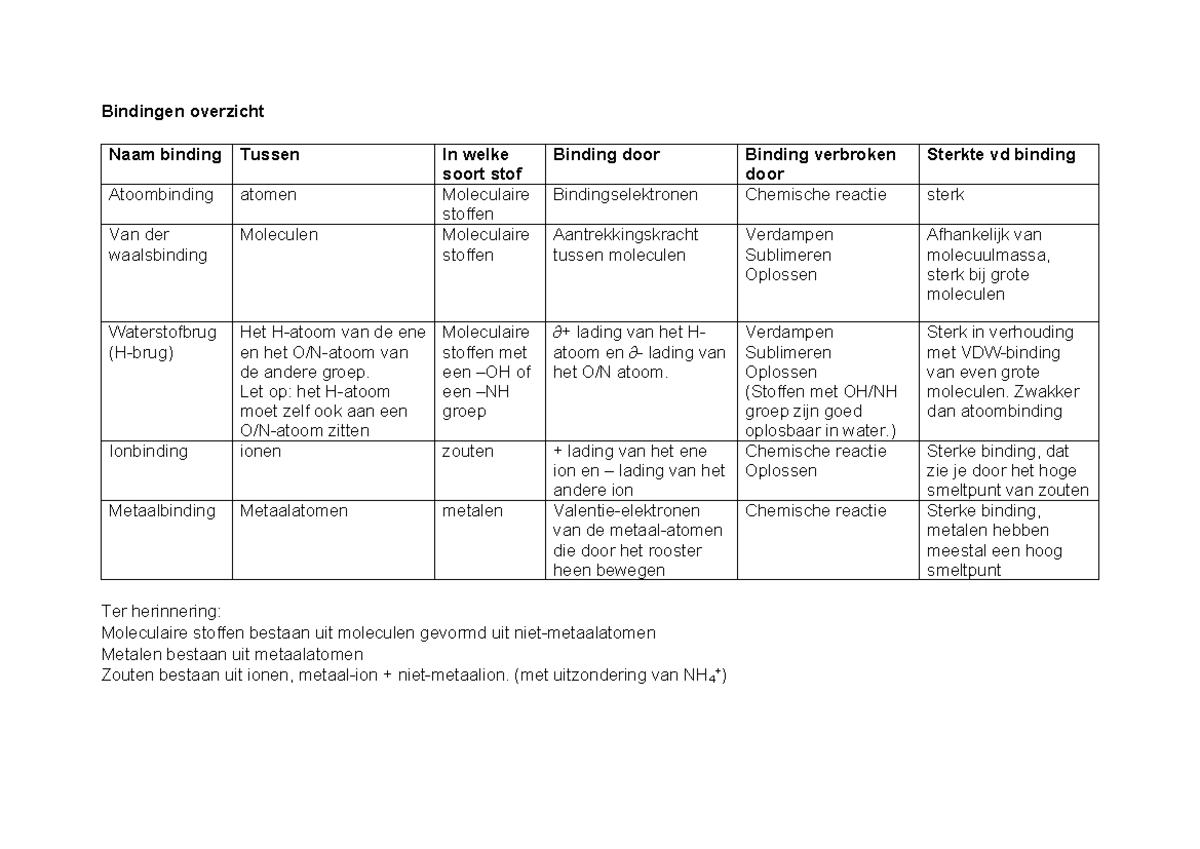
Een ander belangrijk voorbeeld is stikstofgas (N2). Dit is de vorm waarin stikstof het meest voorkomt in de lucht. Hier bindt stikstof met zichzelf! En hoe doen ze dat? Met een drievoudige binding! Elke stikstofatoom levert 3 elektronen aan de binding. Dit is een super sterke binding, en dat is waarom stikstofgas zo inert is (reageert niet snel met andere stoffen).
Zie het als twee stikstofatomen die een intense armworsteling aangaan. Ze houden elkaar stevig vast en laten niet los. Die drievoudige binding is dus echt een krachtpatser!
Uitzonderingen bevestigen de regel
Maar wacht eens even... wat als stikstof zich niet aan de regels houdt? Nou, dan krijg je dus uitzonderingen. Soms, onder speciale omstandigheden, kan stikstof toch vier bindingen aangaan. Denk aan het ammonium-ion (NH4+).
Hoe kan dat nou? In het ammonium-ion heeft stikstof vier waterstofatomen aan zich gebonden, en draagt het een positieve lading. Dit gebeurt wanneer ammoniak (NH3) een proton (H+) opneemt. Eigenlijk is het alsof je een extra gast uitnodigt op dat feestje, terwijl je eigenlijk al genoeg mensen hebt. Het is een beetje krap, maar het kan wel.
Of neem bijvoorbeeld stikstofoxiden. Sommige van deze verbindingen, zoals stikstofdioxide (NO2) of stikstofmonoxide (NO), hebben een oneven aantal elektronen. Hierdoor is de octetregel niet volledig van toepassing en kan stikstof bindingen aangaan die niet precies aan het ‘drie-bindingen’ model voldoen. Deze stoffen zijn vaak reactiever en spelen een belangrijke rol in bijvoorbeeld luchtverontreiniging.
Wanneer doet Stikstof raar?
Je kunt het vergelijken met dat ene familielid dat op de bruiloft plotseling begint te breakdancen. Het is niet wat je verwacht, maar het kan wel gebeuren. Vaak is er dan een speciale trigger: ofwel een bepaalde reactieomgeving, ofwel de aanwezigheid van andere speciale moleculen.
Die uitzonderingen zijn belangrijk, want ze maken de chemie van stikstof heel divers. Zonder deze uitzonderingen zouden er geen ingewikkelde organische moleculen met stikstof erin bestaan, en dat zou betekenen dat veel processen in de biologie (zoals DNA en eiwitten) er heel anders uit zouden zien!
Stikstof: de sociale vlinder
Dus, stikstof is over het algemeen een sociaal atoom dat graag drie bindingen aangaat. Maar zoals met alle sociale wezens, zijn er uitzonderingen. Soms heeft stikstof behoefte aan meer aandacht en vormt het vier bindingen, of soms zelfs minder.

De sleutel tot het begrijpen van de chemie van stikstof ligt in het aantal valentie-elektronen en de drang om een volle buitenste schil te bereiken. Of het nu gaat om ammoniak, stikstofgas, of andere stikstofverbindingen, de bindingseigenschappen van stikstof bepalen hun eigenschappen en reactiviteit.
De volgende keer dat je een zak chips openmaakt waarvan de verpakking is gevuld met stikstofgas (om ze knapperig te houden!), denk dan even aan al die stikstofatomen die daar met elkaar aan het armworstelen zijn in een stevige drievoudige binding. Het is allemaal chemie, en het is verrassend boeiend!
En onthoud: net als in het echte leven, zijn de uitzonderingen vaak het interessantst!










.jpg)



.jpg)
