Hoe Weet Je Of Een Stof Polair Of Apolair Is

Polariteit, in de scheikunde, is een fundamenteel concept dat beschrijft hoe elektronen verdeeld zijn binnen een molecuul. Of een stof polair of apolair is, bepaalt in grote mate de eigenschappen van die stof, zoals oplosbaarheid, kookpunt en reactiviteit. Kort gezegd: in een polair molecuul is de verdeling van elektronen oneerlijk, waardoor er lichte positieve en negatieve ladingen ontstaan. In een apolair molecuul is de verdeling gelijkmatig.
Wat is polariteit en waarom is het belangrijk?
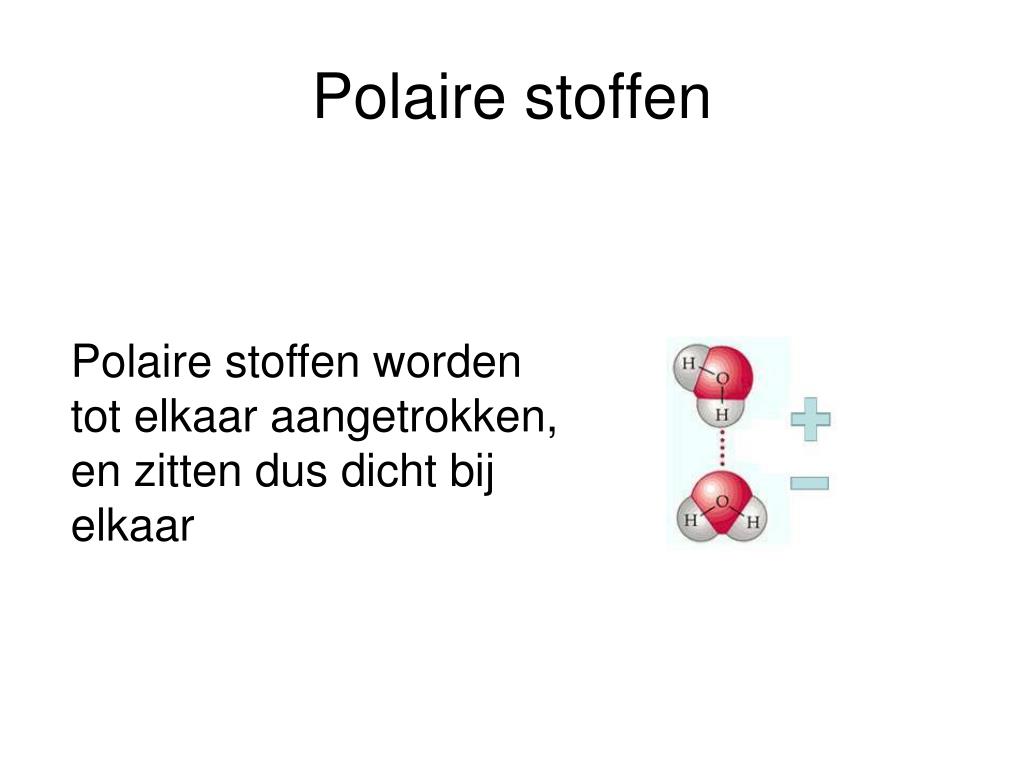
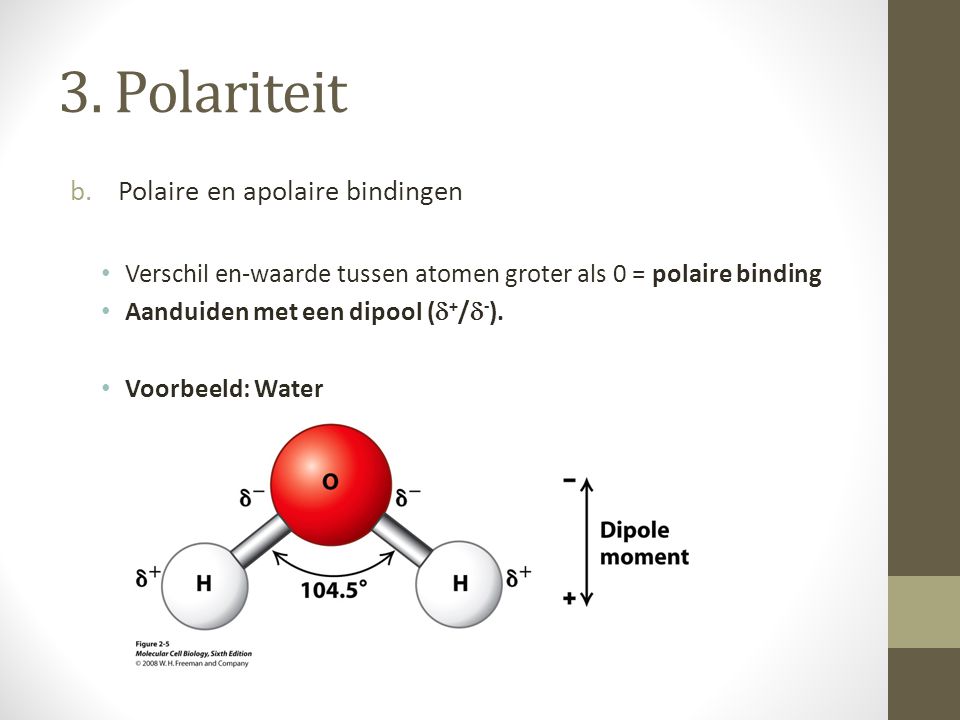
De sleutel tot het begrijpen van polariteit ligt in de elektronegativiteit van atomen. Elektronegativiteit is de mate waarin een atoom elektronen aantrekt in een chemische binding. Als twee atomen met een significant verschil in elektronegativiteit een binding aangaan, trekken de elektronen meer naar het meest elektronegatieve atoom. Dit resulteert in een gedeeltelijke negatieve lading (δ-) op het elektronegatieve atoom en een gedeeltelijke positieve lading (δ+) op het andere atoom. Deze ongelijke ladingsverdeling creëert een dipoolmoment, en het molecuul wordt beschouwd als polair.
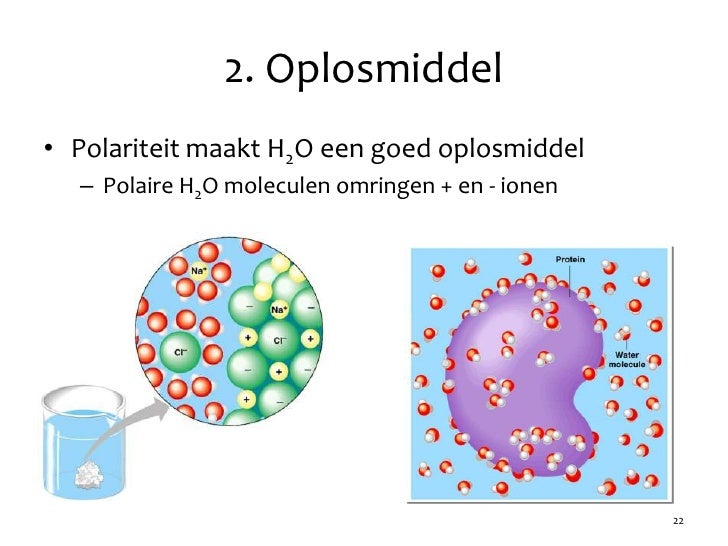
Waarom is dit belangrijk? De polariteit van een stof beïnvloedt direct hoe deze interageert met andere stoffen. "Like dissolves like" is een bekende vuistregel in de scheikunde. Dit betekent dat polaire stoffen goed oplossen in polaire oplosmiddelen (zoals water), en apolaire stoffen goed oplossen in apolaire oplosmiddelen (zoals olie). Denk aan de alledaagse ervaring van het proberen te mengen van olie en water – het lukt niet omdat water polair is en olie apolair.
Must Read
De invloed op studenten
Voor studenten is het begrijpen van polariteit cruciaal om chemische reacties, oplosbaarheid, en zelfs biologische processen te begrijpen. Bijvoorbeeld, de werking van zeep is gebaseerd op het principe van polariteit. Zeepmoleculen hebben een polair "hoofd" dat zich aangetrokken voelt tot water en een apolaire "staart" dat zich aangetrokken voelt tot vet. Hierdoor kan zeep vet en vuil emulgeren in water, waardoor ze weggespoeld kunnen worden.

Hoe bepaal je de polariteit van een stof?
Er zijn verschillende manieren om te bepalen of een stof polair of apolair is:
- Kijk naar de bindingen: Zijn de atomen in het molecuul verschillend en is er een significant verschil in elektronegativiteit? Zo ja, dan is de binding waarschijnlijk polair.
- Bekijk de moleculaire geometrie: Zelfs als een molecuul polaire bindingen bevat, kan het molecuul als geheel apolair zijn als de dipoolmomenten elkaar opheffen. Een symmetrisch molecuul zoals CO2 is bijvoorbeeld apolair, hoewel de C=O bindingen polair zijn. De dipoolmomenten wijzen in tegengestelde richtingen en heffen elkaar op.
- Experimenteer: Je kunt de oplosbaarheid van een stof testen in water (polaire oplosmiddel) en olie (apolaire oplosmiddel). Als de stof goed oplost in water, is het waarschijnlijk polair; als het goed oplost in olie, is het waarschijnlijk apolair.
Voorbeelden uit het dagelijks leven en school
In de school: Tijdens practica leren leerlingen over extractietechnieken. Denk aan de extractie van cafeïne uit thee met behulp van dichloormethaan, een apolair oplosmiddel. De cafeïne lost beter op in dichloormethaan dan in water vanwege de apolaire aard van beide stoffen. Dit experiment demonstreert de praktische toepassing van polariteit.
In het dagelijks leven: Het bakken van een cake vereist dat je vet (apolair) mengt met bijvoorbeeld eieren (deels polair). Emulgatoren, zoals lecithine in eieren, helpen om deze stoffen te mengen door zowel polaire als apolaire delen aan te trekken.
“Understanding polarity is fundamental to grasping the behavior of molecules and their interactions,” zegt Dr. Anna de Vries, een scheikundedocent.
Conclusie
Polariteit is een cruciaal concept in de scheikunde dat de eigenschappen en het gedrag van stoffen bepaalt. Door de principes van elektronegativiteit, moleculaire geometrie, en de 'like dissolves like' regel te begrijpen, kunnen studenten de polariteit van een stof voorspellen en de implicaties daarvan begrijpen in zowel academische contexten als in het dagelijks leven.