Hoe Herken Je Een Zuur Base Reactie

Zuur-base reacties, ook wel neutralisatiereacties genoemd, zijn fundamentele chemische processen die een cruciale rol spelen in vele aspecten van ons dagelijks leven en in de industrie. Of het nu gaat om het neutraliseren van maagzuur met een antacidum, het regelen van de pH in de bodem voor een optimale plantengroei, of het produceren van zeep, zuur-base reacties zijn alomtegenwoordig. Het begrijpen van hoe je een zuur-base reactie kunt herkennen is dan ook essentieel voor iedereen met een interesse in scheikunde of voor wie simpelweg beter wil begrijpen hoe de wereld om ons heen werkt. Dit artikel zal dieper ingaan op de belangrijkste kenmerken en signalen van zuur-base reacties, waardoor je in staat zult zijn ze te identificeren en te begrijpen.
De Basisprincipes: Zuren en Basen
Voordat we dieper ingaan op de herkenning van zuur-base reacties, is het belangrijk om de basisdefinities van zuren en basen te begrijpen. Er zijn verschillende theorieën die zuren en basen definiëren, maar de meest voorkomende zijn:
- Arrhenius theorie: Zuren produceren waterstofionen (H+) in waterige oplossingen, terwijl basen hydroxide-ionen (OH-) produceren.
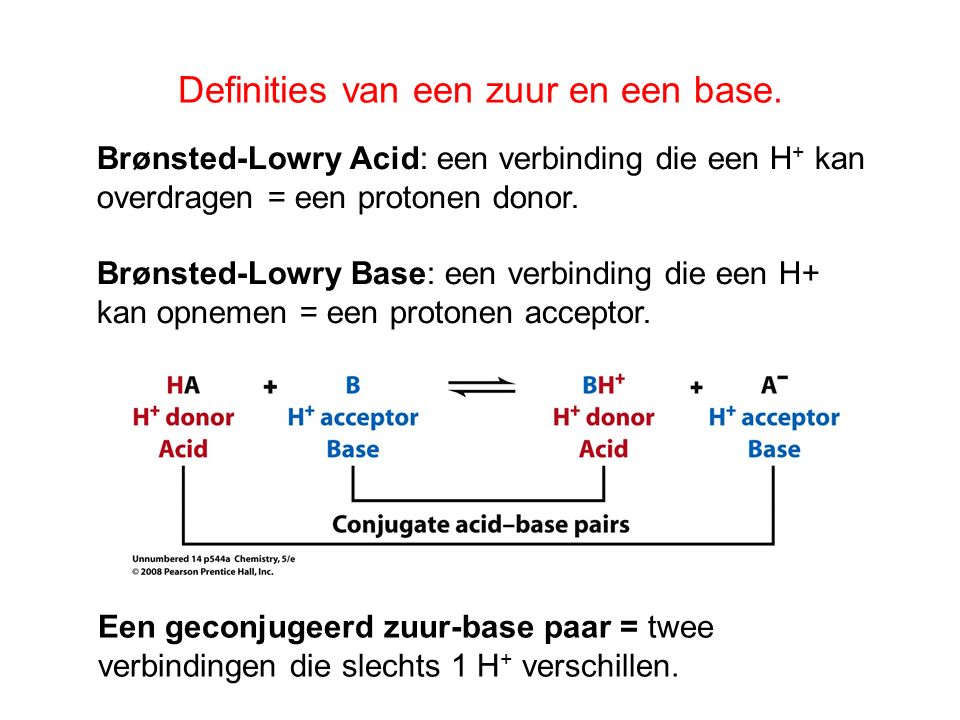
- Brønsted-Lowry theorie: Zuren zijn protondonoren (ze staan H+ af) en basen zijn protonacceptoren (ze nemen H+ op). Dit is de meest gebruikte definitie.
- Lewis theorie: Zuren zijn elektronenpaaracceptoren en basen zijn elektronenpaardonoren. Deze definitie is het meest algemeen.
In de context van dit artikel zullen we voornamelijk de Brønsted-Lowry theorie gebruiken, omdat deze het meest relevant is voor het herkennen van zuur-base reacties in de praktijk.
Must Read
Belangrijke Kenmerken van Zuren:
- Zure smaak: (Let op: proeven is nooit veilig in een laboratorium!).
- Reageren met metalen: Vele zuren reageren met metalen, waarbij waterstofgas (H2) vrijkomt. Denk aan de reactie van zoutzuur (HCl) met zink (Zn).
- Veranderen de kleur van indicatoren: Zuren kleuren lakmoespapier rood en fenolftaleïne kleurloos.
- Neutraliseren basen: Dit is het kernpunt van een zuur-base reactie.
Belangrijke Kenmerken van Basen:
- Bittere smaak: (Ook hier geldt: proeven is nooit veilig!).
- Glad aanvoelen: Basen voelen vaak zeepachtig aan.
- Veranderen de kleur van indicatoren: Basen kleuren lakmoespapier blauw en fenolftaleïne roze (in voldoende concentratie).
- Neutraliseren zuren: Dit is de wederzijdse actie van een zuur-base reactie.
Hoe Herken je een Zuur-Base Reactie?
Het identificeren van een zuur-base reactie vereist aandacht voor verschillende potentiële indicatoren. Hier zijn de belangrijkste signalen:
1. pH-verandering
De pH is een maat voor de zuurgraad of basiciteit van een oplossing. Een pH van 7 is neutraal, lager dan 7 is zuur en hoger dan 7 is basisch. Een zuur-base reactie resulteert in een verandering van de pH. Als een zuur aan een base wordt toegevoegd (of omgekeerd), zal de pH van de oplossing naar de 7 gaan. De pH-verandering kan gemeten worden met een pH-meter, pH-papier, of door gebruik te maken van indicatoren.
Voorbeeld: Als je een sterke base zoals natronloog (NaOH) toevoegt aan een zure oplossing zoals zoutzuur (HCl), zal de pH van de oplossing stijgen naarmate de base wordt toegevoegd. Uiteindelijk zal de pH rond de 7 stabiliseren wanneer het zuur en de base elkaar neutraliseren.

2. Kleurverandering van een Indicator
Indicatoren zijn stoffen die van kleur veranderen afhankelijk van de pH van de oplossing. Er zijn veel verschillende indicatoren beschikbaar, elk met een eigen pH-bereik waarin ze van kleur veranderen. Enkele bekende indicatoren zijn:
- Lakmoes: Rood in zure oplossing, blauw in basische oplossing.
- Fenolftaleïne: Kleurloos in zure oplossing, roze in basische oplossing (boven pH 8.3).
- Methyloranje: Rood in zure oplossing, geel in basische oplossing.
De kleurverandering van een indicator is een duidelijk teken dat een zuur-base reactie plaatsvindt. De keuze van de indicator hangt af van het verwachte pH-bereik van de reactie.
Voorbeeld: Stel je voor dat je een onbekende oplossing hebt en je voegt er een paar druppels fenolftaleïne aan toe. Als de oplossing roze wordt, weet je dat de oplossing basisch is. Als je vervolgens een zuur toevoegt, zal de roze kleur verdwijnen naarmate het zuur de base neutraliseert.
3. Warmteontwikkeling (Exotherme Reactie)
De meeste zuur-base reacties zijn exotherm, wat betekent dat ze warmte produceren. Wanneer een zuur en een base reageren, wordt energie vrijgegeven in de vorm van warmte, waardoor de temperatuur van de oplossing stijgt. Dit kan worden gemeten met een thermometer.
Let op: Niet alle reacties die warmte produceren zijn zuur-base reacties. Er zijn ook andere chemische reacties die exotherm zijn.
Voorbeeld: Het mengen van geconcentreerd zwavelzuur (H2SO4) met water is een zeer exotherme reactie. De temperatuur van het water zal aanzienlijk stijgen. Belangrijk: Voeg altijd zuur toe aan water, nooit water aan zuur, om spatten en overkoken te voorkomen!
4. Vorming van een Zout en Water
Een zuur-base reactie resulteert in de vorming van een zout en water. Het zout is een ionische verbinding die bestaat uit het kation van de base en het anion van het zuur.
Algemene reactievergelijking:
Zuur + Base → Zout + Water
Voorbeeld:
HCl (zuur) + NaOH (base) → NaCl (zout) + H2O (water)
In dit voorbeeld is zoutzuur (HCl) een zuur en natronloog (NaOH) een base. De reactie produceert natriumchloride (NaCl), beter bekend als keukenzout, en water (H2O).

5. Gasontwikkeling (in sommige gevallen)
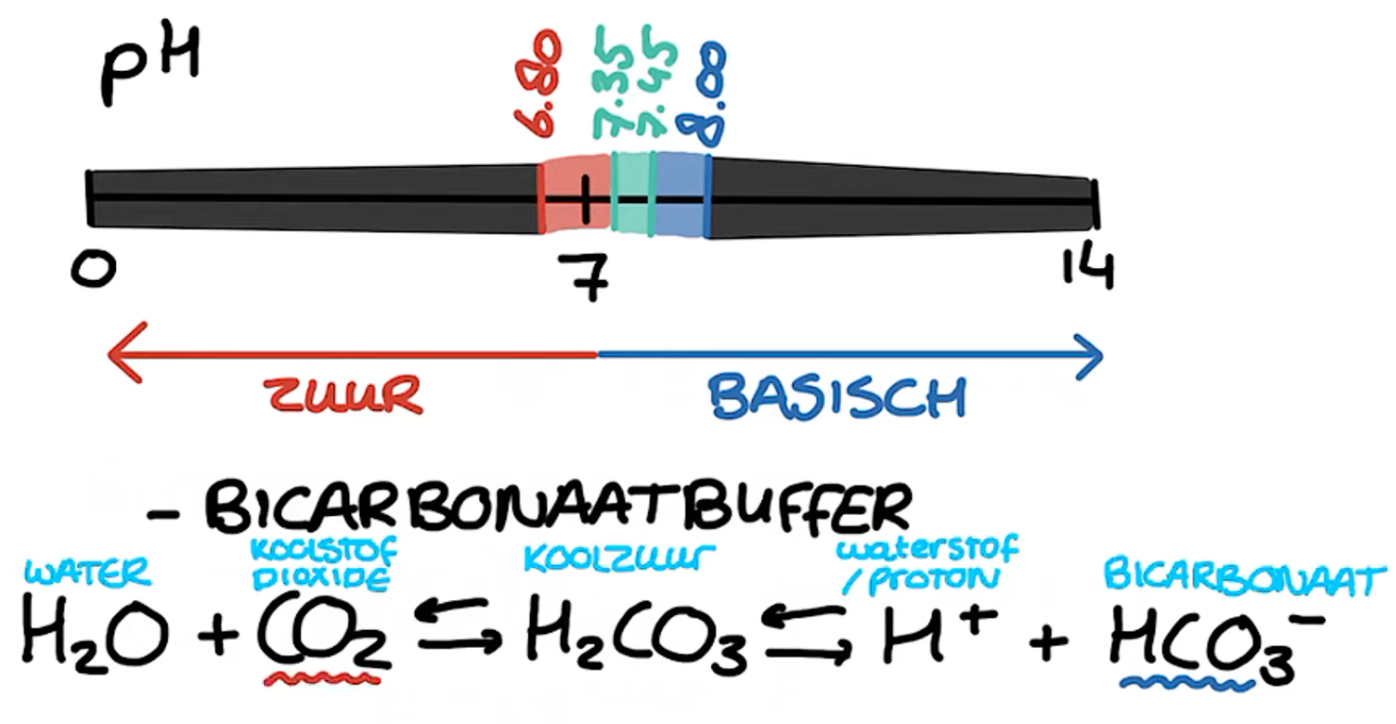
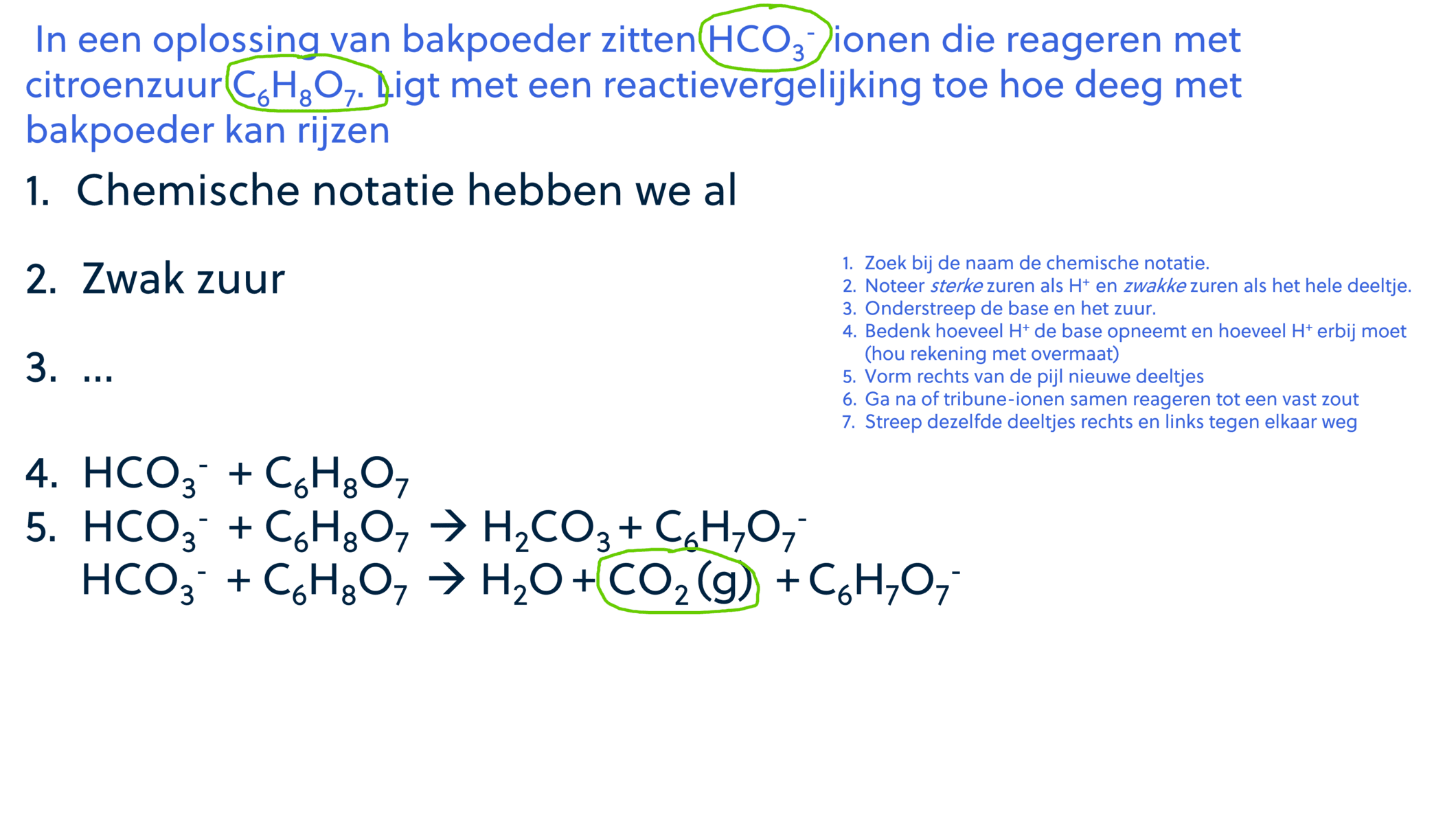
Hoewel niet alle zuur-base reacties gas produceren, zijn er sommige waarbij dit wel gebeurt. Dit gebeurt vooral wanneer een zuur reageert met een carbonaat (CO32-) of bicarbonaat (HCO3-) zout. Bij deze reactie ontstaat koolzuur (H2CO3), wat direct uiteenvalt in water (H2O) en koolstofdioxide gas (CO2). De bruisende werking die je ziet is het gevolg van de vrijgekomen CO2.
Voorbeeld: Het toevoegen van azijnzuur (CH3COOH) aan bakpoeder (NaHCO3) produceert koolstofdioxide gas, water en natriumacetaat. Dit is de basis achter het rijzen van deeg bij het bakken.
Real-World Voorbeelden en Data
- Antacida: Maagzuur is een oplossing van zoutzuur (HCl). Antacida bevatten vaak basen zoals magnesiumhydroxide (Mg(OH)2) of calciumcarbonaat (CaCO3) om het maagzuur te neutraliseren. De reactie verhoogt de pH in de maag, waardoor brandend maagzuur vermindert.
- Bodemneutralisatie: Zure grond kan de groei van planten belemmeren. Landbouwers gebruiken vaak kalk (calciumcarbonaat, CaCO3) om de zuurgraad van de bodem te neutraliseren en de pH te verhogen tot een niveau dat geschikt is voor plantengroei. Data uit bodemanalyses tonen aan dat na toevoeging van kalk de pH significant stijgt.
- Titraties: In de chemie worden titraties gebruikt om de concentratie van een zuur of base in een oplossing te bepalen. Een bekende oplossing van een zuur of base (de titrant) wordt langzaam toegevoegd aan de onbekende oplossing totdat de reactie voltooid is. De completion wordt vaak bepaald door een indicator of een pH-meter.
- Zeepfabricage (Verzeping): Zeep wordt gemaakt door een vet (een ester) te laten reageren met een sterke base zoals natronloog (NaOH). Deze reactie, bekend als verzeping, produceert zeep (een zout van een vetzuur) en glycerol.
Conclusie en Call to Action
Het herkennen van een zuur-base reactie is essentieel voor het begrijpen van chemische processen in verschillende contexten, van het dagelijks leven tot de industrie. Door te letten op pH-veranderingen, kleurveranderingen van indicatoren, warmteontwikkeling, de vorming van zout en water, en in sommige gevallen gasontwikkeling, kun je een zuur-base reactie identificeren.
Om je begrip verder te verdiepen, moedigen we je aan om zelf te experimenteren met eenvoudige zuur-base reacties, zoals het neutraliseren van azijn met bakpoeder. Lees meer over verschillende indicatoren en hun pH-bereiken. Zoek naar online simulaties van titraties om de principes van neutralisatie beter te begrijpen. Door actief bezig te zijn met deze concepten, zul je een dieper inzicht krijgen in de fascinerende wereld van de scheikunde!