Hoe Bereken Je Het Aantal Neutronen

Weet je, het kan best overweldigend zijn om te duiken in de wereld van de atoomstructuur. Je hoort termen als protonen, elektronen en neutronen, en het lijkt soms alsof je een compleet nieuwe taal moet leren. Veel mensen worstelen met basisconcepten uit de scheikunde en natuurkunde, en het berekenen van het aantal neutronen is daar vaak een van. Misschien heb je een schoolopdracht, ben je gewoon nieuwsgierig, of probeer je ingewikkelde concepten in de nucleaire geneeskunde te begrijpen. Wat je reden ook is, het is belangrijk om te weten dat je niet de enige bent! Laten we dit samen stap voor stap ontrafelen.
Waarom zou je eigenlijk het aantal neutronen willen weten? Nou, het is crucialer dan je denkt. De verhouding tussen protonen en neutronen in een atoom beïnvloedt de stabiliteit van de atoomkern. Dit is van direct belang bij:
- Kernenergie: De stabiliteit van atomen in brandstof (zoals uranium) is essentieel voor veilige en efficiënte energieproductie.
- Medische toepassingen: Radioactieve isotopen (verschillende versies van een atoom met een verschillend aantal neutronen) worden gebruikt in de diagnostiek (scans) en behandeling van kanker. Het begrijpen van hun vervalprocessen vereist kennis van het aantal neutronen.
- Dateringstechnieken: Koolstof-14 datering, een methode om de leeftijd van organisch materiaal te bepalen, is gebaseerd op de vervalsnelheid van een koolstof-isotoop met een specifiek aantal neutronen.
- Fundamenteel onderzoek: Wetenschappers gebruiken botsingen van deeltjes in deeltjesversnellers om de fundamentele bouwstenen van materie te bestuderen. Kennis van de samenstelling van atoomkernen is hierbij onmisbaar.
De Basis: Atoomnummer en Massagetal
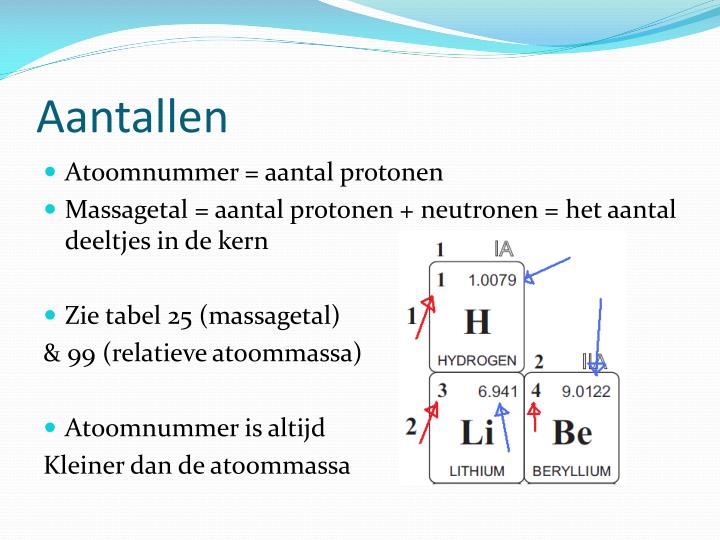
Laten we beginnen met de basis. Elk atoom heeft een atoomnummer (symbool: Z) en een massagetal (symbool: A).
Must Read
Het atoomnummer (Z) staat voor het aantal protonen in de kern van het atoom. Dit getal bepaalt welk element het is. Zo heeft elk atoom met 1 proton in de kern een atoomnummer van 1 en is het waterstof (H). Elk atoom met 6 protonen is koolstof (C), enzovoort. Je vindt het atoomnummer terug in het periodiek systeem.
Het massagetal (A) is het totale aantal protonen en neutronen in de kern. Het is dus de 'massa' van de kern, vandaar de naam. Let op: dit is niet de atoommassa zoals je die in het periodiek systeem vindt (deze is een gemiddelde van de massa's van alle isotopen, zie verderop).
De Formule
De formule om het aantal neutronen (N) te berekenen is eigenlijk heel simpel:

N = A - Z
Ofwel:
Aantal neutronen = Massagetal - Atoomnummer
Een Stap-voor-Stap Voorbeeld
Laten we dit illustreren met een voorbeeld: Koolstof-12 (12C).
- Zoek het atoomnummer (Z) van koolstof (C) op in het periodiek systeem. Je vindt dat Z = 6. Dit betekent dat een koolstofatoom 6 protonen heeft.
- Het massagetal (A) van koolstof-12 is 12. Dit is aangegeven als superscript voor het symbool C: 12C.
- Gebruik de formule: N = A - Z. Dus N = 12 - 6 = 6.
- Conclusie: Een koolstof-12 atoom heeft 6 neutronen.
Nog een voorbeeld: Uranium-238 (238U)
- Atoomnummer (Z) van uranium (U): 92 (zoek dit op in het periodiek systeem).
- Massagetal (A) van uranium-238: 238
- Bereken het aantal neutronen (N): N = 238 - 92 = 146
- Conclusie: Een uranium-238 atoom heeft 146 neutronen.
Isotopen: Variaties in het Aantal Neutronen
Nu wordt het iets ingewikkelder, maar blijf bij me! Isotopen zijn atomen van hetzelfde element (dus met hetzelfde atoomnummer) maar met een verschillend aantal neutronen. Dit betekent dat ze een verschillend massagetal hebben.
Neem bijvoorbeeld koolstof. We hebben koolstof-12 (12C) bekeken, maar er is ook koolstof-14 (14C). Beide zijn koolstof, dus ze hebben allebei 6 protonen (Z = 6). Maar koolstof-14 heeft een massagetal van 14. Dus het aantal neutronen in koolstof-14 is N = 14 - 6 = 8. Koolstof-14 heeft dus 2 neutronen meer dan koolstof-12.
Het bestaan van isotopen verklaart waarom de atoommassa die je in het periodiek systeem vindt, vaak geen geheel getal is. De atoommassa is namelijk een gewogen gemiddelde van de massa's van alle isotopen van dat element, rekening houdend met hun natuurlijke voorkomen.

Veelgemaakte Fouten en Hoe Ze Te Vermijden
Een veelgemaakte fout is het verwarren van het atoomnummer en het massagetal. Onthoud: het atoomnummer definieert het element, het massagetal is de som van protonen en neutronen. Kijk altijd goed naar de notatie! Soms staat het massagetal niet expliciet vermeld, maar moet je het afleiden uit de context van de vraag of de gegeven informatie.
Een andere fout is het vergeten dat de atoommassa (zoals vermeld in het periodiek systeem) een gemiddelde is en niet het massagetal van een specifiek isotoop. Gebruik altijd het gegeven massagetal als je dat hebt.
Kritiek en Alternatieve Methoden (voor geavanceerde gebruikers)
Voor de meesten van ons is de formule N = A - Z voldoende. Maar in sommige zeer specifieke contexten kan het nodig zijn om rekening te houden met nog subtielere effecten, zoals de massa-defecten (het kleine verschil tussen de massa van een atoomkern en de som van de massa's van de individuele protonen en neutronen). Dit is echter alleen relevant bij zeer nauwkeurige berekeningen in de kernfysica.
Sommige geavanceerde technieken, zoals massaspectrometrie, worden gebruikt om de massa's van individuele isotopen zeer nauwkeurig te bepalen. Dit kan indirect worden gebruikt om het aantal neutronen af te leiden.

Oefening Baart Kunst
De beste manier om dit onder de knie te krijgen, is door te oefenen. Zoek een periodiek systeem op, kies een aantal elementen en isotopen, en bereken het aantal neutronen. Daag jezelf uit! Je zult merken dat het al snel vanzelf gaat.
Hier zijn een paar oefenopgaven:
- Bepaal het aantal neutronen in helium-4 (4He).
- Bepaal het aantal neutronen in zuurstof-16 (16O).
- Bepaal het aantal neutronen in jodium-131 (131I).
En onthoud: er is geen schande om er even over te doen. Rome is ook niet in één dag gebouwd! Iedereen leert op zijn eigen tempo. Als je vastloopt, zoek dan online naar meer informatie, bekijk YouTube-video's, of vraag hulp aan een docent of medestudent.
We hopen dat dit artikel je heeft geholpen om het berekenen van het aantal neutronen beter te begrijpen. Het is een fundamenteel concept dat de deur opent naar een dieper begrip van de wereld om ons heen. Maar nu, wat ga jij doen met deze nieuwe kennis? Ga je nu verder met het bestuderen van isotopen, kernenergie of misschien de medische toepassingen van radioactiviteit?