Hoe Bereken Je De Molaire Massa

Ken je dat gevoel? Je zit te zwoegen op een scheikundeopgave, de deadline nadert, en je staart je blind op die ene cruciale berekening: de molaire massa. Of je bent een ouder die zijn kind probeert te helpen met huiswerk, maar merkt dat de scheikunde van jouw schooltijd toch net iets anders was. Misschien ben je zelfs een docent die voortdurend zoekt naar manieren om dit concept duidelijker uit te leggen. De molaire massa kan een struikelblok zijn, dat is zeker. Maar vrees niet! Met de juiste aanpak en een beetje geduld, wordt het een fluitje van een cent.
Wat is Molaire Massa Eigenlijk?
Laten we beginnen bij de basis. De molaire massa is de massa van één mol van een bepaalde stof. Een mol? Ja, dat is de hoeveelheid stof die evenveel deeltjes bevat als er atomen zijn in 12 gram koolstof-12. Dit getal, bekend als de constante van Avogadro, is ongeveer 6,022 x 1023 deeltjes. In simpelere termen: de molaire massa vertelt je hoeveel gram een "stapel" van 6,022 x 1023 deeltjes van die stof weegt. Het is een cruciale eenheid in de scheikunde, omdat het ons in staat stelt om van massa naar aantal deeltjes (en vice versa) te converteren.
De eenheid van molaire massa is gram per mol (g/mol). Het is de massa in grammen van één mol van een stof. Je kunt de molaire massa zien als een soort 'gewicht per dozijn', maar dan voor atomen en moleculen.
Must Read
Waarom is het Belangrijk?
Molaire massa is geen abstract concept dat alleen in laboratoria wordt gebruikt. Het is essentieel voor:
- Stoichiometrie: Het berekenen van de hoeveelheden reactanten en producten in chemische reacties.
- Concentratiebepaling: Het bepalen van de concentratie van oplossingen.
- Analyse: Het identificeren van onbekende stoffen.
- Farmacie: Het berekenen van doseringen van medicijnen.
Kortom, de molaire massa is een fundamentele bouwsteen voor vrijwel alle kwantitatieve berekeningen in de scheikunde. Zonder het, zouden we niet in staat zijn om nauwkeurig te voorspellen hoeveel van een bepaalde stof we nodig hebben voor een reactie, of hoeveel product we kunnen verwachten te vormen.
Hoe Bereken Je het: Stap voor Stap
Stap 1: Zoek de Chemische Formule
Dit is de allereerste stap. Je moet de chemische formule van de stof kennen. Bijvoorbeeld, water heeft de formule H2O, natriumchloride is NaCl, en glucose is C6H12O6. Zonder de juiste formule, kun je de molaire massa niet correct berekenen.
Voorbeeld: We gebruiken water (H2O) als voorbeeld.

Stap 2: Zoek de Atoommassa's op in het Periodiek Systeem
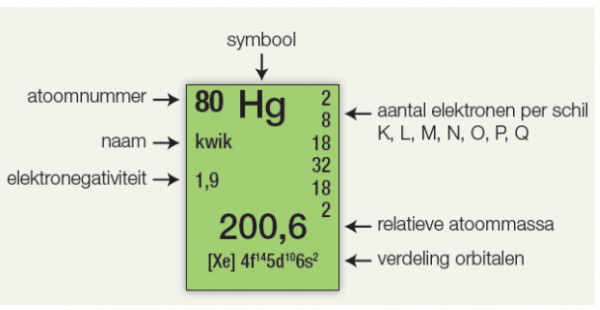
Het periodiek systeem der elementen is je beste vriend hier. Voor elk element vind je de atoommassa, meestal aangegeven als een decimaal getal onder het symbool van het element. Deze atoommassa is eigenlijk de gemiddelde massa van een atoom van dat element, rekening houdend met de natuurlijke verhoudingen van de verschillende isotopen.
Belangrijk: Rond de atoommassa's niet te vroeg af. Gebruik minimaal één decimaal voor nauwkeurigere resultaten.
Voorbeeld:
- Waterstof (H): Atoommassa ≈ 1,01 g/mol
- Zuurstof (O): Atoommassa ≈ 16,00 g/mol
Stap 3: Vermenigvuldig Atoommassa's met het Aantal Atomen
In de chemische formule zie je hoeveel atomen van elk element er in de molecule aanwezig zijn. Vermenigvuldig de atoommassa van elk element met het aantal atomen van dat element in de formule.

Voorbeeld:
- Water (H2O):
- Waterstof (H): 2 atomen x 1,01 g/mol = 2,02 g/mol
- Zuurstof (O): 1 atoom x 16,00 g/mol = 16,00 g/mol
Stap 4: Tel de Resultaten bij Elkaar op
Tel de resultaten van de vorige stap bij elkaar op om de totale molaire massa te krijgen.
Voorbeeld:
- Water (H2O): 2,02 g/mol + 16,00 g/mol = 18,02 g/mol
Dus, de molaire massa van water is ongeveer 18,02 g/mol.

Voorbeelden en Oefeningen
Laten we een paar voorbeelden bekijken om de puntjes op de i te zetten:
Voorbeeld 1: Natriumchloride (NaCl)
- Natrium (Na): Atoommassa ≈ 22,99 g/mol
- Chloor (Cl): Atoommassa ≈ 35,45 g/mol
- Molaire massa NaCl = 22,99 g/mol + 35,45 g/mol = 58,44 g/mol
Voorbeeld 2: Glucose (C6H12O6)
- Koolstof (C): Atoommassa ≈ 12,01 g/mol
- Waterstof (H): Atoommassa ≈ 1,01 g/mol
- Zuurstof (O): Atoommassa ≈ 16,00 g/mol
- Molaire massa Glucose = (6 x 12,01 g/mol) + (12 x 1,01 g/mol) + (6 x 16,00 g/mol) = 72,06 g/mol + 12,12 g/mol + 96,00 g/mol = 180,18 g/mol
Oefening voor Thuis:
Bereken de molaire massa van:

- Ammoniak (NH3)
- Zwavelzuur (H2SO4)
- Ethanol (C2H5OH)
Tips en Trucs
- Wees Nauwkeurig: Gebruik de atoommassa's uit het periodiek systeem zo nauwkeurig mogelijk. Te vroeg afronden kan leiden tot onnauwkeurige resultaten.
- Let op de Haakjes: Als er haakjes in de formule staan, vermenigvuldig dan de aantallen atomen binnen de haakjes met de subscript buiten de haakjes. Bijvoorbeeld, in Mg(OH)2, zijn er 2 zuurstofatomen en 2 waterstofatomen.
- Controleer Je Werk: Dubbelcheck je berekeningen. Het is makkelijk om een foutje te maken, vooral bij complexere formules.
- Gebruik een Rekenmachine: Een goede rekenmachine met wetenschappelijke functies is essentieel.
- Oefening Baart Kunst: Hoe meer je oefent, hoe sneller en zelfverzekerder je wordt.
Veelgemaakte Fouten
Sommige fouten komen vaak voor bij het berekenen van de molaire massa. Hier zijn een paar om op te letten:
- Verkeerde Formule: De meest voorkomende fout is het gebruik van een verkeerde chemische formule. Controleer de formule altijd zorgvuldig.
- Verkeerde Atoommassa's: Het gebruik van verkeerde atoommassa's uit het periodiek systeem. Zorg ervoor dat je de juiste waarden gebruikt.
- Vergeten te Vermenigvuldigen: Vergeten de atoommassa's te vermenigvuldigen met het aantal atomen van elk element in de formule.
- Afrondingsfouten: Te vroeg afronden van atoommassa's kan leiden tot een significant verschil in het eindresultaat.
Molaire Massa in de Praktijk: Een Voorbeeld in de Klas
Stel je voor: je doet een experiment in de klas waarbij je magnesiumoxide (MgO) maakt door magnesium te verbranden. Je wilt weten hoeveel magnesium je nodig hebt om een bepaalde hoeveelheid magnesiumoxide te produceren. Om dit te berekenen, heb je de molaire massa van magnesium (Mg) en magnesiumoxide (MgO) nodig.
Je berekent de molaire massa van Mg (24,31 g/mol) en MgO (24,31 g/mol + 16,00 g/mol = 40,31 g/mol). Met deze waarden kun je de stoichiometrie van de reactie gebruiken om te bepalen hoeveel gram magnesium je nodig hebt om bijvoorbeeld 10 gram MgO te produceren. Dit is een concreet voorbeeld van hoe molaire massa wordt gebruikt in een praktische context.
Een Persoonlijk Verhaal: Ik herinner me dat ik zelf worstelde met molaire massa tijdens mijn eerste scheikunde les. Ik begreep het concept gewoon niet. Pas toen mijn docent het uitlegde aan de hand van alledaagse voorwerpen (zoals het aantal eieren in een doos), begon ik het te begrijpen. Het is belangrijk om geduldig te zijn met jezelf en om verschillende benaderingen te proberen totdat je het begrijpt.
Conclusie
De molaire massa is een essentieel concept in de scheikunde, maar met de juiste aanpak is het zeker te begrijpen. Door de stappen zorgvuldig te volgen, veel te oefenen en aandacht te besteden aan details, kun je deze cruciale berekening onder de knie krijgen. Onthoud: oefening baart kunst! En vergeet niet, het periodiek systeem is je vriend! Dus, pak je rekenmachine, duik in de wereld van de scheikunde, en laat die molaire massa's maar komen!





+%EF%83%A0+getalwaarde+gelijk+aan+de+molecuulmassa+of+atoommassa+van+de+stof..jpg)



+van+een+stof+is+in+getalwaarde+gelijk+aan+de+molecuulmassa+of+atoommassa+van+de+stof..jpg)



