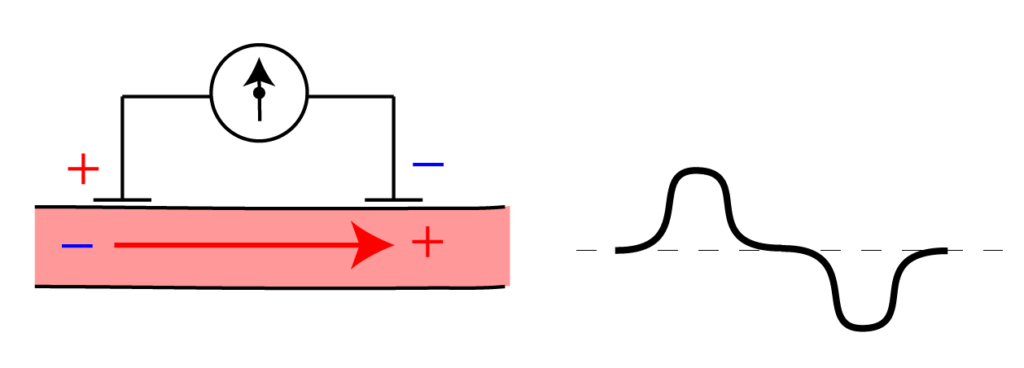
Elektrode Aan De Positieve Pool
Het klinkt misschien als iets uit een scheikundeles die je lang geleden hebt gehad, maar de elektrode aan de positieve pool – in veel gevallen de anode – is een fundamenteel onderdeel van talloze alledaagse technologieën. We denken er zelden over na, totdat iets niet meer werkt, zoals een batterij die leeg is, of een auto die niet start. Laten we eens dieper ingaan op dit belangrijke, maar vaak onopgemerkte concept.
Wat is een Elektrode en Waarom is de Positieve Pool Belangrijk?
Simpel gezegd, een elektrode is een elektrische geleider die wordt gebruikt om een niet-metalen deel van een circuit aan te sluiten. Denk aan een batterij, een galvanisch element, of een elektrolyse opstelling. Ze maken de stroom van elektriciteit mogelijk naar of van een object. De polariteit van de elektrode – positief of negatief – is cruciaal omdat het de richting van de stroom en de chemische reacties die plaatsvinden bepaalt.
De Rol van de Anode
De anode, of positieve elektrode, is de plaats waar oxidatie plaatsvindt. Oxidatie betekent in essentie dat een atoom, molecuul of ion elektronen verliest. In een batterij bijvoorbeeld, geeft het materiaal van de anode elektronen af die via het externe circuit naar de kathode (de negatieve elektrode) stromen. Dit creëert de elektrische stroom die we gebruiken om onze apparaten aan te drijven.
Must Read
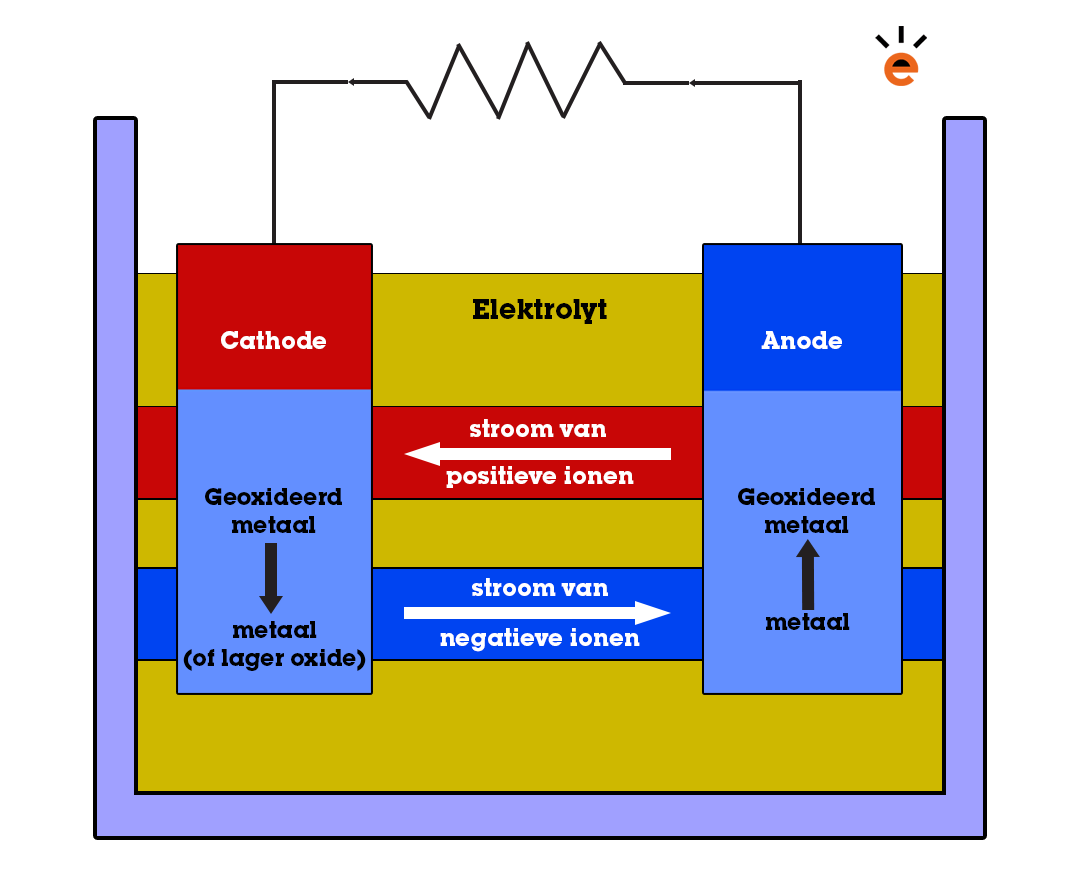
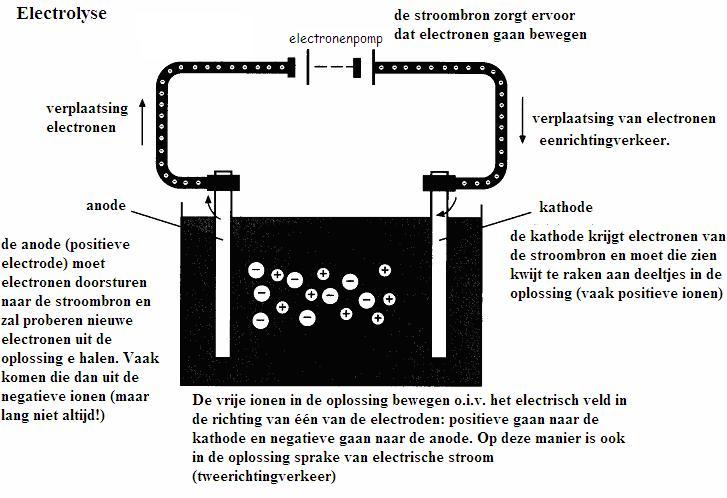
Het is belangrijk op te merken dat de termen 'anode' en 'positieve elektrode' niet altijd synoniem zijn. In een galvanisch element (zoals een batterij) is de anode inderdaad de positieve elektrode. Echter, in een elektrolysecel (waarbij elektrische energie wordt gebruikt om een chemische reactie te forceren) is de anode de negatieve elektrode, omdat elektronen hier naartoe worden getrokken om de oxidatie te laten plaatsvinden.
Laten we dit verduidelijken met een paar voorbeelden:
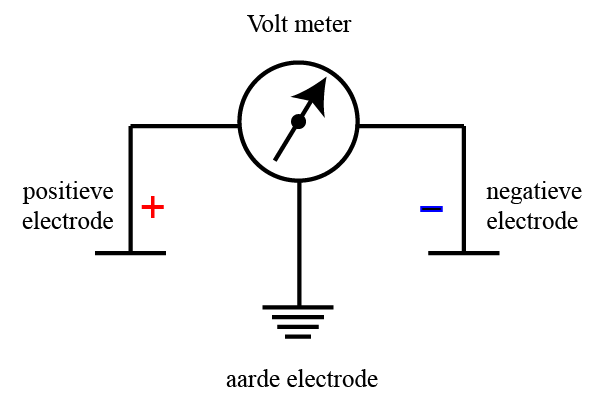
- Batterijen: Hier is de anode de positieve pool. Denk aan een AA-batterij. De positieve kant is de anode waar de chemische reactie plaatsvindt die elektronen vrijgeeft.
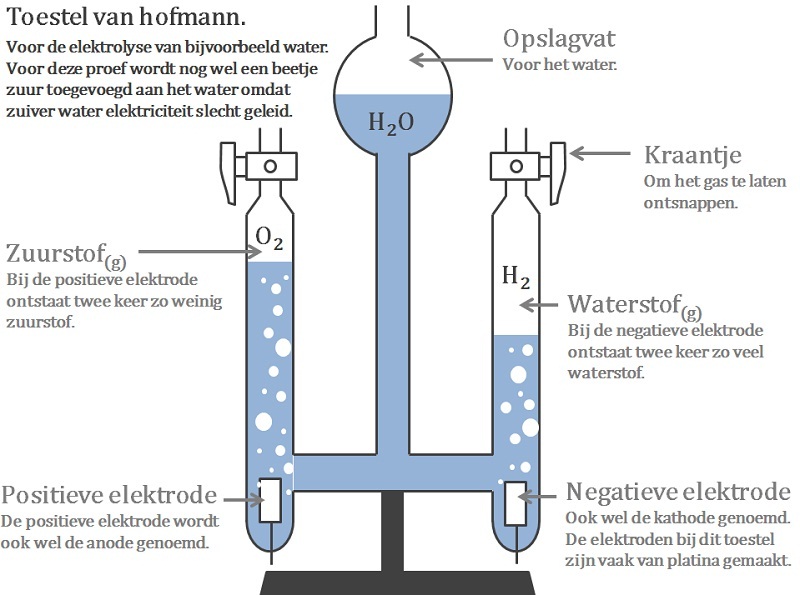
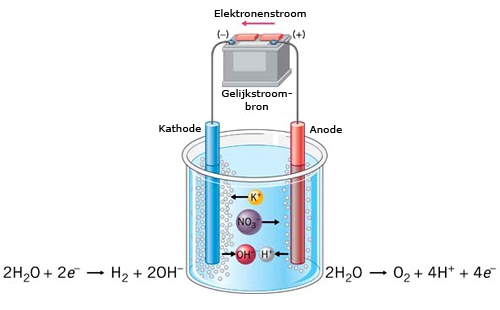
- Elektrolyse van water: Hier is de anode de positieve pool. Water wordt afgebroken in zuurstof en waterstof. Zuurstof wordt gevormd aan de anode.
- Lassen: Bij sommige lasprocessen fungeert de elektrode als anode. De hitte die vrijkomt bij de elektrische stroom smelt het metaal.
De Impact in de Praktijk: Meer dan Alleen Batterijen
De principes rond de anode en de positieve pool zijn niet beperkt tot batterijen. Ze hebben een immense invloed op diverse industrieën en technologieën:
- Autobatterijen: Het starten van je auto is direct afhankelijk van de chemische reacties die plaatsvinden aan de anode van de accu. Een slechte anode betekent een auto die niet start.
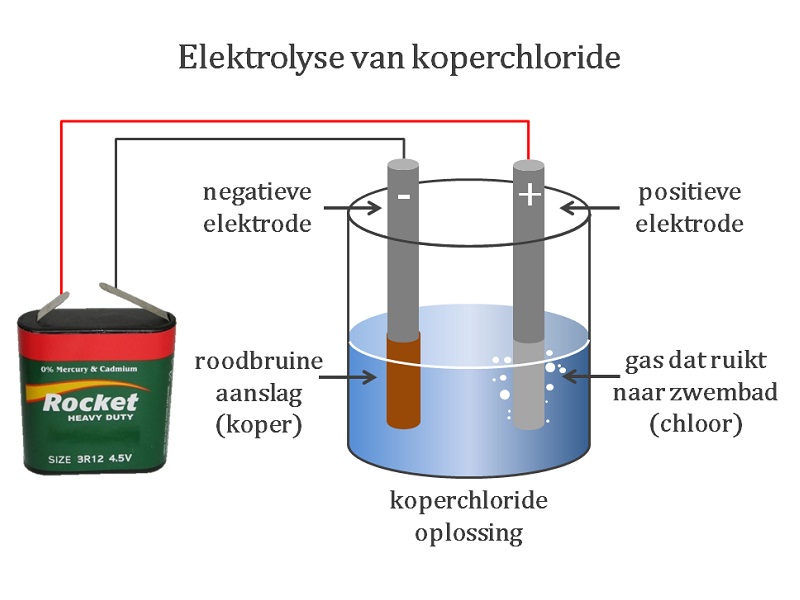
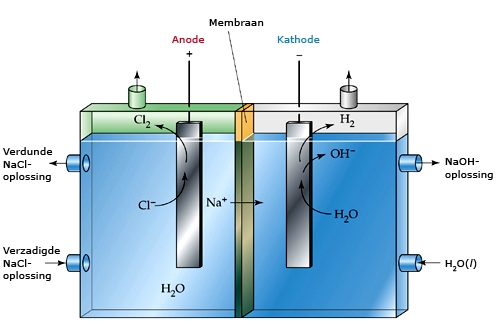
- Elektrolyse: Gebruikt voor het winnen van metalen uit ertsen (bijvoorbeeld aluminium) en het produceren van chemicaliën (zoals chloor). De anode is essentieel voor het proces.
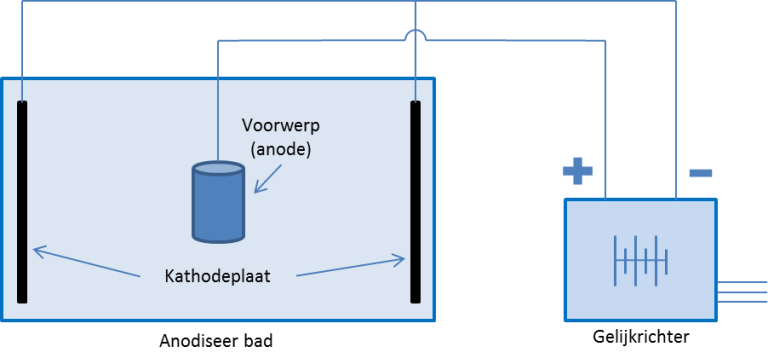
- Oppervlaktebehandeling: Anodiseren, een proces waarbij een beschermende oxidelaag op metalen wordt aangebracht (zoals aluminium), maakt gebruik van de anode als onderdeel van het proces. Dit verbetert de duurzaamheid en corrosiebestendigheid.
- Brandstofcellen: In brandstofcellen vindt oxidatie plaats aan de anode, waardoor elektriciteit wordt opgewekt. Een kritische technologie voor schone energie.
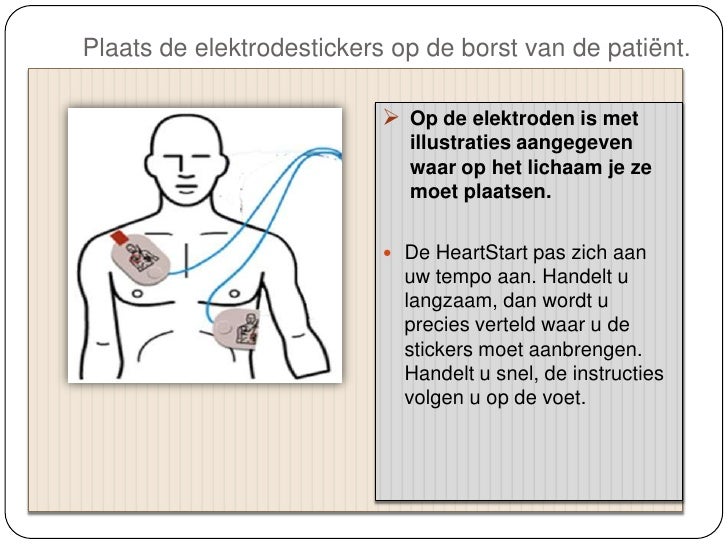
- Medische toepassingen: Elektroden worden gebruikt in medische apparaten voor het stimuleren van zenuwen en spieren, en ook voor het bewaken van de hartactiviteit. De positieve elektrode speelt hierbij een belangrijke rol.
Dus, of je nu je smartphone gebruikt, in een auto rijdt of een metalen constructie ziet met een beschermende laag, de kans is groot dat de principes van de elektrode aan de positieve pool een cruciale rol hebben gespeeld.
+reductor.jpg)
Kritische Beschouwingen en Alternatieve Perspectieven
Het is belangrijk om te erkennen dat er alternatieve materialen en ontwerpen zijn voor elektroden. Bijvoorbeeld, er is veel onderzoek naar nieuwe materialen voor batterijen, zoals lithium-zwavel of solid-state batterijen, die de prestaties en veiligheid kunnen verbeteren. Deze nieuwe technologieën proberen vaak de nadelen van traditionele materialen, zoals de beperkte levensduur of het potentieel voor oververhitting, te overwinnen.
Een ander punt van discussie is de milieu-impact van de materialen die worden gebruikt in elektroden. Het delven en verwerken van metalen zoals lithium en kobalt, die vaak in batterijen worden gebruikt, kan aanzienlijke milieuschade veroorzaken. Daarom is er een groeiende focus op recycling en het ontwikkelen van duurzamere materialen.
Sommige experts beweren dat de huidige afhankelijkheid van lithium-ion batterijen niet duurzaam is en dat er behoefte is aan meer diversificatie in de energieopslagtechnologieën. Alternatieven zoals waterstofbrandstofcellen en flowbatterijen worden actief onderzocht als potentiële oplossingen.
Oplossingen en Vooruitgang
De uitdagingen rond elektroden, en met name de anode, stimuleren innovatie. Er zijn verschillende oplossingen in ontwikkeling:
- Nieuwe materialen: Onderzoek naar materialen die goedkoper, overvloediger en milieuvriendelijker zijn, zoals natrium-ion batterijen of magnesium-ion batterijen.
- Verbeterde recyclingtechnologieën: Ontwikkelen van efficiëntere en effectievere manieren om materialen uit oude batterijen te recyclen.
- Duurzame productiemethoden: Het minimaliseren van de milieu-impact van de productie van elektroden door het gebruik van hernieuwbare energie en het verminderen van afval.
- Slimme batterijbeheersystemen: Het optimaliseren van het gebruik en de levensduur van batterijen door middel van geavanceerde software en sensoren.
- Alternatieve energieopslag: Investeren in onderzoek en ontwikkeling van alternatieve energieopslagtechnologieën, zoals waterstofbrandstofcellen en flowbatterijen.
Door te focussen op deze oplossingen kunnen we de prestaties, duurzaamheid en betaalbaarheid van energieopslag verbeteren, waardoor een meer duurzame toekomst mogelijk wordt.

Voorbeelden van Innovaties
- Siliconenanodes: Siliconen kunnen veel meer lithiumionen opslaan dan grafiet, wat leidt tot batterijen met een hogere energiedichtheid.
- Grafeen elektroden: Grafeen heeft een hoge elektrische geleidbaarheid en oppervlakte, wat het een veelbelovend materiaal maakt voor elektroden.
- 3D-geprinte batterijen: 3D-printen maakt het mogelijk om batterijen met complexe geometrieën te creëren, wat kan leiden tot een betere prestatie en efficiëntie.
Conclusie
De elektrode aan de positieve pool, de anode, is meer dan alleen een technisch detail. Het is een cruciaal onderdeel van technologieën die ons dagelijks leven vormgeven, van de batterijen in onze smartphones tot de brandstofcellen die de weg vrijmaken voor een schonere toekomst. Hoewel er uitdagingen zijn, zoals de milieu-impact van materialen en de behoefte aan betere prestaties, zijn er ook tal van innovatieve oplossingen in ontwikkeling die ons in staat stellen om deze uitdagingen te overwinnen.
Door te blijven investeren in onderzoek en ontwikkeling, recycling en duurzame productiemethoden, kunnen we de toekomst van energieopslag vormgeven en een meer duurzame wereld creëren.
Nu, met al deze informatie in gedachten, welke rol zie jij jezelf spelen in het stimuleren van een duurzamere toekomst als het gaat om energie en technologie?