Bij Welke Temperatuur Bevriest Water

Water, de levensader van onze planeet, is een stof die we dagelijks gebruiken en vaak als vanzelfsprekend beschouwen. Een van de meest fundamentele eigenschappen van water is de mogelijkheid om te bevriezen, een proces dat een cruciale rol speelt in het klimaat, de ecologie en tal van industriële toepassingen. Maar bij welke temperatuur gebeurt dit nu precies? Het antwoord is minder simpel dan je wellicht denkt.
Het Theoretische Vriespunt: 0 graden Celsius
In de schoolboeken leren we dat water bevriest bij 0 graden Celsius (32 graden Fahrenheit). Dit is het nominale vriespunt, vastgesteld onder standaardomstandigheden. Standaardomstandigheden verwijzen naar een specifieke luchtdruk (1 atmosfeer) en puur water, zonder verontreinigingen. In deze ideale situatie gaan watermoleculen, die in vloeibare vorm vrij bewegen, over in een geordende, vaste structuur – ijs – wanneer de kinetische energie daalt tot een punt waarop de aantrekkingskrachten tussen de moleculen de overhand krijgen.
De Invloed van Druk
Hoewel vaak genegeerd in dagelijkse situaties, speelt druk een significante rol in het vriespunt van water. Verhoogde druk verlaagt het vriespunt. Dit komt doordat ijs minder dicht is dan water. Door druk uit te oefenen wordt de vorming van het ijsrooster tegengehouden, waardoor het vriespunt daalt. Het effect is echter relatief klein bij normale drukvariaties. Diep in de oceanen, waar de druk enorm hoog is, kan het vriespunt van water aanzienlijk lager zijn dan 0 graden Celsius.
Must Read
De Rol van Verontreinigingen
De aanwezigheid van verontreinigingen, zoals zouten en mineralen, heeft een veel grotere invloed op het vriespunt. Dit fenomeen staat bekend als vriespuntdepressie. De verontreinigingen verstoren de vorming van de ijskristalstructuur, waardoor er meer energie (dus een lagere temperatuur) nodig is om de overgang van vloeibaar naar vast te bewerkstelligen.
Vriespuntdepressie: Een Diepere Uitleg
Vriespuntdepressie is een colligatieve eigenschap, wat betekent dat de mate van depressie afhangt van de concentratie van de opgeloste deeltjes, niet van de aard van de deeltjes zelf. Hoe meer zout je aan water toevoegt, hoe lager het vriespunt wordt. Deze eigenschap wordt op grote schaal gebruikt in de praktijk.

Zout Strooien in de Winter
Een alledaags voorbeeld is het strooien van zout op wegen in de winter. Het zout vermengt zich met het ijs of de sneeuw en vormt een zoutwateroplossing. Deze oplossing heeft een lager vriespunt dan puur water, waardoor het ijs smelt, zelfs als de temperatuur onder nul is. De effectiviteit van zout strooien is echter beperkt. Bij temperaturen onder ongeveer -10 graden Celsius is het effect van zout minimaal, omdat de benodigde hoeveelheid zout om het vriespunt significant te verlagen dan te groot wordt.
Antivries in Auto's
Een ander belangrijk voorbeeld is het gebruik van antivries in auto's. Antivries, meestal ethyleenglycol, wordt aan het koelwater toegevoegd om het vriespunt te verlagen. Hierdoor kan de motor, zelfs bij strenge vorst, niet bevriezen en beschadigd raken. Tegelijkertijd verhoogt antivries ook het kookpunt van het koelwater, waardoor oververhitting in de zomer wordt voorkomen. De juiste concentratie antivries is cruciaal voor optimale bescherming.

Onderkoeling: Vloeibaar Water Onder Nul
Een fascinerend fenomeen is onderkoeling, waarbij water in vloeibare toestand blijft, zelfs onder het nominale vriespunt van 0 graden Celsius. Dit kan gebeuren als het water zeer zuiver is en er geen nucleatiepunten aanwezig zijn. Nucleatiepunten zijn kleine onzuiverheden of oppervlakken waarop ijskristallen kunnen beginnen te vormen. Zonder deze nucleatiepunten kunnen de watermoleculen niet gemakkelijk een ijskristalstructuur vormen, zelfs bij temperaturen onder nul.
Onderkoeling in de Natuur
Onderkoeling komt ook in de natuur voor. Bijvoorbeeld, in wolken kunnen kleine waterdruppeltjes onderkoeld zijn. Wanneer deze onderkoelde druppeltjes in contact komen met een object, zoals een vliegtuigvleugel of een boomtak, kunnen ze onmiddellijk bevriezen, waardoor ijsafzetting ontstaat. Dit kan gevaarlijke situaties opleveren, bijvoorbeeld voor vliegtuigen die in ijzel terechtkomen.

Praktische Toepassingen van Onderkoeling
Onderkoeling wordt ook in de praktijk gebruikt, bijvoorbeeld bij het koelen van organen voor transplantatie. Door organen snel af te koelen tot onderkoelde temperaturen kunnen ze langer bewaard worden zonder dat ze beschadigd raken door ijskristalvorming. Dit vergroot de tijdspanne waarin een orgaan getransplanteerd kan worden en vergroot de kans op een succesvolle transplantatie.
Real-World Data en Metingen
Wetenschappers hebben uitgebreide metingen verricht om de exacte relatie tussen temperatuur, druk en zoutgehalte en het vriespunt van water te bepalen. Oceanografische studies tonen aan dat het vriespunt van zeewater in de diepzee, vanwege de hoge druk en het zoutgehalte, kan dalen tot ongeveer -2 graden Celsius. Laboratoriumexperimenten hebben aangetoond dat zeer zuiver water onder ideale omstandigheden kan worden onderkoeld tot temperaturen van -40 graden Celsius voordat spontane ijsvorming optreedt.
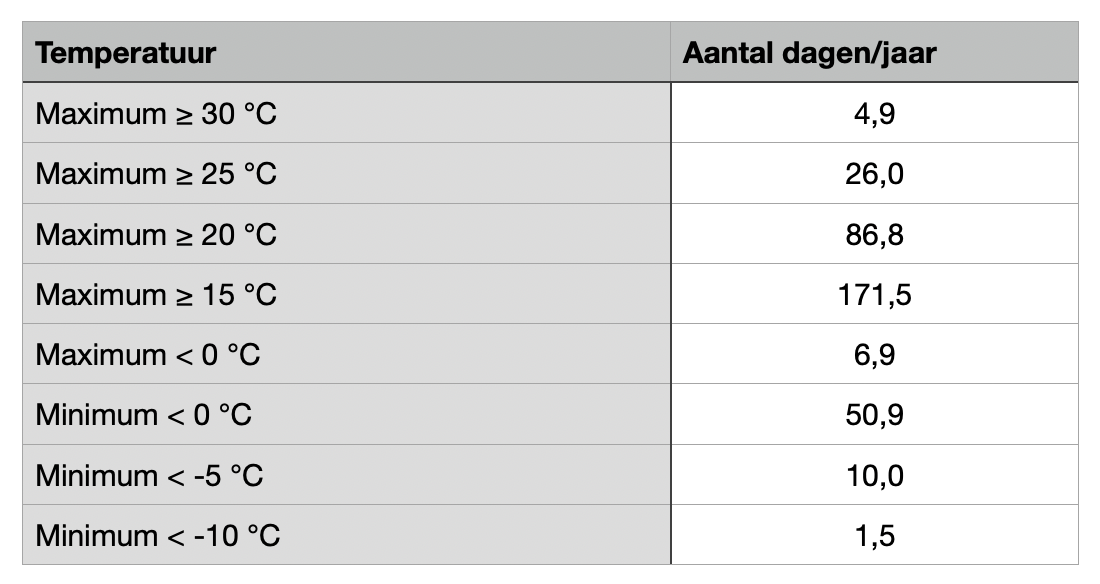
Data van het KNMI
Het KNMI (Koninklijk Nederlands Meteorologisch Instituut) verzamelt continu data over temperaturen, neerslag en ijsvorming in Nederland. Deze data wordt gebruikt om weersvoorspellingen te maken en om de effecten van klimaatverandering op de waterhuishouding te bestuderen. Door het analyseren van langjarige temperatuurreeksen kan het KNMI inzicht krijgen in de frequentie en de intensiteit van vorstperiodes en de impact hiervan op bijvoorbeeld de scheepvaart en de landbouw.
Conclusie: Meer dan Alleen 0 Graden
Het vriespunt van water is dus geen absolute constante. Hoewel 0 graden Celsius een nuttige referentie is, wordt het daadwerkelijke vriespunt beïnvloed door factoren zoals druk, verontreinigingen en de aanwezigheid van nucleatiepunten. Het begrijpen van deze factoren is cruciaal voor diverse toepassingen, van het voorkomen van ijsvorming op wegen tot het bewaren van organen voor transplantatie.
Dus, de volgende keer dat je ijs ziet, denk dan even na over de complexe fysica en chemie die hieraan ten grondslag liggen. Experimenteer zelf! Voeg zout toe aan water en kijk wat er met het vriespunt gebeurt. Onderzoek verder en ontdek de vele fascinerende aspecten van deze alledaagse, maar toch zo bijzondere stof: water.




+bevriest..jpg)