Atomic Mass And Atomic Number

Heb je je ooit afgevraagd waaruit de wereld om ons heen is opgebouwd? Het is een vraag die wetenschappers al eeuwen bezighoudt. Het antwoord ligt in de atomen, de minuscule bouwstenen van alle materie. Maar om atomen echt te begrijpen, moeten we dieper duiken in concepten als atoommassa en atoomnummer. Het kan in eerste instantie wat intimiderend lijken, maar geloof me, met een beetje uitleg wordt het allemaal helderder.
Veel mensen raken in de war door de termen atoommassa en atoomnummer. Ze klinken misschien ingewikkeld, maar ze zijn eigenlijk heel belangrijk om de eigenschappen van elementen te begrijpen. Stel je voor: je probeert een recept te volgen, maar je hebt geen idee hoeveel van elk ingrediënt je nodig hebt. Dat is vergelijkbaar met het proberen te begrijpen van chemische reacties zonder kennis van atoommassa en atoomnummer. Ze geven ons de essentiële informatie die we nodig hebben om te begrijpen hoe atomen zich gedragen en hoe ze interactie met elkaar hebben.
Wat is het Atoomnummer?
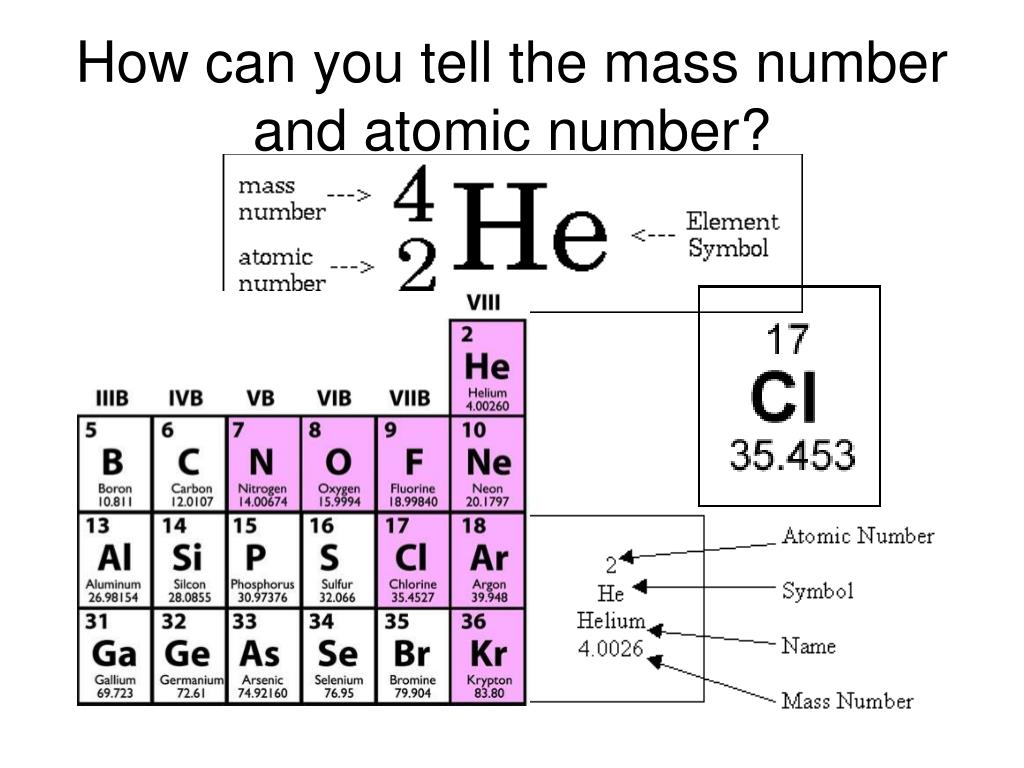
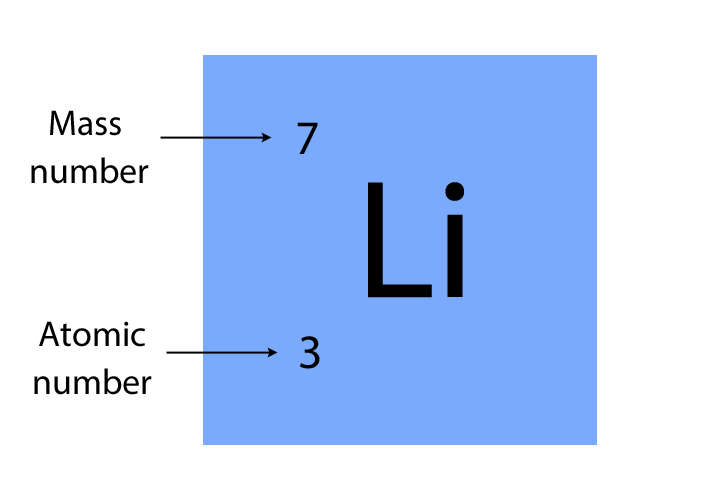
Laten we beginnen met het atoomnummer. Het atoomnummer is een uniek nummer dat elk element identificeert. Het is alsof elk element een eigen postcode heeft. Concreet is het atoomnummer het aantal protonen in de kern van een atoom.
Must Read
Protonen zijn positief geladen deeltjes die zich in de kern (nucleus) van het atoom bevinden. Het aantal protonen bepaalt welk element we bekijken. Bijvoorbeeld:
- Waterstof (H) heeft 1 proton, dus het atoomnummer is 1.
- Helium (He) heeft 2 protonen, dus het atoomnummer is 2.
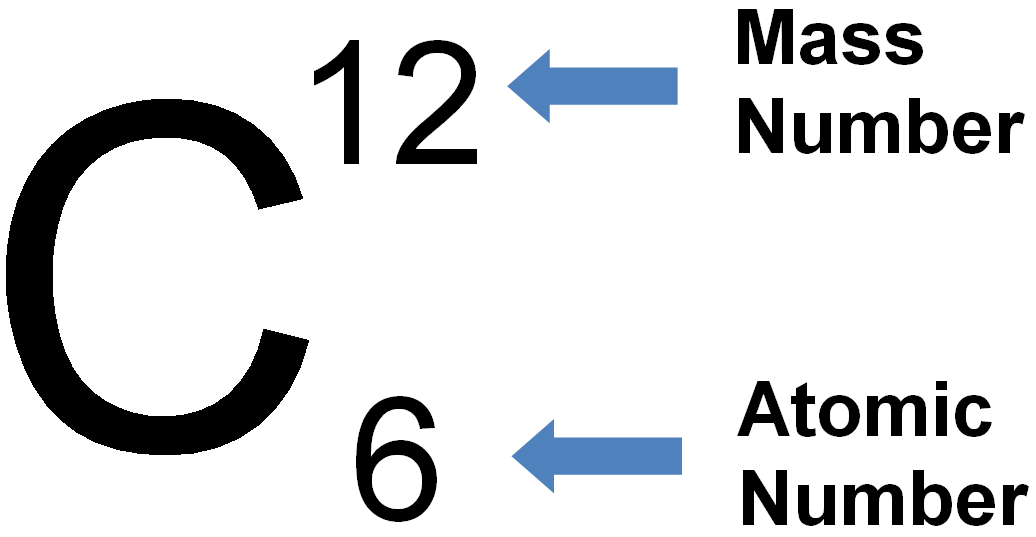
- Koolstof (C) heeft 6 protonen, dus het atoomnummer is 6.
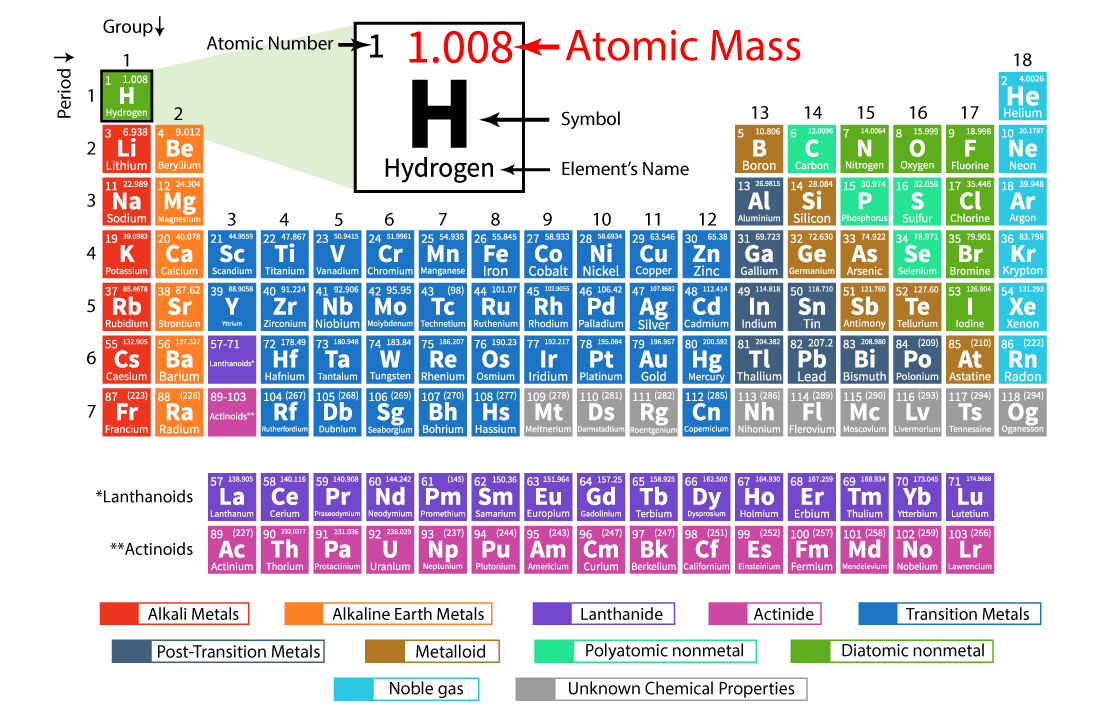
Het atoomnummer is zo belangrijk omdat het de basis vormt voor de positie van een element in het periodiek systeem. Het periodiek systeem is geordend op basis van toenemend atoomnummer, waardoor elementen met vergelijkbare eigenschappen in dezelfde kolom (groep) terechtkomen. Je kunt dus direct aan het atoomnummer zien waar een element zich bevindt en daardoor al iets afleiden over de te verwachten eigenschappen. Handig, toch?
Belangrijk: Het atoomnummer verandert nooit voor een specifiek element. Als het aantal protonen verandert, verandert het element zelf! Dit is een fundamenteel principe in de chemie.
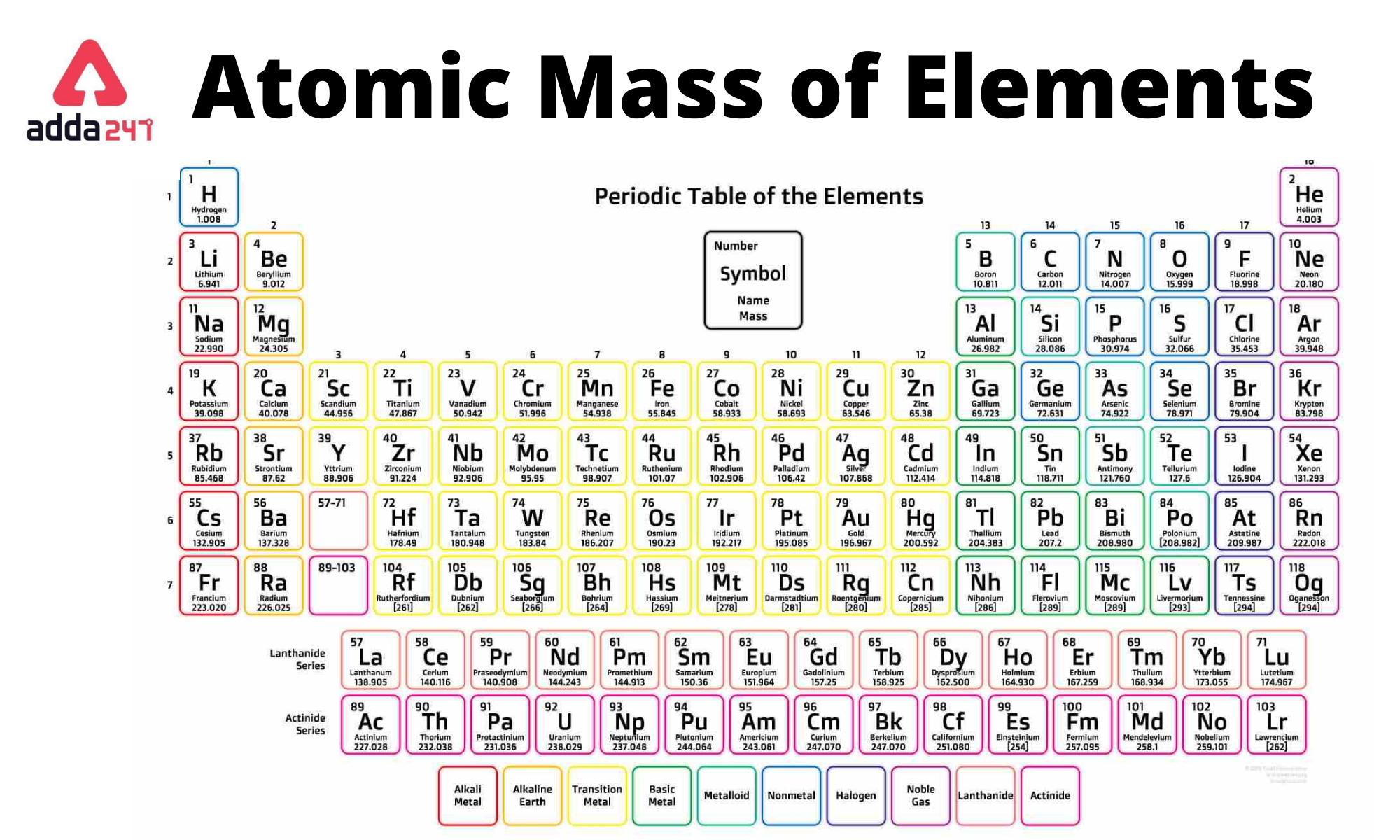
Wat is Atoommassa?
Nu gaan we het hebben over atoommassa. Atoommassa is de totale massa van een atoom, gemeten in atomaire massa-eenheden (amu), of in sommige contexten, Dalton (Da). Het is in feite het gewicht van het atoom. Het wordt voornamelijk bepaald door de massa van de protonen en neutronen in de kern.
Neutronen zijn neutrale deeltjes (ze hebben geen lading) die zich ook in de kern van het atoom bevinden. Ze dragen significant bij aan de massa van het atoom, maar ze beïnvloeden niet het type element (dat wordt bepaald door het aantal protonen).
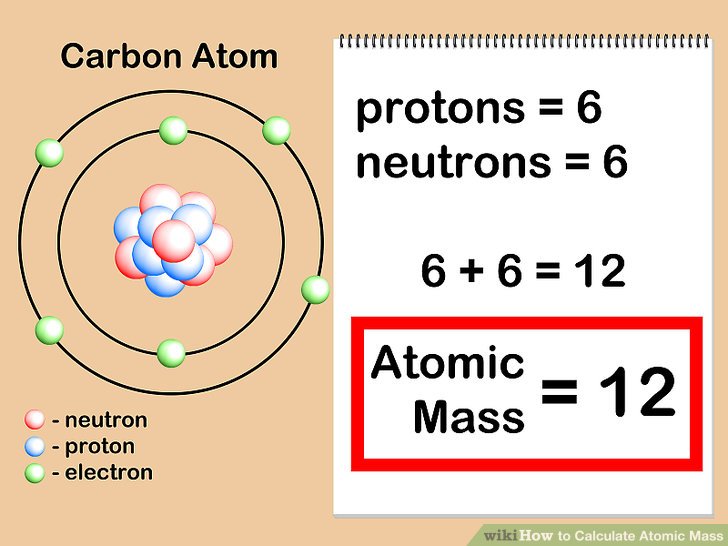
De atoommassa wordt berekend door het aantal protonen en neutronen in de kern bij elkaar op te tellen. Bijvoorbeeld, een koolstofatoom met 6 protonen en 6 neutronen heeft een atoommassa van ongeveer 12 amu (6 + 6 = 12).

Let op: De massa van elektronen is zo klein in vergelijking met protonen en neutronen dat ze in de meeste berekeningen worden genegeerd.
Isotopen en Atoommassa
Nu wordt het iets complexer. De meeste elementen bestaan in verschillende vormen, zogenaamde isotopen. Isotopen hebben hetzelfde aantal protonen (dus hetzelfde atoomnummer), maar een verschillend aantal neutronen. Dit betekent dat isotopen van hetzelfde element een andere atoommassa hebben.
Bijvoorbeeld, koolstof (C) heeft twee belangrijke isotopen: koolstof-12 (12C) en koolstof-14 (14C). 12C heeft 6 protonen en 6 neutronen (atoommassa 12), terwijl 14C 6 protonen en 8 neutronen heeft (atoommassa 14). Ze zijn allebei koolstof, maar ze verschillen in hun aantal neutronen.

Omdat elementen meestal bestaan uit een mengsel van verschillende isotopen, gebruiken we de gemiddelde atoommassa. Dit is het gewogen gemiddelde van de atoommassa's van alle natuurlijke isotopen van een element, rekening houdend met hun relatieve abundantie (hoe vaak ze voorkomen). Deze waarde staat meestal vermeld onder het elementsymbool in het periodiek systeem.
Stel je voor dat je een mand vol appels hebt. Sommige zijn klein (100 gram), andere zijn groot (150 gram). Om de gemiddelde massa van een appel te bepalen, tel je niet gewoon de kleinste en de grootste bij elkaar op en deel je door twee. Je moet ook rekening houden met hoeveel kleine appels en hoeveel grote appels je hebt. De gemiddelde atoommassa is hetzelfde principe, toegepast op atomen en hun isotopen.
Waarom zijn Atoommassa en Atoomnummer Belangrijk?
De kennis van atoommassa en atoomnummer is essentieel voor tal van toepassingen in de wetenschap en technologie:

- Chemie: Ze helpen bij het berekenen van de hoeveelheden stoffen die nodig zijn voor chemische reacties (stoichiometrie). Ze zijn cruciaal bij het begrijpen van chemische bindingen en reactiemechanismen.
- Natuurkunde: Ze spelen een rol bij kernreacties, radioactief verval en de studie van de atoomkern.
- Biologie: Isotopen worden gebruikt in tracer-experimenten om biologische processen te volgen en te bestuderen. Denk bijvoorbeeld aan C14 datering.
- Geneeskunde: Radioactieve isotopen worden gebruikt in medische beeldvorming (scans) en radiotherapie.
- Materiaalkunde: De eigenschappen van materialen worden beïnvloed door de atomen waaruit ze zijn opgebouwd, en dus door hun atoommassa en atoomnummer.
Met de info over atoommassa en atoomnummer kun je bijvoorbeeld voorspellen hoe elementen met elkaar reageren. Denk aan de reactie van natrium (Na) met chloor (Cl) om keukenzout (NaCl) te vormen. Door hun atoomstructuur te begrijpen, kunnen we voorspellen dat natrium een elektron zal afstaan aan chloor, waardoor een ionische binding ontstaat.
Samenvatting
Laten we de belangrijkste punten nog eens kort samenvatten:
- Atoomnummer: Het aantal protonen in de kern van een atoom. Dit bepaalt welk element het is.
- Atoommassa: De totale massa van een atoom, voornamelijk bepaald door de massa van de protonen en neutronen in de kern.
- Isotopen: Atomen van hetzelfde element met een verschillend aantal neutronen (en dus een verschillende atoommassa).
- Gemiddelde atoommassa: Het gewogen gemiddelde van de atoommassa's van alle natuurlijke isotopen van een element.
Hopelijk heb je nu een beter begrip van atoommassa en atoomnummer. Het zijn fundamentele concepten die de basis vormen voor het begrip van de chemie en de wereld om ons heen. Blijf nieuwsgierig en blijf leren!
Dus, de volgende keer dat je iets in je dagelijks leven gebruikt, denk dan even aan de kleine atomen waaruit het is opgebouwd, en bedenk hoe essentieel hun atoommassa en atoomnummer zijn voor de eigenschappen die het object bezit!


![Nucleons, Atomic Number and Mass Number - Definition [with Examples]](https://d1avenlh0i1xmr.cloudfront.net/75a79509-2b1a-4ced-a3bd-c624d63558e9/33.-atomic-no.-and-mass-no-teachoo-01.png)



:max_bytes(150000):strip_icc()/atomic-mass-and-mass-number-606105_v1-80df956ab98440bc9969531d1bb6c874.png)