1 Mol Is Hoeveel Gram

Oké, laten we het even hebben over iets wat in eerste instantie klinkt als een of andere scheikundige marteling: "Mol is hoeveel gram?". Klinkt ingewikkeld, toch? Maar geloof me, het is minder eng dan een spin in je badkamer (en waarschijnlijk nuttiger dan een hoop van de dingen die je op Netflix kijkt).
Wat is die Mol eigenlijk?
Denk aan de mol als een soort mega-dozijn. We weten allemaal wat een dozijn is: 12 stuks. Twaalf eieren, twaalf donuts (mmmm, donuts...). Een mol is net zoiets, maar dan veel groter. Het is 6.022 x 1023 deeltjes. Ja, dat lees je goed. Een belachelijk groot aantal. Waarom zo groot? Omdat atomen en moleculen piepklein zijn. Zo klein, dat we er een gigantische hoeveelheid van nodig hebben om er iets mee te kunnen doen dat we kunnen zien, wegen of gebruiken.
Stel je voor: je wilt een taart bakken, en het recept zegt: "Gebruik 1 mol suiker". Nou, je kunt je voorstellen dat je dan een zwembad vol suiker nodig hebt. Misschien een olympisch zwembad. (Ik zeg niet dat je dat moet doen, graag niet doen.)
Must Read
Waarom hebben we die Mol nodig?
Goede vraag! Scheikunde is eigenlijk een soort receptenboek, maar dan voor het maken van alles, van medicijnen tot plastic bekers. Die recepten werken alleen als we de juiste verhoudingen gebruiken. Dus, in plaats van te zeggen "gebruik 1 atoom van dit en 2 atomen van dat", gebruiken we de mol. De mol is als een universele taal voor scheikundigen. Het helpt ze te communiceren over hoeveel ze van elk ingrediënt nodig hebben.
Stel je voor dat je een recept voor pannenkoeken hebt. Het recept zegt: "2 eieren, 1 kopje bloem, 1 kopje melk". Je zou nooit zeggen: "Gebruik 2 moleculen ei, 1 molecuul bloem, 1 molecuul melk". Dat zou onzin zijn! De mol doet eigenlijk hetzelfde voor scheikunde. Het maakt het praktisch.
Mol en Grammen: De Relatie
Hier komt de connectie: de molaire massa. Elke stof heeft een molaire massa, en die vind je terug in het periodiek systeem. De molaire massa vertelt je hoeveel gram één mol van die stof weegt.
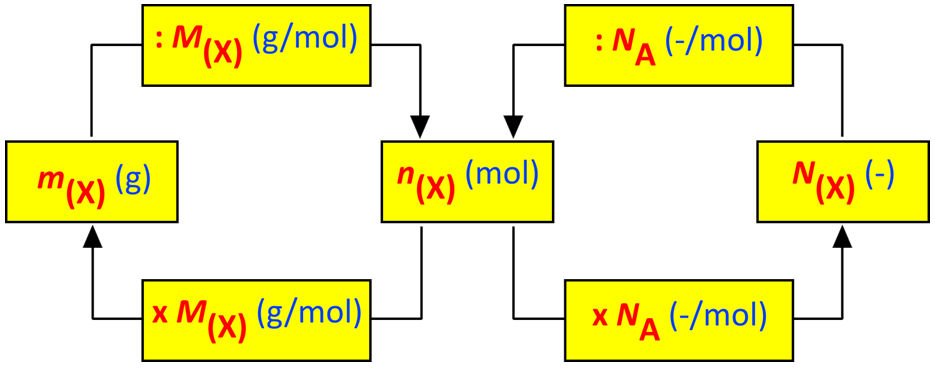
Bijvoorbeeld: de molaire massa van koolstof (C) is ongeveer 12 gram per mol. Dat betekent dat 6.022 x 1023 koolstofatomen (dus 1 mol koolstof) 12 gram weegt. Simpel, toch? (Oké, misschien niet meteen simpel, maar na een paar kopjes koffie wel!)
Dus, als je wilt weten hoeveel gram 0.5 mol koolstof weegt, dan is dat de helft van 12 gram, dus 6 gram.
Even een Stapje Verder: Water (H2O)
Laten we het even hebben over water. Water is H2O, dus twee waterstofatomen en één zuurstofatoom. De molaire massa van waterstof (H) is ongeveer 1 gram per mol, en de molaire massa van zuurstof (O) is ongeveer 16 gram per mol.

Dus, de molaire massa van water is (2 x 1) + 16 = 18 gram per mol. Dit betekent dat 6.022 x 1023 watermoleculen (dus 1 mol water) 18 gram weegt.
Stel je voor dat je een klein flesje water hebt dat 18 gram water bevat. Dat flesje bevat dus precies 1 mol watermoleculen. Zo zie je maar, het is best tastbaar!
Hoe gebruik je dit in de praktijk?
Oké, je denkt nu misschien: "Leuk verhaal, maar wat heb ik hieraan in mijn dagelijks leven?". Nou, misschien bak je geen medicijnen in je keuken (hoop ik niet!). Maar het principe achter de mol wordt gebruikt in heel veel industrieën.

- Medicijnen: Om de juiste dosis te bepalen is precisie essentieel. De mol helpt apothekers en farmaceutische bedrijven om de juiste hoeveelheid werkzame stof in een pil te stoppen.
- Landbouw: Om te bepalen hoeveel meststoffen nodig zijn voor een optimale groei van gewassen, gebruiken boeren en landbouwkundigen kennis van de mol om de juiste verhoudingen van voedingsstoffen toe te dienen.
- Voedselindustrie: Om de juiste verhouding van ingrediënten in een voedingsproduct te bepalen.
- Materialen: Om nieuwe materialen te ontwikkelen met specifieke eigenschappen.
Denk er maar aan dat de volgende keer dat je een pil slikt, iemand de mol heeft gebruikt om ervoor te zorgen dat je de juiste dosis krijgt. Je kunt gerust zijn!
Een grappige anekdote
Ik herinner me een keer dat ik probeerde een recept na te maken voor een of andere fancy cocktail. Het recept zei: "Gebruik 0.01 mol van een bepaalde chemische stof" (natuurlijk niet iets gevaarlijks!). Ik had geen flauw idee hoeveel dat was, dus ik begon te gokken. Uiteindelijk smaakte de cocktail naar afwasmiddel. Les geleerd: de mol is belangrijk, zelfs bij cocktails!
Conclusie: De Mol is je Vriend (eigenlijk...)
De mol is misschien een beetje intimiderend in het begin, maar het is eigenlijk een heel handig concept. Het helpt ons om atomen en moleculen te kwantificeren, en het maakt het mogelijk om nauwkeurige recepten te maken voor alles, van medicijnen tot taarten. Dus, de volgende keer dat je de mol hoort, hoef je niet meer weg te rennen. Denk er gewoon aan als een mega-dozijn, en je bent al halverwege!

Onthoud dit:
- Een mol is een enorme hoeveelheid deeltjes (6.022 x 1023).
- De molaire massa vertelt je hoeveel gram één mol van een stof weegt.
- De mol is essentieel voor scheikunde en veel andere industrieën.
En het belangrijkste: wees niet bang om vragen te stellen! Scheikunde is soms een beetje gek, maar het is ook fascinerend.
Dus, ga ervoor, omarm de mol, en wie weet, misschien ontdek je wel je innerlijke scheikundige! (Of op zijn minst, leer je hoe je betere cocktails maakt).


+van+een+stof+is+in+getalwaarde+gelijk+aan+de+molecuulmassa+of+atoommassa+van+de+stof..jpg)










+Liters+of+GAS+(at+STP).jpg)
